Искусственное дыхание |
||
 |
 |
Оглавление
|
Искусственное дыханиеИскусственное дыхание (синоним: искусственная вентиляция легких, управляемая вентиляция легких, контролируемая вентиляция легких, управляемое дыхание) — перемежающаяся или непрерывная замена воздуха в легких искусственными методами при прекращении или недостаточности естественной вентиляции. Существует мнение, что искуственное дыхание и искусственная вентиляция легких — два различных понятия. Искусственная вентиляция легких замещает только одну стадию процесса дыхания — вентиляцию, влияя на остальные — альвеолокапиллярную диффузию газов, легочный кровоток, тканевой газообмен — лишь опосредованно. К искуственному дыханию относят способы управления окислительно-восстановительным метаболизмом внелегочными путями: парапульмональную оксигенацию (энтеральную, артериальную), введение ферментов и энергетических веществ, улучшающих тканевое окисление, подавление метаболизма гипотермией, гибернацией и другим. В данной статье дается традиционно сложившееся изложение понятия искуственного дыхания как процесса обмена газа между альвеолярным воздухом и атмосферным. Искусственное дыхание, искусственная вентиляция легких.Оглавление 2 — Физиологическое воздействие 3 — Показания и противопоказания 6 — Особенности искусственного дыхания в различных условиях Искуственное дыхание осуществляется перемежающимся введением воздуха в легкие и удалением его, что достигается двумя различными группами методов: вдуванием (инсуффляцией) воздуха в дыхательные пути (искусственное дыхание по принципу вдувания) или изменением формы и объема грудной клетки (наружные, внешние методы искусственного дыхания). Ту и другую группу методов можно применять как с использованием инструментов и аппаратов, так и без них. Особой формой искусственного дыхания является так наз. диффузионное дыхание, при котором кислород непрерывно поступает в дыхательные пути на фоне апноэ, в отличие от перемежающегося (вдох — выдох) искусственного дыхания. Применение искусственного дыхания требуется при внезапном или постепенном прекращении естественной (спонтанной) вентиляции из-за травмы, болезни, клинической смерти, а также при плановом выключении вентиляции во время общей анестезии или интенсивной терапии. В истории применения искусственного дыхания можно выделить два принципиально различных периода. Первый — от глубокой древности до середины 20 в., когда искусственное дыхание применялось только для оживления или поддержания жизни при внезапном прекращении дыхания. Искусственное дыхание сравнительно широко использовалось для оживления новорожденных, при утоплении и других несчастных случаях и внезапных заболеваниях. В этот период искусственное дыхание применяли только по срочным показаниям и на короткий срок. |
Со второй половины 20 в. искусственное дыхание стали применять не только при несчастном случае или внезапном заболевании, но и в плановом порядке — для выключения спонтанной вентиляции при различных оперативных вмешательствах и методах анестезии, для многосуточной интенсивной терапии различных терминальных состояний и для многомесячной заместительной терапии при некоторых заболеваниях нервной и мышечной системы. Новые требования привели к модернизации старых и появлению новых методов искусственного дыхания.
Исторически более ранними и более широко применяющимися для искусственного дыхания являются методы вдувания воздуха в легкие (экспираторные методы): оживляющий вдувает в дыхательные пути больного выдыхаемый им самим воздух. Такой метод широко применяли в акушерстве для оживления новорожденных еще в 17 в. Впервые в медицинской литературе подробно описал успешное применение этого метода искусственного дыхания англ. хирург Тосса (W. Tossah) в 1732 г. Техника метода описана в 1766 г. С. Г. Зыбелиным. В 1796 г. Херхолт и Рафн (J. D. Негholdt, G. G. Rafn) исследовали данный метод в клинических и физиологических аспектах и рекомендовали его для широкого применения. Большую роль в развитии экспираторных и иных методов искусственного дыхания сыграли общества спасения утонувших, созданные в 17 —19 вв. в различных странах.
С середины 19 до 50-х гг. 20 в. экспираторные методы искусственного дыхания были вытеснены так называемым ручными методами, основанными на изменении объема грудной клетки приложением внешнего усилия. Элам (J. О. Elam, 1965) полагает, что главной причиной отказа от экспираторных методов искусственного дыхания изо рта в рот и изо рта в нос были эстетические соображения. Впервые ручные методы сжатия грудной клетки и живота для искусственного дыхания применил во Франции в 1829 г. Леруа Д′Этуаль (Leroy D′Etoilles). В последующем широкое распространение в медицинской практике получили многократно сменяющие друг друга ручные способы иск. дыхания Холла (М. Hall, 1856), Сильвестра (Н. Silvester, 1858), Шефера (Е. A. Schafer, 1904), Нильсена (Н. Nielsen, 1932) и их многочисленные модификации, имеющие лишь историческое значение.
В 50-х гг. 20 в. применение ручных методов искуственного дыхания резко сократилось по многим причинам. Во-первых, они не обеспечивали проходимость верхних дыхательных путей. Во-вторых, эффективность этих методов, то есть объемы обеспечиваемой ими вентиляции, оказалась невелика. Сравнение, проведенное в 1946 г. Макинтошем и Машин (R. R. Macintosh, W. W. Mushin), показало, что экспираторный метод искусственного дыхания дает, по крайней мере вдвое большие объемы вентиляции, чем способы качания Шефера, Сильвестра. Сафар (P. Safar, 1958) сообщил, что при использовании различных ручных методов иск. дыхания обеспечить больному дыхательный объем 500 мл смогли от 14 до 50% специально тренированных людей, тогда как при использовании экспираторных методов тот же объем вентиляции смогли дать 89—100% даже не прошедших подготовки людей. Подробную сравнительную оценку достоинств и недостатков различных ручных способов искусственного дыхания провел Г. А. Степанский (1960), который полагает, что большинство ручных способов искуственного дыхания утомительно (третья причина, по которой эти методы были оставлены). Вчетвертых, способы ручного искуственного дыхания, при которых пострадавший лежит не на спине, не позволяют одновременно с искусственным дыханием проводить массаж сердца. Один лишь факт существования более 120 ручных способов искуственного дыхания свидетельствует об их недостаточной эффективности.
Малая эффективность ручных способов искуственного дыхания и повреждения грудной стенки и органов живота, нередко сопровождающие их, привели к восстановлению в медицинской практике экспираторных методов. Начиная с сообщения Элама с соавторами (1954) появились многочисленные исследования, реабилитирующие незаслуженно забытые экспираторные методы искуственного дыхания, что привело к почти полному вытеснению из повседневной практики ручных способов. Последние применяют лишь при невозможности использовать экспираторные методы и отсутствии каких бы то ни было приборов и инструментов, если надо провести искуственное дыхание при инфекционных заболеваниях, отравлениях газообразными боевыми отравляющими и боевыми радиоактивными веществами.
Как для методов вдувания, так и для внешних методов искуственного дыхания с давних пор применяли различные инструменты и аппараты. Для облегчения экспираторного метода искуственного дыхания уже в 18 в. применяли специальные воздуховоды и маски. Так Парацелъс использовал для вдувания в легкие воздуха каминные мехи, а А. Везалий применял аналогичный прибор, как для вдувания, так и для активного удаления воздуха из легких. Дж. Гунтер в 1776 г. предложил для искуственного дыхания двойной мех с клапаном, а Гудвин (Goodwyn, 1788) рекомендовал для тех же целей кислород вместо воздуха.
С начала 19 века появляются автоматические респираторы; первый из них был выпущен фирмой «Дрегер» в Германии (1911). Эпидемии полиомиелита в 30—50 -х гг. 20 века способствовали развитию многочисленных методов и созданию аппаратов для наружного искуственного дыхания. В 1929 г. Дринкери и Шо (Ph. Drinker, L.A.Shaw) предложили боксовый (танковый, «железные легкие») респиратор, в котором вокруг тела больного создавалось перемежающееся разрежение и положительное давление, обеспечивающее вдох и выдох. В 1937 г. появился первый кирасный респиратор, создававший перепады давления только вокруг грудной клетки и живота больного. Эти приборы многократно усовершенствовались и видоизменялись. В 1932 г. Ив (F. С. Eve) предложил «качающийся респиратор», в котором тело больного раскачивалось вокруг горизонтальной оси: при поднятии головного конца на 20—30° диафрагма смещалась в сторону живота — происходил вдох, при опускании — выдох. Способ качания Ива практически не применяется из-за громоздкости, неблагоприятного влияния на гемодинамику и нередкого пассивного затекания желудочного содержимого в носоглотку с последующей аспирацией. Постепенно наружные (нательные, внешние) респираторы были вытеснены респираторами вдувания, которые обеспечивали более эффективную вентиляцию, оказались менее громоздкими и не затрудняли доступ к больному для проведения различных манипуляций. В 50-х гг. 20 века Сарнов (S. J. Sarnoff) с соавторами (1950) ввели в практику электрофренический метод искусственного дыхания — ритмичную электростимуляцию диафрагмальных нервов или диафрагмы, сокращение которой обеспечивает вдох. Продолжается совершенствование электрофренического метода по параметрам тока (частота, продолжительность, форма и амплитуда импульса), надежности электростимуляторов и электродов. Однако широкого распространения метод не получил главным образом из-за сравнительно быстро возникающей «усталости» нерва или нервно-мышечного синапса и нестабильности в связи с этим режима искусственного дыхания.
Помимо изменений, возникающих в организме в результате адекватного или неадекватного обмена воздуха в легких, искусственное дыхание прямо или косвенно влияет на различные функции организма главным образом благодаря механическому эффекту и связанным с ним рефлекторным реакциям.
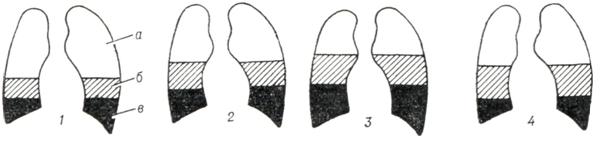
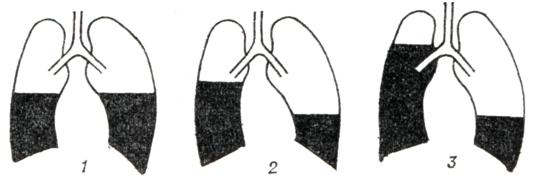
Механика дыхания меняется в зависимости от метода и режима искусственного дыхания. При искусственном дыхании по принципу вдувания вдох осуществляется благодаря принудительному нагнетанию воздуха в легкие, при раздувании которых расширяется грудная клетка, тогда как при спонтанной вентиляции первичным является расширение грудной клетки с увеличением разрежения в плевральной полости, благодаря чему в легкие поступает воздух. Характеристика процессов, происходящих в легких при различных видах искусственного дыхания по принципу вдувания, представлена на рисунке 1. Внутрилегочное давление в конце вдоха бывает при искусственном дыхании +15, +20 см водного столба, а при спонтанной вентиляции 0, — 1 см водного столба. Внутри-плевральное давление в тот же момент равно соответственно +3 и —10 см водного столба. В конце выдоха как при искусственном дыхании с пассивным выдохом, так и при спонтанной вентиляции внутрилегочное давление бывает 0, + 1 см водного столба, а внутриплевральное —5 см водного столба. При искусственном дыхании с активным выдохом, то есть при отсасывании воздуха из легких, внутрилегочное и внутриплевральное давление в конце искусственного выдоха отличается от показателей при спонтанной вентиляции. Благодаря этим различиям транспульмональное давление (разность между внутрилегочным и внутриплевральным давлением) при искусственном дыхании и спонтанной вентиляции различно, а именно транспульмональное давление является движущей силой вентиляции. Более близкая к естественной динамика внутрилегочного и внутриплеврального давлений во время дыхательного цикла возникает при использовании внешних методов искусственного дыхания, например кирасных и боксовых респираторов, а также электрофренического метода. Однако и здесь не наблюдается абсолютно сходных величин, потому что искусственное и естественное расширение грудной клетки не равнозначны: в естественных условиях вентиляция отдельных легочных зон и, соответственно, плевральное давление имеют четкие региональные различия. Кроме того, кирасные и боксовые респираторы нарушают естественную динамику внутрилегочного и внутриплеврального давлений из-за большей податливости брюшной стенки по сравнению с грудной клеткой.
Благодаря различию абсолютных величин и динамики транспульмонального давления при искусственном дыхании и спонтанной вентиляции механика вдоха и выдоха меняется: это относится и к растяжимости легких — гудной клетки (эластическое сопротивление), и к аэродинамическому сопротивлению дыхательных путей, и к деформационному (тканевому) сопротивлению легких и грудной клетки. Лишь четвертый вид общего дыхательного сопротивления — инерционное — как при спонтанной вентиляции, так и при искусственном дыхании одинаково зависит от массы движущихся органов и возникающих ускорений (частоты дыхания). Известно, что при длительном искусственном дыхании растяжимость легких постепенно снижается. Это происходит из-за ателектазирования различных зон легких в связи с нарушением дренажной функции, патологии вентиляционно-перфузионным соотношением, деструкцией сурфактанта, а также из-за лимфостаза и нередкой гипергидратации.
Дренажная функция легких при искусственном дыхании нарушается почти всегда. Это связано с исключением кашлевого механизма очистки, с нарушением работы реснитчатого эпителия из-за недостаточного (реже избыточного) увлажнения, с сужением бронхиол из-за лимфостаза и отека. Определенную роль играет, вероятно, и снижение выработки сурфактанта при длительном искусственном дыхании, благодаря чему облегчается развитие ателектазов и уменьшается растягивающий эффект альвеол на мелкие дыхательные пути. Начавшаяся задержка мокроты закрывает отверстия в межальвеолярных перегородках (поры Кона) и другие пути коллатеральной вентиляции: дистальнее обструкции не может попасть воздух, благодаря чему силы поверхностного натяжения затрудняют отхождение мокроты от стенок альвеол и дыхательных путей. Нарушение дренажной функции легких ведет к росту аэродинамического и эластического сопротивления дыханию, снижается растяжимость легких, благодаря чему вентиляция нарушается еще больше.
Газообмен и распределение вентиляционно-перфузионных соотношений.
В большинстве случаев искусственное дыхание проводится в режиме гипервентиляции, вызывающем респираторный алкалоз и связанные с ним нарушения центральной регуляции дыхания, гемодинамики, электролитного состава и тканевого газообмена. Гипервентиляционный режим — вынужденная мера, связанная с нефизиологическим соотношением вентиляции и кровотока в легких во время искусственного вдоха и выдоха: при искусственном вдохе, в отличие от естественного, в легких увеличивается объем воздуха и уменьшается объем крови, при выдохе — наоборот. Другая причина неадекватности искусственного дыхания по сравнению со спонтанной вентиляцией того же объема — нефизиологическое внутрилегочное распределение воздуха, крови и вентиляционно-перфузионного соотношения. Нефизиологичность такого распределения связана с различными причинами:
1) своеобразная механика дыхания при искусственном дыхании вызывает отличноеот естественного дыхания регионарное распределение вентиляции;
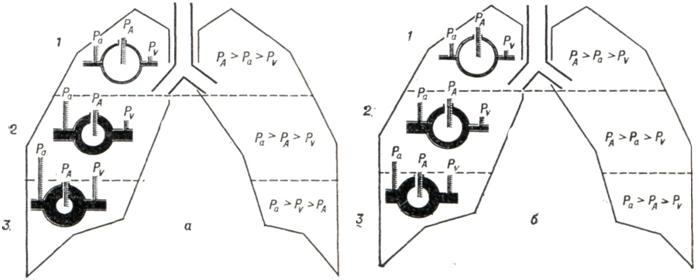
2) поскольку при искусственном дыхании воздух нагнетается в легкие поддавлением, легочный кровоток вовремя искусственного вдоха сокращается; благодаря этому меняется общее соотношение вентиляция—кровоток в легких, что выражается в изменении физиологического дыхательного «мертвого» пространства, альвеолярного шунта и других компонентов общего легочного объема; 3) изменение альвеолярного давления и связанное с этим изменение легочного капиллярного кровотока меняет регионарное распределение вентиляционно-перфузионных соотношений, так как это распределение зависитот соотношения альвеолярного, артериального и венозного легочного давления (рис. 2). Показано, что при искусственном дыхании по принципу вдувания невозможно найти режимвентиляции, обеспечивающий строго физиологическое распределение вентиляционно-перфузионных соотношений.
Альвеолокапиллярная диффузия при искусственном дыхании может нарушаться из-за утолщения альвеолокапиллярной мембраны в связи с лимфостазом и отеком, связанными с высоким внутригрудным давлением.
Влияние искусственного дыхания на тканевой газообмен зависит от адекватности вентиляции уровню метаболизма. Поскольку при большинстве методов и режимов искусственное дыхание менее физиологично, чем спонтанная вентиляция, подобрать его адекватный объем нелегко. Возникающие из-за этого гиперкапния, гипокапния и реже гипоксемия влияют на кривую диссоциации оксигемоглобина и нарушают тканевой газообмен.
Регуляция дыхания.
Искусственное дыхание нарушает регуляцию дыхания и нередко мешает восстановлению спонтанной вентиляции. Происходит это не только из-за нередкого уменьшения содержания углекислоты в крови. Чаще при искусственном дыхании наблюдается извращение эффекта рецепторов растяжения легких и грудной стенки, посылающих информацию в дыхательный центр.
Изменения в системе кровообращения.
На систему кровообращения влияет связанное с искусственным дыханием устранение или, наоборот, возникновение гипоксемии, респираторного ацидоза или алкалоза. Кроме того, искусственное дыхание оказывает на систему кровообращения прямое механическое воздействие, которое считалось настолько выраженным, что Уотерс (R. M. Waters, 1921) рекомендовал искусственное дыхание как механический двигатель крови для восстановления кровообращения. При искусственном дыхании по принципу вдувания нарушается присасывающее действие грудной клетки, обеспечивающее возврат значительной части венозной крови при естественном вдохе. В связи с этим венозный возврат затрудняется, и, хотя различные компенсаторные механизмы обеспечивают адекватное кровообращение на протяжении многих часов, дней и даже месяцев, при сопутствующей патологии системы кровообращения искусственное дыхание с неудачно подобранным режимом может вызвать опасные для жизни гемодинамические расстройства.
Поскольку давление в легочных капиллярах равно 10—12,мм ртутного столба, то искусственное дыхание с более высоким давлением вдоха неизбежно нарушает легочный кровоток. Вытеснение из легких крови в левое предсердие во время искусственного вдоха и противодействие выбросу правого желудочка вносят дисбаланс в работу правой и левой половин сердца. Менее выраженный дисбаланс имеется и при спонтанной вентиляции, однако соотношения гемодинамики правого и левого сердца во время естественного вдоха и выдоха противоположны наблюдаемым при искусственном дыхании.
Изменения в водном обмене.
При длительном искусственном дыхании могут возникать интерстициальные отеки, физиологический механизм которых многообразен. Во-первых, высокое внутрилегочное давление нарушает возврат лимфы через грудной проток в венозное русло, а лимфостаз способствует развитию отеков. Во-вторых, нарушение венозного возврата и высокое периферическое венозное давление также могут способствовать возникновению отеков. Втретьих, изменение наполнения камер сердца и крупных внутригрудных сосудов может через систему волюморецепторы — гипоталамус — гипофиз — антидиуретический гормон (АДГ) — альдостерон увеличить реабсорбцию воды в почках и привести к гипергидратации. Установлено, что чем выше среднее внутригрудное давление во время искусственного дыхания, тем большими бывают уровни АДГ плазмы и тем меньшим оказывается диурез. И, наконец, при длительном искусственном дыхании недостаточное питание на фоне высокого катаболизма белков может вызвать гипопротеинемию, низкое онкотическое давление крови и, следовательно, отеки.
Несмотря на перечисленные отрицательные физиологические эффекты, искусственное дыхание обеспечивает главное — газообменную функцию легких, то есть является средством реанимации и интенсивной терапии для больных с острой дыхательной недостаточностью.
Показания и противопоказания
Применение искуственного дыхания показано во всех случаях, когда объем спонтанной вентиляции недостаточен для обеспечения адекватного газообмена. Это требуется при многих срочных и плановых клинических, ситуациях: 1) расстройства центральной регуляции дыхания в связи с клинической, смертью, нарушением мозгового кровообращения, отеком, воспалением, травмой или опухолью мозга, медикаментозными и другими видами отравлений; 2) поражение нервных путей и нервно-мышечного синапса — травма шейного отдела головного мозга, полиомиелит и другие вирусные инфекции, полиневриты, миастения, ботулизм, столбняк, токсический эффект антибиотиков, отравление пахикарпином, фосфорорганическими соединениями и другими холинергическими ядами, применение миорелаксантов при анестезии и интенсивной терапии; 3) болезни и повреждения дыхательных мышц и грудной стенки — полимиозиты, миодистрофии, полиартрит с поражением реберно-позвоночных суставов, открытый пневмоторакс (в том числе операционный), множественные переломы ребер и грудины; 4) рестриктивные и обструктивные поражения легких — интерстициальный отек, пневмония и пневмонит, бронхоастматическое состояние, бронхиолит и другое, сопровождающиеся интенсивной работой дыхательных мышц, поглощающих большую часть кислорода и дающих избыток недоокисленных продуктов; высокое дыхательное «мертвое» пространство при некоторых болезнях легких.О необходимости искуственного дыхания судят по сочетанию клинических, симптомов и данных функциональных методов исследования. Наличие возбуждения или комы, цианоза, повышенной потливости, тахи- и брадисистолии, изменение величины зрачков, активное участие в дыхании вспомогательной мускулатуры на фоне диспноэ и гиповентиляции требуют применения искуственного дыхания. Если судить по данным газового анализа и других функциональных исследований, то применение искуственного дыхания показано, когда дыхание учащается вдвое по сравнению с нормой, жизненная емкость легких снижается на 40—50% и объем спонтанной вентиляции не позволяет получить в артериальной крови насыщение гемоглобина кислородом больше 70—80%, рО2 выше 60 мм ртутного столба, рСО2 ниже 50—60 мм ртутного столба, а рН выше 7,2. Но даже в тех клинических, ситуациях, когда эти показатели при спонтанной вентиляции несколько лучше, но достигаются избыточной работой дыхательных мышц, а также при опасности декомпенсации из-за сопутствующей патологии показан переход на искуственное дыхание.
В тех случаях, когда причиной гипоксемии является не гиповентиляция, а иные механизмы патологии легких (например, нарушение альвеоло-капиллярной диффузии, большой альвеолярный шунт венозной крови и другого), искуственное дыхание, почти не увеличивая поступления кислорода из легких в кровь, снижает его потребление дыхательными мышцами и, следовательно, повышает количество кислорода, поступающего в жизненно важные органы.
В большинстве случаев искуственное дыхание является лишь вспомогательным методом, не подменяющим интенсивной терапии, направленной на основной физиологический механизм патологии.
Применение искуственного дыхания необходимо, когда спонтанная вентиляция выключается с помощью миорелаксантов, введенных в лечебных целях: анестезия во время операции, интенсивная терапия судорожного и гипертермического синдрома и другое.
Абсолютных противопоказаний к искуственному дыханию нет, существуют лишь противопоказания к применению различных методов и режимов искуственного дыхания. Так, при затруднении венозного возврата крови противопоказаны режимы искуственного дыхания, еще более нарушающие его, при травме легкого могут быть противопоказаны методы искуственного дыхания по принципу вдувания с высоким давлением вдоха и тому подобное.
Чаще применяют методы искуственного дыхания, основанные на принципе вдувания. К ним относятся экспираторные методы (изо рта в рот, в нос, в интубационную трубку или воздуховод), аппаратные методы с ручным приводом (мешок Амбу, РПА, РДА, дыхательный мешок или мех наркозного аппарата и другие) и аппаратные методы с автоматическим приводом (автоматические респираторы РО-2, РО-5, РОА-2, ДП-8, АНД-2, ЛАДА, РД-1, РД-2, РД-4 и другие). Меньшее распространение имеют внешние методы искуственного дыхания с использованием боксовых и кирасных респираторов.
Методика и техника искуственного дыхания имеет общие для всех методов и специфические для каждого черты. К общим требованиям относятся: 1) обеспечение проходимости дыхательных путей специальным положением тела больного, введением воздуховода, интубационной трубки, наложением трахеостомы; 2) тщательный контроль адекватности искуственного дыхания, проводящийся на основании внешних признаков или специальных исследований; 3) обеспечение дренажа дыхательных путей при помощи увлажнения дыхательной смеси, аэрозольных ингаляций, туалета трахеи и бронхов и тому подобное; 4) профилактика возможных осложнений и вредных влияний искуственного дыхания на различные функции организма.
Во время искуственного дыхания считают необходимым проводить каждые 30 — 40 мин. вдувание в легкие утроенного дыхательного объема. Это нужно для профилактики ателектазов, поскольку при искуственном дыхании нарушается дренажная функция дыхательных путей, ненормальны вентиляционно-перфузионные соотношения, питание альвеолярной ткани и тому подобное. В некоторых респираторах (РО-5, РО-6) предусмотрено автоматическое раздувание легких повышенным объемом вдоха каждые 20—40 мин.
Необходимое условие длительного искуственного дыхания—увлажнение дыхательной смеси. При спонтанной вентиляции дыхательная смесь, проходя через нос и носоглотку, согревается, очищается и увлажняется. При искуственном дыхании газовая смесь попадает непосредственно в трахею: высушивая слизистую оболочку дыхательных путей, она лишает ее антибактериальных барьерных свойств, нарушает дренажную функцию бронхов и способствует возникновению обструктивных и воспалительных осложнений. Для нормального состояния слизистой оболочки дыхательных путей вдыхаемый газ должен быть полностью увлажнен. Полное насыщение дыхательной смеси водяными парами при t° 37° происходит при давлении 47 мм ртутного сталба, для чего требуется ок. 50 мг воды на 1 л воздуха. Относительная 100% влажность воздуха при комнатной температуре (20°) снижается до 36%, когда воздух попадает в трахею, где температура 37°. Это обосновывает необходимость применения увлажнителей при искуственном дыхании.
Наиболее эффективны ультразвуковые генераторы аэрозолей, увлажнители других типов менее производительны. При вентиляции 12 л/мин температура воды в испарителе падает на 13° ниже окружающей, следовательно, испаритель должен иметь подогрев. Опасность инфицирования при увлажнителях такого типа больше. Бендиксен (Н. Bendixen) с соавт. (1965) полагает, что при искуственном дыхании объемом 10 л/мии во вдыхаемую смесь необходимо добавлять 650 мл воды в сутки.
Избыточное увлажнение представляет не меньшую опасность, поскольку ухудшается растяжимость легких, лишняя вода всасывается в легких, нередко приводя к гипергидратации.
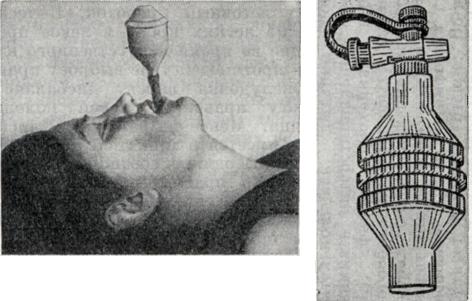
Важная мера поддержания нормального увлажнения слизистой оболочки дыхательных путей — использование «искусственного носа» (рис. 3), представляющего собой емкость с гофрированной фольгой, поддерживающей близкий к ламинарному поток воздуха и конденсирующей на себе влагу, благодаря чему потери ее снижаются. Это устройство можно подсоединить к интубационной или трахеостомической трубке. В некоторых современных респираторах предусмотрены датчики, контролирующие уровень влажности и включающие генератор аэрозолей при недостатке влаги.
 |
 |
 |
Рис. 3. | ||
Адаптация больного к респиратору (синхронизация с собственными дыхательными движениями) достигается несколькими методами. Суггестивный метод (команда «вдох — выдох») применим у находящихся в сознании больных и эффективен при умеренной гипервентиляции. Выраженная гипервентиляция (30—40% сверх должной величины) также позволяет синхронизировать дыхательные движения больного с респиратором. Наркотические и седативные средства, подавляющие собственные дыхательные попытки, применяют при неэффективности предшествующих методов.
Миорелаксанты короткого действия используют в начале искусственного дыхания; миорелаксанты длительного действия для адаптации к респиратору следует применять лишь при отсутствии эффекта от остальных методов или при необходимости подавления судорожного синдрома. Десинхронизация дыхательных движений больного и респиратора возникает чаще всего при нарушении герметичности дыхательного контура и при гиповентиляции.
Экспираторные методы
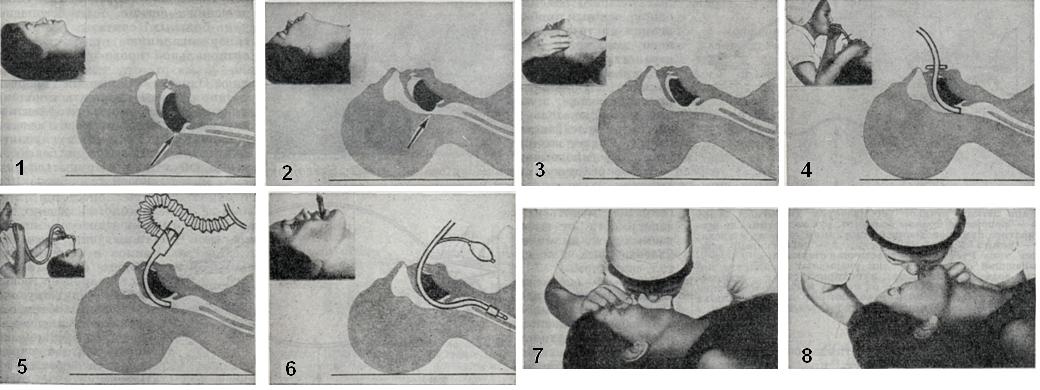
Экспираторные методы применяются только в срочных ситуациях — при внезапном прекращении дыхания и невозможности применить аппаратные методы. Чтобы обеспечить проходимость верхних дыхательных путей, голову лежащего на спине пострадавшего максимально разгибают в позвоночно-затылочном сочленении, выдвигая нижнюю челюсть вперед и вверх так, чтобы подбородок занимал самое возвышенное положение (рис. 4). Обеспечение проходимости дыхательных путей облегчается введением S-образного воздуховода или интубационной трубки. Оживляющий вдувает в рот или нос пострадавшего выдыхаемый им самим воздух после предшествующего глубокого вдоха,
При вдувании в рот ноздри пострадавшего должны быть зажаты пальцами или щекой оживляющего, хотя в ряде случаев эта мера является излишней, поскольку мягкое небо выполняет роль клапана и не пропускает вдуваемый воздух в полость носа. При вдувании в нос должен быть закрыт рот пострадавшего, который следует открывать при выдохе, если мягкое небо пе пропускает воздух через нос.
Главный критерий эффективности экспираторных методов искусственного дыхания — расширение грудной клетки при вдувании воздуха и спадение ее при пассивном выдохе. Частота вдуваний зависит от скорости пассивного выдыхания воздуха и для взрослого человека колеблется в пределах 10—20 в 1 минуту, а объем вдуваемого воздуха каждый раз — 0,5 —1,0 л. Поскольку при давлении свыше 20 см водного столба воздух может попадать в желудок, вызывая регургитацию желудочного содержимого и другие осложнения, необходимо, чтобы давление вдоха не превышало эту величину. При хорошей проходимости дыхательных путей давление вдоха 12—15 см водного столба достаточно, чтобы вдуть в легкие пострадавшего необходимый объем воздуха.
В тех случаях, когда искусственное дыхание сочетается с закрытым массажем сердца, делают одно вдувание через 4—5 сжатий грудной клетки. Если один оживляющий проводит искусственное дыхание и закрытый массаж сердца, то рекомендуется два вдувания подряд, а затем 10—12 сжатий грудной клетки.
Несмотря на то, что в выдыхаемом воздухе, который вдувают пострадавшему, содержится только 15 — 17% кислорода и 2—4% углекислоты, экспираторные методы высокоэффективны в поддержании необходимого газообмена на протяжении десятков минут и даже часов.
Однако эти методы не только утомительны для оживляющего, но благодаря гипервентиляции неизбежно ведут к возникновению у него респираторного алкалоза, снижению сосудистого тонуса и другим расстройствам. Поэтому экспираторные методы применяют в экстренных случаях.
Ручные респираторы
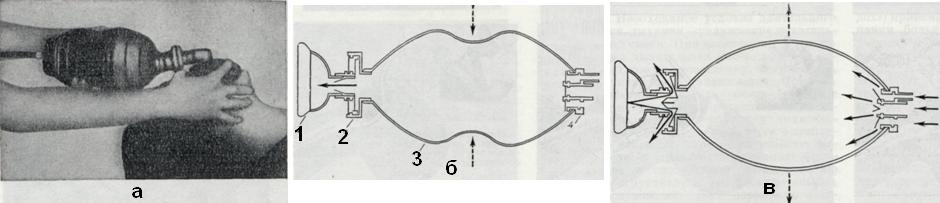
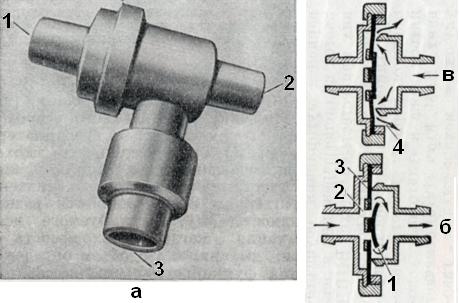
Ручные респираторы, так же как и экспираторные методы искусственного дыхания, применяются главным образом в срочных случаях. Частным случаем планового применения ручных респираторов является искусственное дыхание периодическим сжатием дыхательного мешка (рис. 5) или меха наркозного аппарата при проведении анестезии с миорелаксацией.
При искусственном дыхании ручными респираторами необходимо, так же как и при экспираторных методах, обеспечить проходимость верхних дыхательных путей их очисткой, специальным положением тела, введением воздуховода или интубационной трубки. Обязательным условием искусственного дыхания ручными респираторами любого типа (Амбу, РДА-1, РПА-2 и других) является наличие между дыхательными путями больного и респиратором нереверсивного клапана (типа Рубена, ВНИИМП и других), обеспечивающего разделение вдуваемого и пассивно выдыхаемого воздуха (рис. 6). Объем, частота, давление и контроль эффективности искусственного дыхания ручными респираторами такие же, как при экспираторных методах искусственного дыхания. Однако, в отличие от последних, искусственное дыхание ручными респираторами позволяет добавлять к вдыхаемому воздуху кислород либо даже проводить искусственное дыхание 100% кислородом.
Автоматические респираторы
Автоматические респираторы применяются как для кратковременного искусственного дыхания в условиях скорой помощи (ДП-7, ГС-8, РД-1 и другие), так и для длительного (от нескольких часов до нескольких лет) искусственного дыхания в стационаре (РО-2, РО-3, РО-5, ДП-8, АНД-2, ЛАДА и другие). Если искусственное дыхание рассчитано на несколько часов, оно проводится через интубационную трубку. Для миогосуточного и более длительного искусственного дыхания требуется, как правило, трахеостомия.
В клинической, практике применяют главным образом три режима искусственного дыхания, отличающихся друг от друга характером выдоха: с перемежающимся положительным давлением вдоха + 15, + 20 см водного столба при пассивном выдохе (ППД, IPPV английских авторов), при активном выдохе с отрицательным давлением —3, —5 см водного столба (ППОД, IPNPV) и при сохранении положительного давления +3, +8 см водного столба к концу выдоха (ППДвыд, PEEPV).
Помимо принципиальной характеристики выдоха, режим искусственного дыхания подбирают по минутному и дыхательному объему вентиляции, частоте дыхания, пиковой величине и кривой давления вдоха и выдоха, продолжительности и соотношению фаз вдоха, выдоха и паузы. Регулировать все перечисленные параметры независимо друг от друга не позволяет ни один из существующих респираторов; поэтому, подбирая один или два параметра искусственного дыхания, изменяют в нужном направлении остальные.
Минутный объем искусственного дыхания выбирают по одной из специальных номограмм, например номограмме Радфорда, номограмме Энгстрема — Герцога, составленным с учетом пола, возраста, веса, поверхности тела больного и иногда других показателей. Такой выбор, однако, является лишь ориентировочным и требует внесения поправок еще до начала искусственного дыхания, как это предусматривают и сами авторы номограмм. Полученную по номограмме величину увеличивают или уменьшают на 10 — 20% в зависимости от наличия хронической дыхательной недостаточности, морфологических изменений легких, отклонения температуры тела от нормальной, характера анестезии и операции, введения интубационной или трахеостомической трубки, растяжимых (гофрированных) или жестких соединительных шлангов и тому подобное.
Учитывая столь многочисленные поправки, объем искусственного дыхания, выбранный по номограмме, корригируют в соответствии с изменениями некоторых функций организма во время искусственного дыхания. Главными критериями для коррекции являются парциальное давление кислорода и двуокиси углерода (рО2 и рСО2) артериальной крови, центральное венозное давление и другие показатели кровообращения, а также общедоступные клинические, показатели (цвет и влажность кожных покровов и другое).
Учитывая нефизиологичность влияние искусственного дыхания по принципу вдувания на вентиляционно-перфузионные соотношения в легких, более безопасной для больных считают умеренную гипервентиляцию, при которой рСО2 артериальной крови (РаСО2) равно 30—35 мм ртутного столба, чем гиповентиляцию. Однако выраженная гипервентиляция может нарушить гемодинамику из-за механического эффекта навнутригрудной объем крови и из-за гипокапнии. При этом может углубляться уровень оощей анестезии без добавления анестетика, нарушаться тканевой газообмен. Перспективно увеличениедыхательного объема содновременным прибавлением инструментального «мертвого» пространства. Тогда большая альвеолярная вентиляция лучше расправляет легкие, а увеличенное дыхательное «мертвое» пространство предупреждает возникновение гипокапнии. Выбор режима искусственного дыхания зависит отего цели (искусственного дыханиепри анестезии, при патологии легких или мышечного аппарата дыхания, внезапное апноэ и тому подобного), от состояния больного (возраст, характер основной и сопутствующей патологии, объем оперативного вмешательства и другого), от возможностей лечебного учреждения и обстановки. В течение искусственного дыхания режим может многократно меняться в зависимости от вызываемых искусственным дыханием благотворных или патологических, эффектов.
Режим с перемежающимся давлением вдоха и выдоха.
Наиболее распространенным режимом является искусственное дыхание с положительным давлением вдоха при пассивном выдохе. Режим с отрицательным давлением выдоха применяют главным образом для снижения вредного влияния искусственного дыхания на гемодинамику. Однако при этом режиме распределение вентиляционно-перфузионного соотношения бывает более нарушенным в связи с углублением аномального эффекта внутрилегочного давления на вентиляцию и кровоток (при вдохе в легких много воздуха и мало крови, при выдохе — наоборот). Кроме того, режим искусственного дыхания с отрицательным давлением выдоха способствует более выраженному экспираторному закрытию дыхательных путей, в связи с чем растет шунтирование венозной крови через легкие. По этой причине применение такого режима искусственного дыхания, полезного при высоком сопротивлении дыхательных путей или интубационной трубки, не рекомендуется у больных, где ведущим механизмом повышенного сопротивления является экспираторное закрытие дыхательных путей (обструктивная эмфизема легких, астматический бронхит и другое). Режим искусственного дыхания с активным выдохом противопоказан также при отеке легких, ателектазах, множественных переломах ребер.
Режим искусственного дыхания с сохранением положительного давления к концу выдоха рекомендуется для снижения внутрилегочного объема крови, например при отеке легких, в том числе иитерстициальном, для уменьшения экспираторного закрытия дыхательных путей в послеоперационном периоде, при обструктивной эмфиземе легких и тому подобное.
Брадипноический режим
Брадипноический режим (частота вдуваний 4—6 в 1 минуту при увеличении дыхательного объема в 2—4 раза) применяется для снижения внутригрудного давления, а также для обеспечения относительно неподвижного операционного поля при оперативных вмешательствах на диафрагме, средостении, легких. В. А. Гологорский (1971) находит, что брадипноическое искусственное дыхание обеспечивает адекватный газообмен, хотя влияние его на другие функции организма требует дальнейшего уточнения.
Тахипноический режим
Тахипноический режим выполняется в двух вариантах: при увеличении частоты вдуваний до 30—40 в 1 минуту с преднамеренной гипервентиляцией [Грей (Т. С. Gray), 1960] или при частоте до 80 — 110 в 1 минуту с нормовентиляцией [Йонсон (A. Jonson) с соавторами, 1971, 1973]. При тахипноическом искусственном дыхании дыхательный объем снижен, давление вдоха равно от+5до +10 см водного столба, выдоха от 0 до —5 см водного столба. Среднее внутрилегочное и внутригрудное давление низкое, нарушения гемодинамики минимальны, газообмен, как правило, адекватен, если учтена величина дыхательного «мертвого» пространства. Чтобы достичь частоты вдуваний 100—110 в 1 минуту, требуются респираторы со специальным электронным клапаном-прерывателем.
Асинхронный режим
Асинхронный режим применяется редко, главным образом для снижения среднего внутригрудного давления; сущность — поочередная вентиляция правого и левого легкого, когда вдувание газовой смеси в одно легкое сочетается с выдохом в другом легком. Для проведения асинхронного искусственного дыхания используют по одному респиратору на каждое легкое либо специальный респиратор АР-1.
Ауторегулируемый режим.
Истинно автоматическим является искусственное дыхание, параметры которого регулируются по принципу обратной связи в соответствии с функциональными изменениями организма. Наиболее распространен метод ауторегулируемого искусственного дыхания, режим которого управляется величиной рСО2 альвеолярного газа (Т. М. Дарбинян, с соавторами, 1970). Существует метод ауторегулируемого искусственного дыхания, управляемого биотоками диафрагмального нерва и диафрагмы.
В условиях анестезии и операции.
Для проведения анестезии с искусственной миоплегией используют дыхательный мешок или мех наркозного аппарата (искусственное дыхание с ручным приводом), автоматические респираторы с наркозным блоком (РО-5, РО-6, АНД-2 и другие) или наркозные аппараты с респираторами-приставками (РД-2, «Ассистор» Дрегера и другие). При ручном искусственном дыхании анестезиолог должен приспособиться к «ощущению» мешка, которое складывается из надуваемого объема, растяжимости легких, сопротивления дыхательных путей и тому подобного.
Чтобы сохранить необходимый газовый состав инсуффлируемых анестетиков при использовании респираторов, применяют лишь аппараты с мехом (РО-3, РД-2 и другие) или с большим объемом инжекции (РД-1). При внутригрудных операциях, в частности при операциях на легких, приходится иногда проводить однолегочное искусственное дыхание, для чего используют бронхоблокаторы или раздельную интубацию бронхов. В ряде случаев используют брадипноическое искусственное дыхание, диффузионное дыхание.
Инжекционный метод
Инжекционный метод, впервые предложенный в 1967 г. Сандерсом (R. D. Sanders) и разработанный в СССР Г. И. Лукомским с соавторами (1971), применяется при негерметичности дыхательного контура; например, при некоторых эндобронхиальных манипуляциях (биопсия, удаление инородных тел, лаваж дыхательных путей и тому подобное). При инжекционном методе искусственного дыхания кислород под давлением в несколько атмосфер подается через инжекционную иглу в тубус бронхоскопа, который выполняет роль диффузора. Во время вдоха атмосферный воздух подсасывается через бронхоскоп в легкое, выдох осуществляется пассивно при прекращении вдувания кислорода через иглу. Регулируя давление в игле и продолжительность инжекции, можно получить необходимую продолжительность, давление, объем и объемную скорость вдоха. Существуют специальные автоматические респираторы для инжекционного метода искусственного дыхания.
Диффузионное дыхание
Диффузионное дыхание, или апнойная оксигенация, — инсуффляция кислорода в легкое при отсутствии дыхательных движений. Кислород вводят различными методами— через ротоносовую маску, интубационную трубку, бронхоскоп, катетеры; альвеол он достигает путем газовой диффузии, частично вымывая углекислоту. Метод используют сравнительно редко, главным образом потому, что искусственное дыхание с перемежающимся введением и удалением адекватных объемов газа значительно эффективнее. Тем не менее, искусственное дыхание по методу диффузионного дыхания способно предупредить развитие гипоксемии в течение 10—20 минут, хотя гиперкапния при этом может возникать.
Перед началом диффузионного дыхания необходимо провести денитрогенацию организма ингаляцией 100% кислорода. Адекватность искусственного дыхания при методе апнойной оксигенации в течение указанного срока была доказана А. П. Зильбером (1971) с помощью радиоизотопного исследования. Применение метода показано при операциях на легком для создания неподвижного операционного поля, при травме легкого, когда введение воздуха под давлением противопоказано. Апнойная оксигенация не только обеспечивает достаточную вентиляцию легкого, но и уменьшает шунт венозной крови, неизбежно возникающий в невентилируемом легком (рис. 7). В связи с этим при проведении однолегочного искусственного дыхания на здоровом легком методом ППД или ППОД в неподвижное больное легкое необходимо вводить кислород или азот методом апнойной оксигенации или апнойной нитрогенации — оба приема уменьшают шунт венозной крови.
Глоссофарингеальное дыхание
Глоссофарингеальное дыхание — сравнительно редко применяющийся метод искусственного дыхания, предложенный в 1951 г. Дайлом (С. W. Dail), используется у больных с параличом дыхательной мускулатуры в результате полиомиелита и других нейровирусных инфекций при сохранении у них сознания. Суть метода состоит в том, что после специальной тренировки больной, используя спинку и корень языка как поршень, а носоглотку как камеру для поршня, дробно нагнетает в легкие воздух — 6—8 «глотаний» по 50—80 мл за цикл. Выдох осуществляется пассивно. Аффелдт (J. E. Affeldt) с соавторами (1955) показал, что глоссофарингеальное дыхание вполне обеспечивает адекватный объем вентиляции легких. Особенность этой разновидности искусственного дыхания состоит в том, что больной сам осуществляет искусственное дыхание, но способен делать это лишь в состоянии бодрствования и нуждается в подключении респиратора на время сна.
Вспомогательная искусственная вентиляция легких
Вспомогательная искусственная вентиляция легких (ВИВЛ) — искусственное увеличение вентиляции при неадекватности спонтанной вентиляции. Различают адаптационную вспомогательную искусственную вентиляцию легких, когда недостаточную спонтанную и искусственную вентиляцию синхронизируют различными методами, и «откликающуюся», или триггерную, когда углубление вдоха достигается автоматически при попытке естественного вдоха.
При адаптационной вспомогательной искусственной вентиляции легких используют любые респираторы, а для синхронизации вспомогательной искусственной вентиляции легких со спонтанной вентиляцией применяют суггестивные методы, введение нейролептиков и депрессантов дыхания. В последнем случае вспомогательная искусственная вентиляция легких фактически превращается в искусственное дыхание. Для триггерной вспомогательной искусственной вентиляции легких используют респираторы, снабженные откликающимся устройством (РО-3, РО-5, РО-6 и другими), срабатывающим при достижении определенного разрежения, возникающего в респираторе во время самостоятельного вдоха, и включающим респиратор на режим искусственного вдоха. Фактически триггерная вспомогательная искусственная вентиляция легких является разновидностью ауторегулируемого искусственного дыхания, когда необходимость в искусственном дыхании и его объем определяются функциональными изменениями в организме больного. В данном варианте ауторегуляция осуществляется по степени разрежения в легких при естественном вдохе. Вспомогательнаяй искусственная вентиляция легких показана у «дыхательных хроников», при гиповентиляции в послеоперационном периоде и может применяться даже в амбулаторных условиях. В. М. Юревич (1973) отмечает улучшение механики дыхания, газообмена, снижение энергетических затрат и общий благотворный эффект вспомогательной искусственной вентиляции легких у больных с хронической дыхательной недостаточностью.
При реанимации новорожденных
При реанимации новорожденных искусственное дыхание осуществляется респираторами с ручным приводом и автоматическими. Особенностью искусственного дыхания в таких условиях является высокая частота дыхания при малых объемах вдоха (15 — 20 мл). Умеренное отрицательное давление в конце выдоха необходимо, чтобы преодолеть сопротивление узкой интубационной трубки. Искусственное дыхание у новорожденных может проводиться и модифицированной системой Эйра, когда легкие раздувают закрытием бокового отвода коннектора.
В условиях гипербарической оксигенации.
В связи с возможностью пожара в этих условиях можно использовать респираторы лишь с пневматическим приводом (РД-1, ЛАДА и другие). Одновременно с возрастанием давления в барокамере необходимо повышать давление газа, подающегося к респиратору, что ведет к значительным отклонениям минутной вентиляции, требующим своевременной коррекции. Показатели волюметров в условиях гипербарическои оксигенации также отличаются от условий нормального давления.
В военно-полевых условиях.
Острая дыхательная недостаточность в военно-полевых условиях возникает при тяжелых ранениях и закрытых травмах головного мозга, челюстно-лицевой области и груди, а также при тяжелых отравлениях.
Показания к искусственному дыханию, как и в мирное время, определяются степенью нарушения дыхания, а возможности и способы проведения зависят от количества нуждающихся и условий обстановки.
На поле боя и передовых этапах эвакуации с целью восстановления и поддержания дыхания у тяжело пораженных используются наиболее простые методы, которыми должны владеть санинструкторы и санитары, а также все военнослужащие для оказания взаимопомощи. К таким методам относится дыхание изо рта в рот, изо рта в нос и искусственное дыхание с помощью S-образной трубки, которая имеется в санитарных сумках. В периоды возникновения массовых санитарных потерь и в условиях неблагоприятной боевой обстановки возможность применения и этих методов может оказаться весьма ограниченной.
Более благоприятные условия для искусственного дыхания на БМП, где фельдшер может провести искусственное дыхание через S-образную трубку или через маску портативного ручного дыхательного аппарата. Предварительно с целью восстановления проходимости верхних дыхательных путей, кроме придания раненому соответствующего положения, фельдшер удаляет слизь и кровь из полости рта и носоглотки с помощью портативного отсоса, а при необходимости вводит воздуховод.
На ПМП возможность искусственного дыхания значительно шире, однако и здесь ее проводят только тем пораженным, которым угрожает асфиксия непосредственно или во время предстоящей эвакуации. Помимо ручных дыхательных аппаратов, здесь применяют портативные дыхательные автоматы. В отдельных случаях подключению аппарата предшествует интубация трахеи или трахеостомия.
В МСБ и госпиталях предусматривается возможность осуществления не только кратковременного, но и относительно продолжительного искусственного дыхания с помощью различных аппаратов. Она может проводиться одновременно нескольким пораженным и в большинстве случаев при участии анестезиологов-реаниматологов в условиях противошоковых палат или операционных. Искусственное дыхание — один из важнейших элементов анестезиологического обеспечения многих операций. В этой области для него нет существенных ограничений по сравнению с условиями мирного времени.
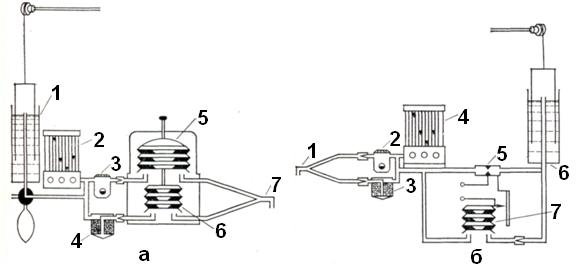
Режим работы респиратора контролируют по вдуваемому объему, абсолютной величине и динамике давления вдоха и выдоха. Волюметры (расходомеры потока) следует устанавливать на канале выдоха, это уменьшает вероятность ошибочных показаний в связи с утечкой. Особые трудности представляет спирография в условиях искусственного дыхания, особенно при наличии наркозного аппарата в общем дыхательном контуре. Вариант включения спирографа с различными респираторами при проведении искусственного дыхания представлен на рисунке 8. При спирометрии в этих условиях возможна внутренняя утечка газа. Схема б в этом отношении более надежна, однако возможность проведения спирометрии при искусственном дыхании и создания соответствующих моделей аппаратов изучается. Пневмотахография, редко применяющаяся в повседневной клинической, практике, позволяет контролировать при искусственном дыхании не только объемы, но и объемную скорость и динамику давлений вдоха и выдоха, а также другие показатели механики дыхания. Датчик пневмотахографа надо устанавливать перед интубационной или трахеостомической трубкой и при выборе объема вентиляции учитывать дополнительное инструментальное «мертвое» пространство.
Почти во всех респираторах имеются манометры, позволяющие контролировать пиковое давление вдоха и выдоха. Существуют устройства («Сигнал-1» и другие), сигнализирующие об отклонении давления от заданных параметров и о разгерметизации контура.
Окончательно об адекватности искусственного дыхания судят по состоянию жизненно важных функций организма, оценивая газы крови, центральное венозное давление и другие показатели гемодинамики, водно-электролитное и кислотно-щелочное состояние, цвет и влажность кожных покровов, участие в дыхании вспомогательной мускулатуры и тому подобное. Переход на спонтанную вентиляцию. Способность больного обеспечить адекватную вентиляцию, по данным клинического, и функционального исследования, позволяет прекратить искусственное дыхание. Иногда после длительного искусственного дыхания это приходится делать в несколько этапов, постепенно приучая больного к спонтанной вентиляции или переводя его вначале на вспомогательную вентиляцию легких. В процессе перехода на спонтанную вентиляцию, который может продолжаться до нескольких суток, необходимо тщательно контролировать ее объем, газы крови, следить за внешним видом больного, проводить дыхательную гимнастику и осуществлять санацию дыхательных путей.
Уход за больными, особенно находящимися на длительном искусственном дыхании, включает, в первую очередь, туалет дыхательных путей с использованием аппарата искусственного кашля, аспирации мокроты, аэрозольных ингаляций муколитических и антибактериальных препаратов, применение постурального дренажа. Важную роль в улучшении дренажа дыхательных путей играет поколачивание по грудной клетке и вибрационный массаж (сотрясение грудной стенки во время выдоха).
Большое значение имеет полноценное зондовое или парентеральное питание, контроль за функцией кишечника, за диурезом, профилактика инфекции мочевых путей и пролежней.
Специальный психологический режим для больных, находящихся в сознании, является важной составной частью ухода при длительном искусственном дыхании. Требуется систематический контроль за гемодинамикой, биохимические исследование крови, мочи и так далее. Результаты исследований, а также режим работы респиратора и проводящиеся больному дополнительные мероприятия регистрируются в специальных картах.
Чаще всего осложнения начинаются с системы дыхания. Помимо респираторного ацидоза и алкалоза, возникающих из-за неправильно выбранного режима, длительное искусственное дыхание нередко ведет к развитию ателектазов в связи с нарушением дренажной функции дыхательных путей, аномальным соотношением вентиляция⁄кровоток и снижением продукции сурфактанта. Микроателектазы могут служить основой для развития пневмонии. Профилактика этих осложнений — тщательный туалет дыхательных путей, периодические раздувания легких. Длительное искусственное дыхание 100% кислородом может вести к возникновению пневмонита, в связи с чем концентрация кислорода не должна превышать 40—50%.
К осложнениям искусственного дыхания относится продленное апноэ при переходе на спонтанную вентиляцию. Обычно оно является результатом аномального раздражения рецепторов легких, подавляющего нормальные рефлексы Геринга — Брейера и другие физиологические механизмы переключения вдоха и выдоха. Электромиографический контроль восстановления нервно-мышечной проводимости позволяет дифференцировать продленное апноэ периферической этиологии (действие миорелаксантов, болезни мышц и нервно-мышечного синапса) от апноэ в связи с нарушением центральной регуляции дыхания из-за респираторного алкалоза, повреждения дыхательного центра и тому подобнго.
Разрывы альвеол с возникновением напряженного пневмоторакса при искусственном дыхании чаще возникают при абсцедирующей пневмонии, особенно у детей. Иногда это осложнение бывает связано с неисправностью респиратора, нередко с десинхронизацией собственного дыхания больного и режима респиратора. Пневмоторакс требует немедленного дренирования плевральной полости.
К осложнениям в системе кровообращения относятся связанное с искусственным дыханием нарушение венозного возврата и уменьшение сердечного выброса. В таких случаях рекомендуется сменить режим искусственного дыхания, в частности использовать ППОД.
Нередко нарушение гемодинамики при искусственном дыхании связано с гипоксией, респираторным алкалозом или ацидозом, особенно при резких колебаниях рО2 и рСО2 в начале и в конце искусственного дыхания.
Нарушение водного обмена (гипергидратация, отеки) связано со многими причинами. Иногда в начале искусственного дыхания наблюдается парез кишечника и снижение кишечной перистальтики. Изредка возникают кровотечения из желудочно-кишечного тракта, причина и патогенез этих осложнений остаются не вполне ясными.
Сравнительно редко у больных, находящихся на длительном искусственном дыхании, развивается почечнокаменная болезнь как результат почечной компенсации респираторного алкалоза путем снижения реабсорбции бикарбонатов. Образованию камней способствует инфекция мочевых путей на фоне щелочной реакции мочи.
К осложнениям искусственного дыхания можно отнести и патологические состояния, связанные с длительным пребыванием в дыхательных путях интубационной или трахеостомической трубки, — стенотические и фибринозно-некротические ларинготрахео-бронхиты, пролежни, кровотечения из дыхательных путей.
Различают аппараты для наружного искусственного дыхания и аппараты, действующие по принципу вдувания. Последние более эффективны, позволяют легко управлять режимом вентиляции и более просты конструктивно.
Источником энергии для работы аппарата искусственного дыхания может быть сжатый газ, электричество или мускульная сила. Аппарат с пневматическим приводом (рис. 9 и 10) имеет небольшие размеры, так как в его состав баллоны с газом обычно не входят. Такой аппарат более удобен во время проведения ингаляционного наркоза, так как менее взрывоопасен. Аппараты искусственного дыхания с электроприводом (рис. 11 и 12) больше по размеру, но значительно удобнее для длительной вентиляции. Из аппаратов с ручным приводом наиболее распространены модели с эластичным самонаполняющимся мешком (рис. 13).
 |
 |
 |
Рис. 9. | ||
 |
 |
 |
Рис. 10. | ||
 |
 |
 |
Рис. 11. | ||
 |
 |
 |
Рис. 12. | ||
 |
 |
 |
Рис. 13. | ||
Аппараты искусственного дыхания классифицируют и по назначению — для реанимации, для наркоза, для применения у детей (рис. 14) и так далее.
 |
 |
 |
Рис. 14. | ||
В СССР выпускается более 15 различных моделей аппаратов для искусственного дыхания. Впервые в мире, в частности, осуществляется выпуск аппаратов, автоматически поддерживающих минутную вентиляцию такой величины, которая обеспечивает заданное содержание углекислоты в альвеолярном газе (рис. 15).
 |
 |
 |
Рис. 15. | ||
Основным узлом аппарата искусственного дыхания является генератор вдоха, подающий во время вдоха газ в легкие пациента. В пневматическом аппарате с этой целью обычно используется инжектор, питаемый сжатым кислородом под давлением 4 кгс/см2 и подсасывающий атмосферный воздух или другой газ. В аппаратах с электроприводом генератором вдоха служит центробежная воздуходувка или насос, работающий с заданной частотой дыхания. Если необходимо применять полузакрытый дыхательный контур, то в состав аппарата включают разделительную емкость, эластичный мешок, который входит в дыхательный контур.
Радикальным методом снижения вредного воздействия искусственного дыхания на гемодинамику является применение активного выдоха, что обеспечивается генератором выдоха, аналогичным по устройству генератору вдоха. Необходимую коммутацию газовых потоков осуществляет распределительный механизм, переключающийся из положения вдоха в положение выдоха и обратно после достижения заданных органами управления значений объема газа, промежутка времени или давления. Другие органы управления определяют производительность генератора вдоха, разрежение, создаваемое генератором выдоха, и прочие параметры.
Как правило, в состав аппарата искусственного дыхания входят фильтр, увлажнитель вдыхаемого газа, измерительные приборы, а иногда и сигнализаторы опасных ситуаций. Последние указывают на выход из заданных пределов давления конца вдоха, минутной вентиляции, давления питающего газа или других параметров и, таким образом являются одним из средств обеспечения надежной работы аппарата искусственного дыхания, что имеет для данного вида медицинской техники первостепенное значение.
Перед каждым подключением к пациенту обязательно проверяется работоспособность и герметичность аппарата. Для оценки последней следует перекрыть выходное отверстие аппарата и убедиться в быстром нарастании давления не менее чем до 30 см водного столба при установке минутной вентиляции до 5 л⁄мин. Необходимо соблюдать периодичность и объем технического обслуживания, приведенные в инструкции по эксплуатации, а также требования техники безопасности.
Перед подключением аппарата искусственного дыхания к пациенту дыхательный контур аппарата дезинфицируется. Металлические съемные части автоклавируют, резиновые и пластмассовые детали тщательно промывают, а затем выдерживают в дезинфицирующих растворах или протирают. Кипячение таких деталей ускоряет естественные процессы их старения. Дезинфекция внутренних линий дыхательного контура может осуществляться парами формальдегида, высокоплотным аэрозолем дезинфицирующих средств. После дезинфекции аппарат должен быть продут чистым воздухом для удаления следов дезинфицирующих препаратов.
Аппараты типа РО предназначены для длительного искусственного дыхания. Благодаря полному разобщению дыхательного контура от линии привода они могут обеспечить во время наркоза работу по полузакрытому дыхательному контуру; наиболее удобны в этом случае аппараты РО-5, РО-6Н, в состав которых входит и малогабаритный аппарат ингаляционного наркоза. Все модели данного типа имеют широкие возможности, укомплектованы увлажнителем, измерительными приборами и набором принадлежностей. Модели РО-5 и РО-6 позволяют проводить как управляемую, так и вспомогательную вентиляцию.
Аппараты РД-1 и РД-4 имеют привод от сжатого кислорода под давлением 4 кгс/см2 и выполнены на струйных элементах пневмоавтоматики. РД-1 предназначен для реанимации и имеет широкие возможности, обеспечивая, в частности, вспомогательную вентиляцию. Модель РД-4 является приставкой к универсальному аппарату ингаляционного наркоза Полинаркон-2 и имеет разборный дыхательный контур, что облегчает его дезинфекцию.
Аппарат Пневмат-2 используют для кратковременной реанимации. Наличие в нем баллона с кислородом делает эту модель полностью автономной.
Аппарат Вита-1 предназначен для новорожденных и детей в возрасте до 3 лет, поскольку он обеспечивает возможность дозировать очень малые дыхательные объемы и относительно высокие частоты дыхания. Для измерения фактических значений вентиляции аппарат укомплектован спирометром.
Краткая характеристика наиболее распространенных отечественных аппаратов для искусственного дыхания приведена в табл. 1.
 |
 |
 |
При оказании первой медпомощи в военно-полевых условиях применяют дыхательную трубку ТД-1.О2, а на этапах медицинской эвакуации — портативные ручные аппараты ДП-10.О2, АДР-2 и автоматы ДП-9.02, аппараты искусственного дыхания на пневмоэлементах Пневмат-1 (с фиксированными параметрами дыхания), на пневмоэлементах (УСЭППА) ЛАДА, аппараты искусственного дыхания Фаза-1, Фаза-2. Они удобны и надежны в работе. Кроме дыхательной трубки, все аппараты могут использоваться в зараженной атмосфере благодаря наличию приспособления для подсоса воздуха через коробку противогаза. Укладки металлические, пылебрызгозащищающие (кроме ТД-1.02). Основные характеристики ручных аппаратов приведены в табл. 2.
 |
 |
 |
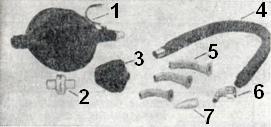
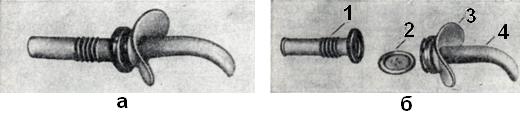
Дыхательная трубка ТД-1.02 состоит из разъемных мундштука с гофрировкой, нереверсивного клапана, нагубника, воздуховода (рис. 16). Аппараты ДП-10.О2, АДР-2 состоят из дыхательного латексного мешка в резиновой камере, двух нереверсивных клапанов и клапанного устройства для подачи кислорода. В комплекты входят аппараты, гофрированная трубка, маски, патрубки для кислорода, роторасширитель, языкодержатель и другое (рис. 17).
 |
 |
 |
Рис. 16. | ||
Автоматические аппараты для искусственного дыхания обеспечивают подачу кислородовоздушной смеси (35— 40%), чистого кислорода или воздуха под давлением (от компрессоров). В зависимости от приводов они подразделяются на пневматические (ДП-9.02, Пневмат-1, ЛАДА) и электрические (Фаза-1, Фаза-2).
Расход газа на привод пневматических аппаратов до 4 л⁄мин. Регулировка параметров плавная (в Пневмат-1 все параметры фиксированы). Респираторы могут подключаться к аппаратам ингаляционного наркоза. Основные характеристики аппаратов искусственног дыхания приведены в табл. 3.
 |
 |
 |
Аппарат для искусственного дыхания ДП-9.02 состоит из самого изделия в сборе с укладкой, кислородных баллонов, воздуховодов, масок, присоединительных элементов, резинового мешка, оголовья, роторасширителя, языкодержателя, заплечных ремней, комплекта запасных инструментов, принадлежностей (ЗИП). Аппарат для искусственного дыхания Пневмат-1 (рис. 18) предназначен для вентиляции легких в операционных, в противошоковых палатках. Он входит в комплект аппарата для ингаляционного наркоза Наркон-2. Состоит из редуктора, пневматического управляющего устройства, инжектора, фильтра, предохранительного клапана. В комплект входят аппарат, маски, дыхательный шланг, нереверсивный клапан, оголовье, переходники и другое. Аппарат для искусственного дыхания ЛАДА (рис. 19) предназначен для автоматического или ручного вспомогательного искусственного дыхания при сохраненном дыхании пациента, а также для постоянной или пульсирующей регламентированной ингаляции дыхательного газа. Представляет собой пневматическую систему с элементами пневмоавтоматики на пневмоплате, выполняющими аналоговые и дискретные логические операции. Аппараты Фаза-1 и Фа-за-2 обеспечивают длительную автоматическую вентиляцию легких воздухом под давлением или кислородо-воздушной смесью (от источника кислорода). Они высокоэффективны для пациентов с частично или полностью нарушенным самостоятельным дыханием.
 |
 |
 |
Рис. 18. | ||
 |
 |
 |
Рис. 19. | ||
Аппарат Фаза-2 рассчитан на двух пациентов; регулировка всех параметров автономная. Состоит из энергетического блока (с электромотором и воздуходувкой), электронного (включающего блоки и органы управления) блока, питания, а также электромагнитных клапанов и распределительного блока, клапанов подсоса, гофрированных трубок, масок, ЗИП. Укладки аппаратов используются в качестве основы подставки.
|
Богоявленский И.Ф., Гальперин Ю.Ш., Зильбер А.П., Уваров Б.С. |

|
⇐ Перейти на главную страницу сайта |
⇑ Вернуться в начало страницы ⇑ |
Библиотека Ordo Deus ⇒ |
⇐ Температура тела |
⇓ Каталог систематический ⇓ |
Искусственное кровообращение ⇒ |
|
Все статьи в полном изложении, Вы можете найти в большой медицинской энциклопедии — Главный редактор: академик АН СССР (РАН) и АМН СССР (РАМН) Б.В. Петровский. — Москва издательство «Советская энциклопедия» 1989г. |
|
Внимание! Вы находитесь в библиотеке «Ordo Deus». Все книги в электронном варианте, содержащиеся в библиотеке «Ordo Deus», принадлежат их законным владельцам (авторам, переводчикам, издательствам). Все книги и статьи взяты из открытых источников и размещаются здесь только для чтения. |
|
Библиотека «Ordo Deus» не преследует никакой коммерческой выгоды. |
|
Все авторские права сохраняются за правообладателями. Если Вы являетесь автором данного документа и хотите дополнить его или изменить, уточнить реквизиты автора, опубликовать другие документы или возможно вы не желаете, чтобы какой-то из ваших материалов находился в библиотеке, пожалуйста, свяжитесь с нами по e-mail: |
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы желаете прожить ещё одну жизнь? Начать всё заново? Исправить ошибки этой жизни? Осуществить несбывшиеся мечты? Перейдите по ссылке: «главная страница».
|
© Ordo Deus, 2010. При копировании ссылка на сайт http://www.ordodeus.ru обязательна. |