Аутоаллергические болезни |
||
 |
 |
Оглавление
|
Аутоаллергические болезниАутоаллергические болезни (греческое autos сам + аллергия) синонимы: аутоиммунные, аутоагрессивные болезни) — группа заболеваний, основным механизмом развития которых является реакция аутоантител и сенсибилизированных лимфоцитов с собственными тканями. Практически все клетки и ткани человека при определенных условиях могут быть объектом повреждающего действия лимфоцитов и аутоантител; поэтому клинические симптомы аутоаллергических болезней чрезвычайно разнообразны и могут проявляться как органными, так и системными поражениями. Возникновение учения об аутоаллергии как причине болезней связано с именем И. И. Мечникова. В 1900—1901 гг. И. И. Мечников и его ученики экспериментально доказали возможность продукции антител к белкам собственных клеток организма. В 1904 г. Донат и Ландштейнер (J. Donath, К. Landsteiner) обнаружили в сыворотке крови больных пароксизмальной холодовой гемоглобинурией антитела, специфически направленные против собственных эритроцитов. В 1908 г. Видаль, Абрами, Брюле (F. Widal, P. Аbrami, M. Brule) выявили аутогемолизины у больных приобретенной гемолитической анемией. С. С. Головин в 1904 г. высказал предположение об аутоиммунном патогенезе симпатической офтальмии. Особенно широкое распространение учение об аутоаллергии получило начиная с 40—50-х годов 20 в. При многих заболеваниях установлены аутоаллергические механизмы патогенеза. Следует, однако, строго разграничивать аутоаллергические болезни, где эти механизмы считаются ведущими, и аутоаллергические синдромы, осложняющие болезни другого генеза. Типичными примерами последних являются постинфарктный синдром, симптоматическая аутоиммунная анемия при лимфолейкозе, острая дистрофия печени при инфекционном гепатите, аутоаллергические синдромы при ожогах и лучевой болезни. Этиология. Ткани и клетки организма приобретают аутоаллергенные (аутоантигенные) свойства в результате повреждающего воздействия различных факторов окружающей среды. Эти повреждения приводят к высвобождению и попаданию в общий кровоток физиологически изолированных компонентов клеток и тканей или к изменению антигенных свойств белковых структур (смотри Аутоаллергия, Аутоантигены). Повреждающими экзогенными факторами могут быть травма, инсоляция, охлаждение, инфекция бактериальная и особенно вирусная, поскольку именно вирусы обладают способностью проникать в клетки и резко изменять структуру внутриклеточного белка. Некоторые лекарственные вещества, обладая тропизмом к определенным клеткам крови, становятся гаптенами, входящими в состав аутоантигенов. За последние годы получила подтверждение теория общих антигенных детерминант определенных штаммов микроорганизмов и тканей человека. Наличие таких детерминант приводит к сенсибилизации не только по отношению к микробам, но и по отношению к собственным тканям с последующим их повреждением. Выделены штаммы стрептококка группы А, имеющие общие антигены с тканью сердца человека, а также нефритогенные штаммы стрептококка, колитогенные штаммы кишечной палочки. При многих аутоаллергических болезнях этиологические факторы остаются до наст, времени неизвестными. Аутоаллергические болезни чаще развиваются у женщин. Патогенез. Можно выделить три пути развития аутоаллергических болезней. Первый путь — образование в организме аутоаллергенов (освобождение изолированных антигенов — коллоид фолликулов щитовидной железы, миелин, антигены хрусталика, яичек; денатурация тканей при ожоге, лучевой болезни и др.; образование комплексных и промежуточных антигенов). В ответ на появление аутоаллергенов включаются иммунологические механизмы, направленные на инактивацию и удаление этих аутоаллергенов. Эти механизмы, будучи в своей основе защитными, в ряде случаев вызывают повреждение клеток и тканей. Такой механизм предполагается при тиреоидите Хасимото, орхите, энцефаломиелите. Второй путь — дефекты в контроле за иммунологическими механизмами защиты организма — объясняет теория «запретного клона» по Бернету. |
В норме по отношению к антигенам собственных тканей существует иммунологическая толерантность (смотри Толерантность иммунологическая) и развитие клонов лимфоидных клеток, котторые могли бы участвовать в иммунологических реакциях с собственными тканями, либо заторможено, либо эти клоны элиминированы. При патологии в силу пока неизвестных причин возможно развитие такого клона, либо такой клон появляется в результате соматической мутации лимфоцита. Клетки такого клона начинают повреждать ткани организма по механизму «трансплантат против хозяина» (смотри Несовместимость иммунологическая). В реализации такого пути развития аутоаллергические болезни придают большое значение генетическому фактору, считая, что благодаря генетическим нарушениям функционируют так называемые запретные клоны иммунокомпетентных клеток, продуцирующих аутоантитела. В качестве фактов, подтверждающих роль генетического фактора, приводятся случаи семейного ревматизма, обнаружение ревматоидного фактора у родственников больных ревматоидным артритом, антител к тиреоглобулину у родственников больных аутоиммунным тиреоидитом, единичные наблюдения системной красной волчанки и других аутоаллергических болезней у однояйцовых близнецов. Однако этих фактов ещё не достаточно, чтобы с уверенностью отнести аутоаллергические болезни к группе генетических.
Третий путь развития аутоаллергических болезней — активация иммунологических механизмов против микрофлоры, имеющей общие антигены с антигенами макро организма. В процессе приспособления к существованию в макро организме у многих микробов появились антигены, общие с антигенами хозяина. Это тормозит включение иммунологических механизмов защиты против такой микрофлоры, так как по отношению к своим антигенам в организме существует иммунологическая толерантность и такие микробные антигены принимаются как свои. Однако в силу какихто различий в строе¬нии общих антигенов все же происходит включение иммунологических механизмов защиты против микрофлоры, что одновременно ведёт и к повреждению собственных тканей. Предполагают участие такого механизма в развитии ревматизма в связи с наличием общих антигенов у некоторых штаммов стрептококка группы А и в ткани сердца, язвенного колита в связи с наличием общих антигенов в слизистой оболочке толстой кишки и у некоторых штаммов Е. coli, в некоторых случаях инфекционно-аллергической формы бронхиальной астмы в связи с наличием общих антигенов в ткани лёгкого и у микрофлоры, вегетирующей в дыхательных путях.
Независимо от патогенетического пути развития аутоаллергические болезни повреждение тканей может вызываться четырьмя иммунологическими (аллергическими) механизмами. Из них три механизма химергические, то есть связанные с действием аутоантител, и четвёртый — китергический, или клеточный (смотри Аллергия). Первый механизм повреждения связан с образованием аллергических антител типа реагинов, которые фиксируются на поверхности клеток и при соединении с аллергеном вызывают освобождение вазоактивных аминов. Последние вызывают нарушение микроциркуляции и другие повреждения. Второй механизм — цитотоксический. Образовавшиеся антитела соединяются с соответствующими клетками и ока¬зывают на них цитотоксическое и цитолитическое действие двумя путями. Прямой путь реализуется через активацию всех компонентов комплемента. Непрямой путь включает участие в этом процессе нейтрофилов, которые освобождают повреждающие факторы. Третий механизм — токсическое действие иммунного комплекса антиген + антитело. Этот комплекс фиксируется в тканях, особенно в стенках кровеносных сосудов. Преципитат фиксирует и активирует комплемент. Это ведет к аккумуляции в данной ткани нейтрофилов, которые фагоцитируют комплекс и при этом выделяют гидролазы и другие факторы, вызывающие повреждение тканей. Четвертый механизм — аллергическая реакция замедленного типа. Все четыре механизма могут принимать участие в повреждении тканей, однако при различных аутоаллергических болезнях действует преимущественно один из них. Участие первого механизма в развитии аутоаллергических болезнях незначительно. Повреждающее действие цитотоксических аутоантител (второй механизм) наиболее чётко демонстрируется при аутоаллергических болезнях крови, повреждающее действие иммунных комплексов — при узелковом периартериите, системной красной волчанке; клеточный механизм — при аутоаллергическом тиреоидите, симпатической офтальмии.
Фактором, способствующим развитию аутоаллергических болезней, является нарушение функции желёз внутренней секреции. Так, например, при аутоаллергической болезни часто выявляется глюкокортикоидная недостаточность.
Патологическая анатомия аутоаллергических (аутоиммунных) процессов и болезней. Морфология аутоиммунных процессов и болезней представлена двумя категориями изменений, разных по своей иммунологической сущности. Первая, изучаемая общей иммуноморфологией, связана с напряжённым (или извращённым) иммуногенезом и ка¬сается в основном иммунокомпетентной системы. Изменения второй категории относятся к области частной иммуноморфологии и представлены морфологией местных иммунологических реакций, совершающихся в сенсибилизированном организме, то есть различными видами тканевой аллергии.
Иммуноморфологическое изучение аутоиммунных процессов и болезней основано на обязательном сопоставлении данных морфологического и иммунологического (функционального) исследований. Это значит, что морфология изменений в очаге иммунной реакции оценивается параллельно с помощью иммунологических (уровень антител и антигенов в крови, моче, лимфе) и морфологических показателей состояния иммунокомпетентной системы.
Для иммуноморфологического изучения аутоиммунных процессов и болезней используют три метода: 1) иммуногистохимический (иммуно-флюоресцентный) метод в различных его модификациях с использованием сочетания люминесцирующих антител или антигенов с радиоактивными метками и «контрастирующими» маркерами и привлечением для этого количественной оценки специфической люминесценции (микрофлюориметрии); 2) микроскопический метод (световая, поляризационная, электронная микроскопия) в сочетании с гистохимическими реакциями; 3) иммунологический метод (выявление антигенов и антител в тканях и жидкостях организма). Ведущее место среди них занимает иммуногистохимический метод, который служит не только для обнаружения иммунных комплексов, но и для их «расшифровки» (идентификация антигена, антитела, комплемента).
Морфология напряжённого иммуногенеза при аутоиммунных процессах и болезнях довольно стереотипна, хотя и зависит от особенностей иммуноло¬гической ситуации и длительности антигенной стимуляции. Она представлена лимфоретикулярной гиперплазией и плазмоцитарно-макрофагальной трансформацией с накоплением клеток, богатых РНК (иммунобласты, пиронинофильные клетки, плазматические клетки) и полисахаридами (PAS-клетки, макрофаги и другие), прежде всего в органах иммунокомпетентной системы (гиперплазия лимф, узлов, селезенки и другого) что отражает процессы клеточной секреции иммуноглобулинов (антителообразование) и продукцию рециркулирующих сенсибилизированных лимфоцитов. Гиперпластические реакции с накоплением лимфоретикулярных элементов и плазмоцитарно-макрофагальной трансформацией при аутоиммунных процессах и болезнях, как правило, выходят за пределы лимфоидной ткани. Они ярко представлены в ретикулоэндотелиальной (ретикулогистиоцитарной) системе печени, лёгких, почек, рыхлой соединительной ткани и могут имитировать картины межуточного воспаления и продуктивных васкулитов (если руководствоваться формально-морфологическими признаками). Выражением напряжённого иммуногенеза следует считать и нередко встречающийся миелоз внутренних органов. Процессы клеточной пролиферации, плазмоцитарно-макрофагальной трансформации и миелоидной метаплазии сопровождаются резкими нарушениями тканевого обмена, завершающимися в ряде случаев развитием тканевого диспротеиноза (накопление PAS-положи-тельного материала в лимфатических, узлах, амилоидоз селезенки, почек и так далее).
Морфология местного повреждения в связи с иммунологической реакцией определяется при аутоиммунных процессах и болезнях как природой антигена (перекрёстно реагирующий, аутологичный), длительностью его циркуляции в крови, так и качеством иммунного комплекса (циркулирующий комплементсвязывающий или местнообразованный за счёт структурного антигена ткани). При этом циркулирующие комплементсвязывающие иммунные комплексы способны обычно вызывать гиперергическое (иммунное) воспаление по типу немедленной аллергии, а местнообразующиеся иммунные комплексы, содержащие тканевой антиген, чаще ведут к развитию изменений по типу замедленной аллергии (смотри Аллергия). Однако это лишь крайние морфологические выражения местных иммунологических реакций. Доказано, что при аутоиммунных процессах и болезнях, индуцированных антигеном с образованием циркулирующих в крови комплементсвязывающих иммунных комплексов, воспалитель¬ные сосудистые и тканевые изменения, завершающиеся фибрино-подобным некрозом, развиваются в связи с гистопатогенным действием этих комплексов, что находит подтверждение при иммунофлюоресцентном исследовании биопсий. При этом специфика развивающихся иммунных повреждений в значительной мере зави¬сит от хим. структуры и величины иммунного комплекса. Например, гистологические и гистохимические особенности волчаночных изменений (гематоксилиновые тельца, кариорексис, выщелачивание ядер, резкая пиронинофилия и другое) связаны прежде всего с особенностью циркулирующего при волчанке иммунного комплекса, содержащего продукты распада клеточных ядер, нуклеопротеиды (антиген) и γG-глобулины (антинуклеарные антитела). Специфика морфологических изменений при ревматоидном артрите также определяется особенностью аутологичного иммунного комплекса и местом его образования. Установлено, что плазматические клетки синовиальных оболочек при ревматоидном артрите вырабатывают аномальные аутоантигенные γG-глобулины, что ведет к появлению антител к этому глобулину (γM-иммуноглобулины), образованию ревматоидного фактора, осаждению комплементсвязывающего крупномолекулярного иммунного комплекса и развитию воспалительно-некротических изменений. С парапротеиноиой макромолекулярной природой иммунного комплекса связано развитие часто встречающегося при ревматоидном артрите амилоидоза.
При истинных аутоиммунных заболеваниях (болезнь Хасимото, идиопатическая аддисонова болезнь, энцефалопатия, полиневрит, множественный склероз, асперматогония и другие), индуцированных органосноцифическим аутологичным антигеном, преобладают клеточные тканевые реакции. Морфология гиперчувствительности замедленного типа в виде лимфогистиоцитарной и макрофагальной реакции становится в этих случаях доминирующей (лимфоцитарный тиреоидит как морфологическое выражение болезни Хасимото). Хронический абактериальный гломерулонефрит, имеющий морфологию мембранозного или мембранозно-пролифсративного (мезангиально-мембранозного), может также рассматриваться как аутоиммунный, так как в развитии его важную роль играет структурный антиген базальной мембраны гломерулярного фильтра. При различных аутоиммунных процессах и болезнях нередки сочетания морфологии аллергии как немедленного, так и замедленного типа.
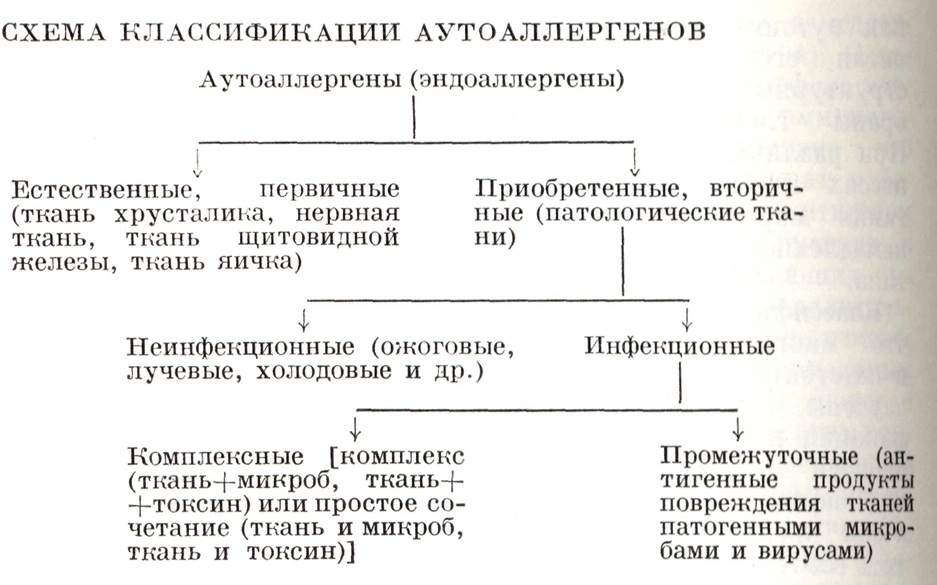
Классификация. В связи с тем, что многие проблемы этиологии и патогенеза аутоиммунных болезней ещё недостаточно изучены, общепринятой их классификации не существует. В качестве рабочей может быть использована классификация В. И. Иоффе (1963), в которой предпринята попытка разделить все аутоиммунные болезни по характеру аутоантигенов и механизмам аллергического (иммунологического) процесса и показать степень участия аутоаллергического процесса в развитии заболевания.
Основным недостатком этой классификации является нечёткое и неполное для современного уровня знаний изложение механизма аутоаллергических процессов. По этой классификации первую группу составляют истинные аутоиммунные болезни. Сюда включены заболевания, вызванные нарушением физиологической изоляции антигенов, по отношению к которым в организме нет иммунологической толерантности. Роль же аутоантител, которые, как и ранило, удаётся выявить в сыворотке больных, неизвестна, так как тканевые изменения имеют характер аллергической реакции замедленного типа. К этой группе с известной долей вероятности можно отнести следующие болезни: симпатическую офтальмию, аутоаллергический тиреоидит Хасимото (смотри Хасимото болезнь), демиелинизирующие процессы — энцефаломиелит, рассеянный склероз, некоторые формы полиневрита, орхита, идиопатическую аддисонову болезнь.
Ко второй группе относятся приобретенная гемолитическая анемия, тромбоцитопеническая пурпура (смотри Пурпура тромбоцитопеническая) и коллагеновые болезни. Антигены при этих заболеваниях не обладают органной специфичностью. Патогенез связан с нарушением гомеостатического контроля иммунологических механизмов. Несомненно, что не все аутоиммунные болезни, включаемые в эту группу, имеют в своей основе нарушение гомеостаза иммуногенеза. Так, например, группа коллагенозов включает ряд нозологических форм, по-видимому, с различным механизмом и различной степенью нарушения гомеостатических механизмов иммуногенеза. Наиболее доказательна его ведущая роль при системной красной волчанке.
К третьей группе аутоиммунных болезней относятся гломерулонефрит, гепатит, агранулоцитоз. Сюда включены болезни, при которых аутоантигенность тканей приобретается за счёт повреждающего действия внешних факторов (микробов, вирусов, лекарств) с образованием комплексных и промежуточных аутоаллергенов. К этой группе можно отнести также ревматизм и вакцинальный энцефаломиелит.
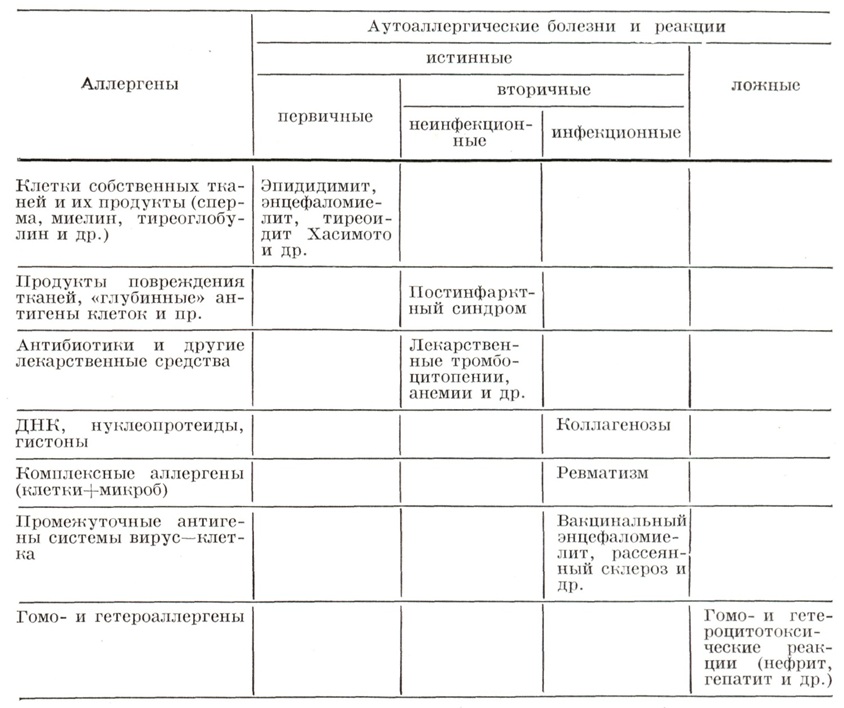
Более широкая классификация А. Д. Адо (1970) включает не только аутоиммунные болезни, но и аутоаллергические реакции (смотри таблицу). В основу этой классификации положены представления о характере аутоаллергенов (аутоантигенов), участвующих в аутоаллергическом процессе, и о самых общих чертах его патогенеза. По патогенезу все аутоаллергические реакции разделены на две группы: 1) истинные, вызываемые активно образованными в организме аутоантителами и сенсибилизированными лимфоцитами; 2) ложные, вызываемые введением в организм готовых антител.
Таблица. Аутоаллергические болезни и реакции, их связь с характером аллегенов
 |
 |
 |
В иммунологических механизмах повреждения тканей участвуют все указанные выше четыре механизма. По характеру аутоаллергенов истинные аллергические болезни и реакции разделены на первичные и вторичные.
Диагностика. Клиническим выражением напряжения иммуногенеза является увеличение лимфатических, узлов и селезёнки. Помимо типичных для каждой аутоиммунной болезни клинических признаков, большое значение для диагностики придается выявлению аутоантител в сыворотке больного. Последние могут быть выявлены различными, определенными для каждого заболевания тестами. При аутоаллергических гемолитических анемиях применяют прямой и непрямой тесты Кумбса (смотри Кумбса реакция). Для выявления противотканевых аутоантител применяют реакцию связывания комплемента, реакцию преципитации в геле по Оухтерлоню (смотри Преципитация), реакцию пассивной гемагглютинации по Бойдену (смотри Бойдена реакция). При некоторых аутоиммунных болезнях в сыворотке выявляются особые белки, по-видимому, имеющие отношение к аутоантителам, например ревматоидный фактор при ревматоидном артрите, волчаночный фактор при системной красной волчанке. Результатом действия противоядерных антител при последнем заболевании следует считать образование волчаночных (LE) клеток. Ориентировочное значение в диагностике имеет гипергаммаглобулинемия. Нередко, особенно в диагностике коллагенозов, применяется анализ материала биопсии тканей.
При многих аутоиммунных болезнях можно получить положительную кожную аллергическую реакцию замедленного типа на соответствующий тканевой гомоантиген.
Однако широкого применения в клинической практике этот метод пока не получил.
Прогноз. Наиболее общей чертой большинства аутоиммунных болезней является их тяжелое прогрессирующее течение, приводящее к необратимым нарушениям функции соответствующего органа или системы. Исключение составляют некоторые лекарственные гемопатии, имеющие благоприятный прогноз при отсутствии повторных контактов с соответствующими лекарствами. Введение в терапию аутоиммунных болезней кортикостероидов значительно продлило жизнь многих больных.
Принципы лечения. Практически при всех аутоиммунных болезнях приходится прибегать к лечению кортикостероидными гормонами, которые действуют как на основной механизм развития болезни, подавляя продукцию аутоантител, так и на вторичные изменения благодаря противовоспалительному действию и замещению недостатка эндогенных кортикостероидов. Схемы лечения различны для каждого заболевания. Как правило, необходимо длительное лечение в сочетании со средствами, снижающими возможность развития побочных реакций. Благоприятные результаты достигнуты, в частности, при комбинированном лечении кортикостероидами в сочетании с производными хинолина (делагил, резохин и другими).
При установлении диагноза лекарственных гемопатии необходимо прекращение контакта с антигеном (гаптеном). При идиопатических формах гемолитической анемии и тромбоцитопении в ряде случаев показана спленэктомия.
В последние годы изучается вопрос лечения аутоиммунных болезней цитостатическими препаратами (новэмбихин, тиоТЭФ и другими) и иммунодепрессантами типа 6-мер-каптопурина.
Профилактика. В связи с неясностью многих вопросов этиологии и патогенеза аутоиммунных болезней абсолютно действенных мер их профилактики пока нет. Предположительно можно говорить о профилактическом значении ограничения чрезмерных воздействий антигенных раздражителей, таких как вакцинация, лекарственная терапия, переливание крови, особенно в периоды наиболее лабильной реактивности организма.
Имеет значение также борьба с бытовым и производственным травматизмом, рациональное лечение хронических общих и очаговых инфекций, ограничение инсоляции, предупреждение переохлаждения. Для профилактики аутоиммунных болезней особенно важна тщательная оценка реактивности организма при выборе момента плановых оперативных вмешательств, бальнео- и физиотерапии.
 |
 |
 |
|
Адрианова H.В.; Пыцкий В.И.; Серов В.В. |

|
⇐ Перейти на главную страницу сайта |
⇑ Вернуться в начало страницы ⇑ |
Библиотека Ordo Deus ⇒ |
⇐ Аурикуло-темпоральный синдром |
⇓ Полный свод знаний. Том первый А. ⇓ |
Аутоаллергия ⇒ |
|
Все статьи в полном изложении, Вы можете найти в большой медицинской энциклопедии — Главный редактор: академик АН СССР (РАН) и АМН СССР (РАМН) Б.В. Петровский. — Москва издательство «Советская энциклопедия» 1989г. |
|
Внимание! Вы находитесь в библиотеке «Ordo Deus». Все книги в электронном варианте, содержащиеся в библиотеке «Ordo Deus», принадлежат их законным владельцам (авторам, переводчикам, издательствам). Все книги и статьи взяты из открытых источников и размещаются здесь только для чтения. |
|
Библиотека «Ordo Deus» не преследует никакой коммерческой выгоды. |
|
Все авторские права сохраняются за правообладателями. Если Вы являетесь автором данного документа и хотите дополнить его или изменить, уточнить реквизиты автора, опубликовать другие документы или возможно вы не желаете, чтобы какой-то из ваших материалов находился в библиотеке, пожалуйста, свяжитесь с нами по e-mail: |
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы не желаете закончить свой жизненный путь в виде омерзительной гниющей органической массы пожираемой копошащимися в ней могильными червями? Вы желаете вернувшись в молодость прожить ещё одну жизнь? Начать всё заново? Исправить совершённые ошибки? Осуществить несбывшиеся мечты? Перейдите по ссылке: «главная страница».
|
© Ordo Deus, 2010. При копировании ссылка на сайт http://www.ordodeus.ru обязательна. |