Опухоли |
||
 |
 |
Оглавление
|
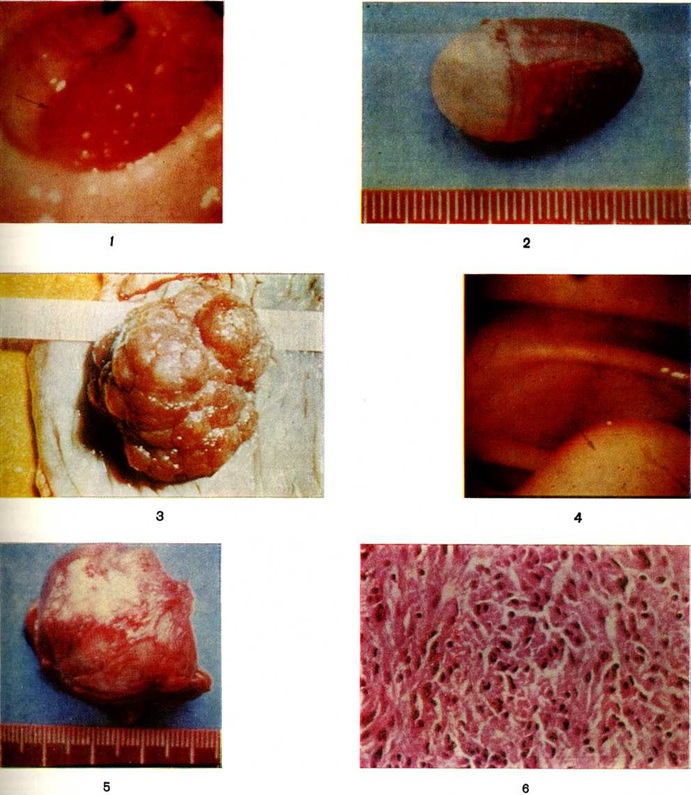
ОпухолиОпухоли (tumores; синонимы: бластомы, новообразования) — избыточное некоординированное с организмом патологическое разрастание тканей, продолжающееся после прекращения действия вызвавших его причин; состоят из качественно изменившихся клеток, ставших атипичными в отношении дифференцировки и характера роста, передающих эти свойства своим потомкам. Опухоли возникает с появления небольшой группы атипичных клеток, за счёт размножения которых происходит её рост., Основными признаками Опухоли являются её атипия (по строению, расположению и взаимоотношению клеток Опухоли отличаются в различной степени . от исходной ткани), .автономный рост (смотри полный свод знаний) и прогрессия опухоли (смотри полный свод знаний). Исследования в области онкогенеза, диагностика, лечение и профилактика. Опухоли являются предметом онкологии (смотри полный свод знаний). Различают доброкачественные и злокачественные Опухоли, например липома (цветной рисунок 1, 2) обладают экспансивным ростом, в результате которого окружающие ткани отодвигаются или раздвигаются иногда и сдавливаются и подвергаются атрофическим изменениям. Чёткие границы между опухолью и окружающими её тканями при экспансивном росте имитирует образование капсулы, хотя истинных капсул, например, подобных органным, у Опухоли нет. Злокачественные Опухоли инфильтрируют и разрушают окружающие ткани. Инфильтративный (инвазивный) рост является главным критерием, отличающим злокачественные Опухоли от доброкачественных. Для злокачественных Опухоли характерна также способность к метастазированию (смотри полный свод знаний). Существуют также так называемый местно деструирующие Опухоли, обладающие инфильтративным ростом, но, как правило, без тенденции к метастазированию. Оглавление Эпидемиология злокачественных опухолей Физико-химическая характеристика роста опухолей Влияние на организм злокачественных опухолей Номенклатура, строение, классификация Реабилитация онкологических больных Распространение в природеОпухоли описаны у всех классов и видов животных, а также у растений. Разрастания паренхимы растений могут напоминать Опухоли животных. Некоторые Опухоли растений, например, так называемый корончатые галлы, состоят из стойко изменённых клеток, сходных по биологический особенностям с клетками Опухоли животных. У насекомых наиболее известна меланома плодовой мушки дрозофилы. Эта опухоль изредка возникает спонтанно может быть вызвана также в эксперименте под воздействием ионизирующего излучения. Опухоли встречаются во многих семействах рыб, по-видимому, чаще всего у костистых. У рыб описаны доброкачественные (фиброма, липома, миксома, хондрома, остеома) и злокачественные (различные типы Сарком) опухоли. У форели, обитающей в водоёмах Швейцарии и Новой Зеландии, встречаются аденомы и аденокарцинома щитовидной железы. |
Возникновение Опухоли у рыб может служить индикатором загрязнения водоёмов онкогенными веществами. Значительная концентрация в корме афлатоксина В или ДДТ приводит к возникновению у форели Опухоли печени. Аквариумные рыбки гуппи могут служить объектом для экспериментального изучения онкогенного действия ряда нитрозосоединений. Штих (H.-F. Stich) в 1975 год в акватории порта Ванкувер, сильно загрязнённой бензпиреном, обнаружил значительное количество Опухоли (папиллом) у камбалы. Такие Опухоли практически не встречаются у рыб, выловленных в менее загрязнённых водоёмах.
Спонтанные Опухоли различной локализации встречаются у амфибий. Чаще всего обнаруживают эпителиальные Опухоли у лягушек, например, множественные аденомы желёз кожи и опухоли мочеполовой системы. У аксолотля встречаются меланома, эпителиома, нейроэпителиома и аденокарцинома.
Среди рептилий фиброма желудка и рак яичников описаны у питона, рак поджелудочной железы и злокачественная меланома — у сосновых змей, фиброаденомы лёгких,—черепах.
Практически все типы Опухоли, известные в патологии млекопитающих, встречаются у птиц. При этом частота их у птиц различных видов не одинакова; например, у гусей и уток Опухоли встречается реже, чем у кур. Из птиц, живущих в зоопарках, особенно часты, и разнообразны у волнистых попугаев. По данным И. И. Касьяненко (1964, 1978), 75% всех Опухоли у кур составляют гемобластозы, а из общего числа других опухолей свыше 59% приходится на опухоли мочеполовой системы. Встречаются также фибромы и разнообразные саркомы. Некоторые из сарком, например так называемые саркомы Рауса, обладают способностью перевиваться фильтратами. Среди гемобластозов кур встречаются различные формы, многие из которых, например болезнь Марека, являются вирусными заболеваниями.
Частота опухолей кроветворной системы у кур, как показывают данные некоторых исследователей, возрастает при введении в рацион питания таких продуктов, как костная и рыбная мука, которые могут содержать онкогенные нитрозосоединения.
Доброкачественные и злокачественные Опухоли встречаются у всех видов млекопитающих. При этом одноименные Опухоли у разных животных морфологически обычно сходны между собой и частота их увеличивается с возрастом. В частоте возникновения Опухоли вообще и в частоте возникновения Опухоли отдельных локализаций Существуют видовые различия. Например, рак лёгкого, желудка, толстой кишки являются частыми злокачественными Опухоли человека и редко встречаются у большинства видов млекопитающих. Примерно 90% всех злокачественных Опухоли человека имеют эпителиальное происхождение, в то время как у некоторых видов животных самыми частыми злокачественными Опухоли являются гемобластозы (у крупного рогатого скота, лошадей и свиней — около 80% всех Опухоли, а у овец— около 90%). У собак примерно 50% всех злокачественных Опухоли составляют саркомы, среди которых особый интерес представляет так называемый трансмиссивная саркома наружных половых органов, передающаяся половым путём. У самок собак самыми частыми являются Опухоли молочных желёз, нередко имеющие строение карциносарком. Частота Опухоли у собак разных пород различна; например, по данным Н. А. Краевского и В. И. Пономарькова (1979), гемобластозы наблюдаются у боксёров в 6 раз чаще, чем у других пород, а остеогенные саркомы встречаются почти исключительно у крупных собак. У лошадей светлой масти часто встречается меланома кожи.
У кошек наибольший интерес представляют лимфосаркомы вирусной природы. У мышей и крыс частота спонтанных Опухоли в значительной мере определяется принадлежностью их к тем или иным инбредным линиям. У одних линий мышей преобладают гемобластозы, у других — аденокарцинома молочных желёз,, у третьих — аденомы лёгких, у четвертых — гепатомы. У крыс наиболее часто встречаются фиброаденомы молочных желёз, Опухоли гипофиза, матки, сальных желёз наружного слухового прохода, гемобластозы; у золотистых хомячков часто обнаруживаются Опухоли надпочечников и преджелудка.
У кроликов самой частой является аденокарцинома матки, реже встречаются Опухоли почек, молочных желёз и другие. Спонтанные Опухоли (лёгких, половых органов и молочных желёз) редко встречаются у морских свинок и индуцируются также с трудом (как правило, лишь очень большими дозами онкогенных веществ). Описаны Опухоли молочной железы у пеструшки, спонтанные железистые Опухоли желудка типа карциноидов, а также Опухоли печени, почек, кроветворной ткани у южноафриканского грызуна мастомиса. У обезьян Опухоли встречаются практически во всех органах и тканях, у самок сравнительно часты Опухоли молочных желёз и яичников.
Статистика
Первые наблюдения распространении злокачественных Опухоли появились в 15 век, когда в городе Шнееберге (Саксония) было отмечено более частое возникновение Опухоли у шахтёров, чем у рабочих других специальностей. В 1728 год в Лондоне была сделана первая попытка регистрации больных раком. В 19 век опубликованы результаты исследований, характеризующие смертность от злокачественных Опухоли. Однако недостаточный учёт не давал возможности сделать какие-либо выводы об особенностях распространения Опухоли
Заболеваемость и смертность от злокачественных Опухоли в России стали изучать в начале 20 век. Первые работы по статистике злокачественных Опухоли проводили Л. Л. Левшин, С. А. Новосельский, А. В. Говоров, И. Э. Гаген-Торн, Н. А. Вельяминов, Сведения о регистрации больных злокачественными Опухоли, подготовленные в 1913 год В. П. Гейнацем для Всероссийской гигиенической выставки, были дополнены Н. Н. Петровым в его докладе на III Международной конференции онкологов в Брюсселе. Однако эти данные не давали представления об истинном распространении Опухоли в 90 губерниях и 7 крупных городах России, где они были собраны. Только после победы Великой Октябрьской социалистической революции наряду с организацией онкологической службы (смотри полный свод знаний) получила развитие государственная система мероприятий по углублённым статистическим исследованиям в области онкологии. В 1932 год в Украинской ССР введена система специального учёта больных злокачественными Опухоли С 1939 год во всех городах, имеющих онкологическое учреждения, началась обязательная регистрация больных с впервые установленным диагнозом злокачественной Опухоли, а с 1953 год такая регистрация стала проводиться повсеместно. В течение 70-х годы в СССР проведены мероприятия по совершенствованию онкологическое статистики, переходу к системе централизованного учёта больных злокачественными Опухоли с обработкой данных с помощью ЭВМ.
При обнаружении злокачественной Опухоли врач заполняет специальное извещение о больном с впервые в жизни установленным диагнозом рака или другой злокачественной Опухоли При этом в онкологическое учреждениях заполняют «Контрольную карту диспансерного наблюдения» за больным злокачественным новообразованием. Статистические данные накапливаются в организационно-методических отделах онкологическое диспансеров, статистических бюро органов здравоохранения и обобщаются Управлением медицинской статистики и вычислительной техники MЗ СССР совместно с НИИ онкологии имени Н. Н. Петрова МЗ СССР. В ряде стран принято проводить выборочные исследования с экстраполяцией данных на все население страны. Имеются популяционные и больничные регистры Опухоли Данные больничных регистров охватывают лишь часть больных злокачественными Опухоли, подлежащих стационарному лечению. В ГДР, Дании, Норвегии, Финляндии и Швеции имеются популяционные регистры рака. В СССР и некоторых других странах — членах СЭВ эту функцию выполняют регистры онкологическое диспансеров и НИИ онкологии.
 |

|  |
| ||
В экономически развитых странах Опухоли занимают второе место (15—23%, по данным ВОЗ) в общей структуре смертности, уступая смертности от сердечно-сосудистых заболеваний. Показатели смертности от злокачественных Опухоли на 100 000 населения в 1950 и 1976 годы составили в США соответственно 141,2 и 175,8, в Англии — 197,0 и 255,4, Японии — 78,9 и 125,3.
Во всем мире ежегодно заболевает злокачественными Опухоли свыше 6,3 миллионов человек, а умирает от них не менее 4,3 миллионов человек Рост смертности от злокачественных Опухоли происходит в основном за счёт рака лёгкого, молочной железы и прямой кишки. Число онкологическое больных в СССР, как и во многих других экономически развитых странах, сохраняет тенденцию к росту, особенно среди мужчин. Мужчины в среднем в 1½ раза чаще, чем женщины, заболевают Опухоли лимфатической и кроветворной ткани, в 2 раза чаще — Опухоли желудка и пищевода и в 4½ раза чаще — Опухоли лёгких. Отмечается тенденция к снижению заболеваемости в СССР злокачественными Опухоли пищевода, желудка, шейки матки, однако нарастают показатели заболеваемости злокачественными Опухоли лёгких, молочной железы и прямой кишки (таблица 1).
Рост смертности от злокачественных Опухоли в первую очередь может быть обусловлен резким снижением смертности от инфекционных, паразитарных и других болезней, а также постарением населения. Большое значение в изучении показателей смертности имеют общие для многих стран особенности её динамики. Анализ показателей смертности от онкологическое заболеваний за период с 1960 по 1978 год свидетельствует о том, что темпы её роста в СССР существенно замедлились. В 70-е годы заметно снизились показатели смертности от Опухоли пищевода и желудка, тогда как смертность от Опухоли лёгких, молочной железы, прямой кишки повысилась (таблица 2).
 |

|  |
| ||
В СССР принято сведения о всех умерших от Опухоли, не состоявших при жизни на учёте в онкологическое учреждениях, включать в данные о впервые заболевших в текущем году. Удельный вес посмертно зарегистрированных больных злокачественными Опухоли среди всех больных с впервые установленным диагнозом злокачественной опухоли составляет в среднем 2,3% (1977). Отмечается снижение показателей заболеваемости и смертности от Опухоли ряда локализаций, что связано с улучшением качества диагностики, развитием и внедрением в практику комплексных методов лечения.
Эпидемиология злокачественных опухолей
Предметом эпидемиологии Опухоли является изучение причин возникновения и закономерностей распространения Опухоли в зависимости от биологических и природных факторов, условий социальной среды отдельных групп населения. Основная задача эпидемиологии Опухоли заключается в накоплении и анализе материалов по этиологии и патогенезу Опухоли, на основании которых можно разрабатывать рациональные методы профилактики и лечения. Комплексное влияние профессиональных и бытовых факторов, индивидуальные особенности организма (с учётом сочетанного влияния этих факторов) создают условия, при которых одни группы населения попадают в так называемый группы риска, а другие избегают этой опасности. По данным Долла (R. Doll) и Хиггинсона (J. Higginson), низкие показатели заболеваемости Опухоли свидетельствуют о так называемый естественном, обычном уровне опухолевых заболеваний, а повышение этих показателей указывает на роль тех или иных факторов окружающей среды. По данным Комитета по профилактике рака ВОЗ, до 90% опухолей связано с воздействием внешних факторов, а 10% зависят от генетических факторов и вирусов.
В эпидемиологии Опухоли используют в основном методы, общепринятые в эпидемиологии, социальной гигиене и медицинский географии.
Л.. А. Зильбер считал, что проведение эпидемиологические исследований Опухоли может способствовать установлению вирусогенетического происхождения некоторых форм злокачественных Опухоли Это оправдалось на примере изучения эпидемиологии болезни Беркитта, и выделение вируса Эпстайна— Барр оказалось важным звеном в цепи этих исследований. Выделение вируса лейкоза кошек, наблюдения за болезнью Марека у кур и лейкозами рогатого скота вызвали необходимость глубоких исследований заболеваемости Опухоли у домашних животных. В этом плане представляет интерес изучение роли вирусов домашних животных для человека, и наоборот, возможность заражения в эксперименте обезьян материалом, взятым от больных лейкозом. Экспериментальные исследования показали возможность получения путём инбридинга (смотри полный свод знаний) высокораковых линий лабораторный животных. У домашних животных, например, у собак, в малых по численности породах чаще возникают определённые формы злокачественных Опухоли, что объясняют близкородственными скрещиваниями. Аналогичные наблюдения отмечены в малых народностях, у жителей отдельных островов и другие
В комплекс исследований эпидемиологии Опухоли входит изучение производственных, бытовых и климатогеографических факторов, оценка приспособительных механизмов организма, частоты возникновения отдельных Опухоли в различных местностях с учётом миграции, этнической принадлежности и степени адаптации; роли наследственных факторов, а также значения нарушений гормональных, обменных и других функций организма.
В эпидемиологии Опухоли широко используются демографические данные, материалы санитарный статистики, результаты социальных, в том числе экспедиционных, обследований различных групп населения. Кроме того, подвергаются анализу и используются данные клинико-диагностических обследований, проводимых с профилактической целью. В комплекс изучения Опухоли входят анализ динамики заболеваемости, а также углублённые исследования Опухоли в выборочных группах населения на отдельных территориях. Большую роль играют унифицированные критерии оценки результатов исследований с применением математических методов. Развитие автоматических систем сбора информации расширяет возможности эпидемиологические исследования. Особую роль эпидемиологические исследования играют при изучении производственных факторов, имеющих значение для возникновения опухолей. В комплексе с экспериментальными исследованиями они дают возможность определить группы риска и выработать систему профилактических мероприятий. Эпидемиологический наблюдения указывают возможные направления экспериментальных исследований онкогенеза. В то же время экспериментальные данные подсказывают необходимость эпидемиологических исследований не только в производственной сфере, но и при изучении влияния бытовых факторов на возникновение Опухоли
Основными этапами исследований являются: определение особенностей распространения Опухоли на изучаемой территории или в отдельных избранных группах населения; разработка рабочей гипотезы, на основе которой проводится оценка, группировка и отбор возможных причинных факторов для составления программированной карты обследования; специальное аналитическое исследование на основе информации, собранной по программированным картам обследования; экспериментальная проверка результатов аналитического обследования; разработка профилактических мер.
Важными источниками сведений для эпидемиологические анализа Опухоли являются демографические показатели, характеризующие степень миграции и плотность населения, а также данные об экономике р-нов проживания изучаемых групп. Сюда входит ряд показателей, касающихся не только задымлённости, загрязнённости среды, наличия бытовых и производственных аллергенов, но и соц.-гигиенические условий, влияющих на состояние здоровья населения. Так, должны быть произведены геологическая и географическая характеристика местности, оценка химический состава почв и воды, климатических и метеорологические факторов, особенностей пищи и характера её приготовления.
В комплекс организованных исследований входит также применение метода картографирования Опухоли с составлением атласов для отдельных территорий, сопоставление с геологическими, метеорологическими и другими параметрами тех же территорий.
Значительная роль в эпидемиологии Опухоли принадлежит ретроспективным исследованиям, основанным на сопоставлении групп больных и здоровых лиц в отношении подверженности их влиянию комплекса изучаемых факторов, а также генетической предрасположенности к возникновению Опухоли Известно свыше 100 наследственных синдромов, например, множественный полипоз толстой кишки со склонностью к малигнизации (синдром Гарднера), синдром Пейтца—Егерса, распространённый полипоз желудочно-кишечные тракта, особенно тонкой кишки, ретинобластома, опухоль Вильмса, пигментная ксеродерма, нейрофиброматоз и ряд других. Частота некоторых злокачественных Опухоли в популяции зачастую сказывается в учащении появления их в отдельных семьях, и только с помощью специальных исследований может быть отдифференцирована при этом роль генетических факторов. Определение степени предрасположения к развитию злокачественных Опухоли в семьях, в которых наблюдались онкол. заболевания, производится с помощью популяционно-генетических и эпидемиологические исследований. Клинико-генеалогический метод даёт возможность выявить путём опроса и изучения учётных документов частоту злокачественных Опухоли в родословных и установить частоту отдельных Опухоли в семьях. Описаны семьи с относительно высокой частотой злокачественных Опухоли в нескольких поколениях. При этом отмечается семейная предрасположенность к раку желудка, молочной железы, лейкозам и меланоме. По данным А. И. Ариона (1978), заболеваемость раком желудка у мужчин первой степени родства оказалась в 1,9 раза выше, а у родственников женщин — в 2,3 раза выше, чем в контрольной группе. Рак молочной железы у родственников первой степени родства также встречается чаще, а у родственниц в климактерическом периоде он наблюдается чаще в 5,2 раза. Преимущественное поражение некоторых этнических групп населения опухолями пищевода (казахи, татары, монголы и другие) может также свидетельствовать о роли генетического фактора.
Этиология и патогенез
В этиологии Опухоли большое значение придают действию ионизирующего излучения (смотри полный свод знаний), онкогенных веществ (смотри полный свод знаний) и вирусов (смотри полный свод знаний Онкогенные вирусы), которое в ряде случаев может быть сочетанным. При этом онкогенный эффект может быть усилен неонкогенными агентами и модифицирован различными факторами. В этиологии тех или иных Опухоли могут преобладать различные этиологического факторы. Так, например, среди причин рака кожи большое значение имеет УФ-излучение, среди причин рака лёгкого, а вероятно и гортани, наибольшее значение придают вдыханию онкогенных веществ из загрязнённого ими атмосферного воздуха, например, при курении. Важную роль могут сыграть нарушения процесса самоочищения лёгких, связанные, например, с хронический бронхитом и другими заболеваниями, которые способствуют задержке и депонированию в лёгких онкогенных веществ. Этиологического факторами, приводящими к развитию рака мочевого пузыря, в одних случаях могут оказаться онкогенные циклические амины, в других — эндогенные бластомогенные дериваты триптофана или тирозина. Способствовать действию онкогенных веществ на слизистую оболочку мочевого пузыря могут нарушения обмена эндогенных метаболитов, повреждения ферментных систем, застой мочи и другие Этиология многих Опухоли, например, рака тела матки, а отчасти и шейки матки, опухолей молочной, предстательной, щитовидной желёз, гипофиза, надпочечников и другие, основана на дисгормональных сдвигах в организме. Фактов, которые, несомненно, свидетельствовали бы об этиологического роли онкогенных вирусов при наиболее часто встречающихся злокачественных Опухоли человека, не получено. Общепринято представление о том, что онкогенные агенты действуют на те макромолекулы клетки, которые определяют синтез белка, а следовательно, рост, размножение, дифференцировку и поведение клеток. В результате, по-видимому, многостадийного процесса возникают клоны клеток, подвергающихся малигнизации (смотри полный свод знаний Онкогенез).
Биология опухолевого роста
В основе возникновения Опухоли лежит появление и размножение в организме опухолевых клеток, способных передавать приобретённые ими свойства в бесконечном ряду поколений (смотри полный свод знаний Онкогенез). Поэтому опухолевые клетки рассматривают как генетически изменённые. Деление предсуществующих опухолевых клеток — основной и в подавляющем большинстве случаев единственный способ роста Опухоли Первичные узлы многих Опухоли человека и животных представляют собой клоны, то есть состоят из клеток, являющихся потомками одной опухолевой клетки. При злокачественных Опухоли перенос и размножение опухолевых клеток в других тканях приводит к образованию метастазов. В условиях эксперимента опухолевые клетки можно трансплантировать из одного организма в другой, а также выращивать и длительно пассировать в клеточных культурах (смотри полный свод знаний Культуры клеток и тканей, в онкологии). В процессе роста Опухоли свойства популяции опухолевых клеток могут меняться, по-видимому, вследствие того, что возникающие новые варианты опухолевых клеток могут приобретать отдельные свойства, отличные от родительских. В культурах клеток можно создавать специальные условия, при которых в них накапливаются варианты опухолевых клеток, менее отличающиеся от нормальных клеток, чем большинство клеток культуры.
Различия между нормальными и опухолевыми клетками возникают в связи с изменениями генома, приводящими к появлению у клетки опухолевых свойств, и характером фенотипических изменений структуры и функции клетки. Существует несколько типов изменений генома, приводящих к появлению опухолевых клеток: 1) интеграция генома онкогенного вируса с геномом клетки, являющаяся основой опухолевой трансформации, вызываемой онкогенными вирусами; 2) мутация клеточного генома (вопрос о специфических генных мутациях, отличающих опухолевые клетки от нормальных, пока неясен; имеются данные о характерных перестройках структуры хромосом в клетках некоторых типов Опухоли и лейкозов); 3) эпигеномные изменения — стойкие изменения генетических свойств, сопровождающие дифференцировку клеток в их эмбриональном развитии. Изменение дифференцировки является характерной чертой многих опухолевых клеток, однако отсутствуют доказательства того, что генетические различия между опухолевыми и сходными нормальными клетками сводятся только к эпигеномным изменениям. При развитии Опухоли, а также на разных стадиях прогрессии одной и той же опухоли роль разных типов генетических изменений может быть различной.
Для опухолевых клеток характерны нарушения реакции на действие факторов микросреды, окружающей клетки в организме (гуморальные факторы, соседние клетки, коллагеновые волокна, базальные мембраны и другие). Наиболее характерными из них являются нарушения регуляции размножения, дифференцировки и образования контактов клетки с различными поверхностями, например, с дном культурального сосуда. Нарушения регуляции размножения у опухолевых клеток состоят в исчезновении способности менять темп размножения в зависимости от влияния регулирующих факторов микросреды. К проявлениям нарушения реакции на гуморальные факторы относится снижение гормональной зависимости роста у многих типов опухолевых клеток: такие клетки приобретают способность к митозу в отсутствие гормонов, которые были необходимы для размножения исходных нормальных клеток. В культуре клеток минимальные концентрации сыворотки, кальция и некоторых других компонентов микросреды, необходимых для их размножения, оказываются нередко более низкими для опухолевых клеток, чем для исходных нормальных.
В ходе прогрессии Опухоли могут утрачиваться многие признаки дифференцировки опухолевых клеток, что является одним из проявлений анаплазии (смотри полный свод знаний). Однако у большинства типов опухолевых клеток сохраняются те или иные признаки тканевой дифференцировки, которые характерны для исходных нормальных клеток. Особой формой нарушений дифференцировки опухолевой ткани можно считать появление способности к синтезу эмбрио специфических белков, то есть белков, которые сходная нормальная ткань синтезирует лишь в эмбриональном периоде, например, эмбриоспецифического печёночного белка альфа-фетопротеина. Степень дифференцировки опухолевой ткани иногда можно, существенно повысить, изменив условия, в которых растут опухолевые клетки. Например, А. Д. Тимофеевскому (1946) удалось добиться повышения степени дифференцировки клеток рабдомиобластомы в культуре ткани; Минтц (В. Mintz) с сотрудники (1976—1977) получила подобные результаты при пересадке клеток мышиной тератобластомы в окружение нормальных эмбриональных клеток.
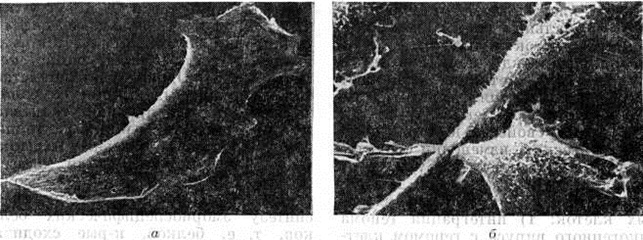
Размножение опухолевых клеток в культуре может стать независимым от контакта с подложкой — дном культурального сосуда и проходить в неприкреплённом суспензированном состоянии, тогда как в норме фибробласты и эпителиальные клетки размножаются лишь после прикрепления к такой подложке. При культивировании клеток обнаруживают также нарушения зависимости размножения от контактов с другими клетками: при достижении критической плотности клеточной популяции (определённого числа клеток на единицу площади подложки) размножение нормальных клеток прекращается, тогда как размножение опухолевых клеток может продолжаться. Нарушение образования контактов опухолевой клетки с различными поверхностями состоит в том, что они в культуре ткани слабее, чем нормальные, прикрепляются к неклеточным подложкам (например, стенкам культурального сосуда), менее распластываются на таких подложках и хуже образуют межклеточные контакты (рисунок). Это, вероятно, является причиной многих нарушений структуры опухолевой ткани в организме.
Опухолевые клетки способны селективно расти и распространяться в тканях потому, что они менее зависимы от, регулирующих факторов микросреды, чем гомологичные нормальные клетки. На ранних стадиях прогрессии Опухоли такое распространение может быть ограничено территорией, специфичной для клеток данного тканевого типа; например, эпителиальные опухолевые клетки карцином in situ Могут распространяться в пределах эпителиального пласта, не прорастая базальную мембрану. На более поздних стадиях прогрессии опухоли рост её может стать инвазивным, то есть опухолевые клетки начинают распространяться в окружающую ткань. Для роста и распространения опухолевых клеток в организме существенно то, что многие из них способны индуцировать в окружающей нормальной ткани размножение клеток соединительной ткани и капилляров (строматогенное и ангиогенное действие опухолевых клеток), что обеспечивает создание в опухолевой ткани сети питающих её сосудов. Индукция такой пролиферации связана с выделением опухолевыми клетками ангио генных факторов, по-видимому, имеющих белковую природу.
В процессе метастазирования может происходить отбор особых вариантов опухолевых клеток, отличающихся по своим свойствам от основной массы первичной Опухоли В эксперименте путём отбора удалось получить из одного опухолевого штамма несколько различных сублиний, резко различающихся по степени метастазирования и локализации метастазов, например, избирательно метастазирующих в лёгкие, мозг и другие органы. Это доказывает, что различия в характере метастазирования могут быть связаны с избирательным сродством некоторых типов опухолевых клеток к определённым тканям.
Природа изменений клеточных структур и функций, определяющих нарушенную реакцию опухолевых клеток на воздействие факторов микросреды, остаётся не вполне ясной. Центральную роль во взаимодействиях опухолевой клетки с микросредой играют её наружная мембрана с молекулами-рецепторами, а также расположенный под наружи ной мембраной клетки кортикальный слой, ответственный за движения мембраны и ряда внутриклеточных структур. Молекулы-рецепторы наружной мембраны опухолевой клетки могут взаимодействовать, например, с молекулами гормонов или поверхностей, с которыми контактирует опухолевая клетка. Это в ряде случаев сопровождается комплексной перестройкой клеточной мембраны с изменением её проницаемости (например, для кальция, натрия, сахаров), активности мембранных ферментов (например, аденилциклазы, катализирующей образование циклического 3-5-аденозинмонофосфата) у а также компонентов кортикального слоя. Эти сдвиги могут служить начальными этапами различных регуляторных перестроек клетки. По мнению многих исследователей, в основе нарушенной реактивности опухолевых клеток лежат изменения их поверхности. Так, на поверхности многих опухолевых клеток отсутствует белок фибронектин. который имеется на наружной поверхности исходных нормальных клеток. Описаны также изменения химический состава углеводных цепей, прикрепляющихся снаружи к некоторым белкам и липидам наружной мембраны опухолевой клетки. При взаимодействии с подложкой под мембраной нормальных клеток наблюдается характерное изменение кортикального слоя, в котором появляются пучки актиновых микрофиламентов. У многих типов опухолевых клеток такие пучки не образуются, что может свидетельствовать о нарушениях структуры кортикального слоя. Остаётся неясным, какие из изменений поверхности клеток наиболее специфичны для опухолевой трансформации; и важны для нарушений реактивности клеток.
Кинетика опухолевого роста. Скорость роста Опухоли зависит от нескольких кинетических характеристик опухолевой ткани: продолжительности митотического цикла опухолевых клеток, размеров .ростовой фракции (пролиферативного пула) и скорости гибели опухолевых клеток. Митотический цикл опухолевых клеток, так же как и нормальных клеток, состоит из пег скольких фаз: фазы G1 (пререпликативной), фазы S (синтеза ДНК), фазы (постсинтетической) и фазы М (собственно митоза). В обычных условиях популяции опухолевых клеток асинхронны, то есть в каждый момент времени клетки популяции распределены равномерно по разным фазам цикла. Средняя продолжительность митотического цикла (промежуток от митоза до следующего митоза, или время генерации) клеток разных Опухоли колеблется в пределах 16—60 часов, что обычно не меньше, чем у интенсивно размножающихся нормальных клеток взрослого организма. Ростовой фракцией называют выраженную в процентах часть клеток опухолевой популяции участвующих в митотическом цикле Ростовая фракция лишь в некоторых Опухоли приближается к 100%; в большинстве исследованных Опухоли животных и человека она составляет более низкую цифру (30—70%). часть о., в Опухоли имеется значительная фракция неразмножающихся клеток, что может быть результатом необратимой дифференцировки клеток (например, ороговения клеток в плоскоклеточном раке); повреждения клеток (например, в результате недостатка питательных веществ); обратимого перехода клеток из митотического цикла в так называемый фазу покоя (фазу G0).
В качестве показателя интенсивности гибели опухолевых клеток используют фактор потери клеток — процентное соотношение числа погибающих клеток к общему числу клеток, прибавившихся в популяции в результате клеточного деления за время одного цикла. В некоторых экспериментальных Опухоли и новообразованиях человека фактор потери клеток составляет 80—90% . Гибель опухолевых клеток чаще всего, пот видимому, является результатом недостатка питательных веществ в растущей Опухоли
Изменение каждого кинетического показателя опухолевого роста может приводить к изменениям скорости роста опухолевого узла; например, замедление роста Опухоли может быть результатом не только увеличения продолжительности митотического цикла, но и уменьшения ростовой фракции, а также увеличения числа гибнущих опухолевых клеток. Скорость роста Опухоли обычно определяют с помощью повторных измерений диаметра опухолевого узла. Рост ряда опухолевых узлов может быть описан как экспоненциальная функция при этом время удвоения числа опухолевых клеток в узле по мере его роста остаётся постоянным. Однако рост многих Опухоли значительно отклоняется от экспоненциального; чаще всего в этих случаях время удвоения числа опухолевых клеток увеличивается по мере роста узла. у Для определения кинетических показателей опухолевой ткани обычно используют радиоавтографические методы с применением тимидина, меченного тритием; для оценки распределения клеток по фазам митотического цикла можно использовать также метод проточной цитоспектрофотометрии. Имеющиеся методы определения ростовой фракции и фактора потери клеток недостаточно точны.
Биохимия
Биологических свойства опухолевой клетки не обусловлены специфическими для Опухоли белками, ферментами или общими для всех Опухоли метаболическими путями, отсутствующими в нормальных клетках организма в тот или иной период его индивидуального развития. Только в Опухоли, индуцированных ДНК содержащими онкогенными вирусами, обнаруживаются специфические белки, участвующие в трансформации этих клеток. Так называемый опухолеспецифические антигены во многих случаях оказались белками эмбрионального происхождения или компонентами онкогенного вируса. Опухоли способны синтезировать эмбриональные белки, например, альфа-фетопротеин, а также эмбриональные изоформы многих ферментов углеводного, азотистого И фосфорного обмена, например, пируваткиназы, тимидинкиназы, щелочной фосфатазы. В гепатомах экспериментальных животных появляется высокоактивная γ-глутамилтранспептидаза, синтезируемая также печенью эмбриона. Некоторые Опухоли иногда синтезируют не свойственные гомологичным тканям эктопические Гормоны; например, плоскоклеточный рак лёгкого в ряде случаев вырабатывает паратиреоидный гормон, овсяноклеточный рак лёгкого — адренокортикотропный гормон и другие Несомненно, что в опухолевой клетке нарушена регуляция процессов жизнедеятельности, и прежде всего обмена веществ. Однако не установлено, отклонение каких именно биохимический процессов обусловливает неконтролируемость роста Опухоли.
Опухоли Варбург открыл особенность энергетического обмена опухолевой клетки — интенсивный анаэробный гликолиз (смотри полный свод знаний), чему способствует, как позднее выяснилось, многократное повышение активности ферментов гексокиназы, фосфофруктокиназы и пируваткиназы, а также резко увеличенная проницаемость для глюкозы наружных мембран опухолевых клеток. Однако бластные клетки при остром лимфолейкозе сохраняют аэробный тип обмена, присущий их нормальным аналогам. Описанная также Варбургом способность опухолевой клетки к аэробному гликолизу оказалась неспецифичной и не проявляется при росте Опухоли в организме.
Опухоли характеризуется потенциально полноценным дыханием, хотя абсолютная активность в её клетках некоторых ферментов дыхательной цепи (цитохромоксидаза, оукциноксидаза) и содержание цитохрома-С понижены. Опухоли окисляют жирные кислоты и белки, а также глюкозу при её избытке. Дыхание Опухоли в организме ослаблено из-за недостаточного её снабжения кислородом, и основным источником энергии для неё служит анаэробный гликолиз. В результате резкого отставания скорости поступления глюкозы от скорости её обмена в ткани Опухоли поддерживается низкое, почти неуловимое, содержание глюкозы, что вызывает существенные сдвиги в гомеостазе. Опухоли реализует в организме лишь небольшую долю своей потенциальной способности к обмену глюкозы и потому может дополнительно поглощать вводимые извне огромные её количества до тех пор, пока уровень глюкозы в ней не уравняется с таковым в других тканях. Опухоли обладают пониженной способностью к синтезу жирных кислот из глюкозы и ацетата. Основное количество необходимых Опухоли липидов она получает из организма в виде липопротеидов очень низкой плотности и свободных жирных кислот в комплексе с альбумином.
Процессы синтеза белков и нуклеиновых кислот в Опухоли преобладают над процессами их распада. Хотя эта особенность присуща и нормальным растущим тканям, но в отличие от них в опухолевых клетках интенсивность распада белков, аминокислот и нуклеиновых кислот ничтожна. Опухоли получает от организма готовые аминокислоты. Особенно велика её потребность в глутамине и аспарагине. В опухолевой ткани отмечается многократное повышение активности ферментов, участвующих в синтезе пуриновых и пиримидиновых нуклеотидных предшественников нуклеиновых кислот с одновременным ослаблением активности ферментов их распада. .
Опухоли, как и любая растущая ткань, усиленно синтезирует полиамины — путресцин, спермидин, спермин. В плазме крови и моче значительной части онкологическое больных увеличено, содержание полиаминов, которое резко снижается после оперативного удаления Опухоли Уменьшение содержания полиаминов в плазме крови и моче и отношения спермидин/спермин может указывать на положительный эффект лечения противоопухолевыми средствами или лучевой терапии.
Для опухолевой ткани характерна биохимический деспециализация, нарушение дифференцировки и извращённая реакция (резистентность или, наоборот, сверхчувствительность) на контролирующие биохимический процессы факторы, в частности гормоны. Эти черты, однако, являются скорее вторичным признаком, результатом прогрессии Опухоли и почти не характерны для доброкачественных Опухоли
В перевиваемых Опухоли, особенно в злокачественных гепатомах, наблюдается выравнивание фосфолипидного состава плазматических, микросомных и митохондриальных мембран. В нормальных же гепатоцитах каждый из указанных типов мембран содержит специфические для него фосфолипиды. В злокачественных Опухоли человека, кроме острых лейкозов, наступает унификация изоферментного спектра лактатдегидрогеназы в сторону увеличения доли V и уменьшения доли I изоферментов. Резкое падение активности изофермента I лактатдегидрогеназы характерно также для доброкачественных Опухоли и бластных клеток при остром лимфо и миелобластном лейкозе. Последняя особенность универсальна для любой Опухоли, хотя биологический смысл явления остаётся неясным. В гепатомах исчезают некоторые специфичные для печени ферменты глюконеогенеза, резко снижается способность образовывать ацетоацетат из жирных кислот. В норме в печени и лейкоцитах подавляется синтез холестерина при избытке его в крови. В опухолевых клетках печени и крови этот механизм регуляции, как правило, утрачивается. Карцинома молочной железы может быть резистентна к эстрогенам и в случае сохранения цитозольных рецепторов к этим гормонам. Индуцированная диметилбензантраценом карцинома молочной железы крысы приобретает зависимость от инсулина: у животного с экспериментальным диабетом рост опухоли прекращается, гомологичные же нормальные клетки не чувствительны к инсулину.
В опухолевой клетке ослаблена избирательность переноса информационных РНК из ядра в цитоплазму, в которую попадает более богатый их набор, чем в покоящейся нормальной клетке. Сходное явление наблюдается и в активно пролиферирующих нормальных тканях.
Очевидно, что приспособляемость Опухоли к неблагоприятным условиям внутренней среды организма (низкое содержание кислорода, метаболитов, ионов и другие), не препятствующих её росту, должна обусловливаться соответствующими сдвигами в ферментном и рецепторном аппарате Опухоли.
Физико-химическая характеристика роста опухолей
Среди физико-химические характеристик роста Опухоли наибольшее значение имеет изучение спектров электронного парамагнитного резонанса опухолевых тканей Н. М. Эмануэлем и сотрудники, А. Н. Саприным, Швартцем (S. Опухоли Schwartz), Дюшеном (P. Y. Duchesne), Майли (Mylay) установлено, что опухолевые клетки характеризуются сигналами электронного парамагнитного резонанса (смотри полный свод знаний), отличными от таковых в гомологичных нормальных тканях. Существует определённая закономерность в изменении интенсивности сигналов электронного парамагнитного резонанса опухоли и нормальных тканей. Воздействия, приводящие к регрессии Опухоли или торможению её роста, сопровождаются нормализацией спектров электронного парамагнитного резонанса опухолевых клеток. В большинстве Опухоли животных и человека обнаружены необычные для биологический объектов сигналы электронного парамагнитного резонанса с триплетной структурой, которые обусловлены нитрозильными комплексами гемопротеинов, локализованными в митохондриях и микросомах. Образование этих комплексов сопряжено с развитием гипоксии в опухолевых клетках и восстановлением нитратов. Однако оказалось, что сигнал электронного парамагнитного резонанса не специфичен для Опухоли, так как обнаруживается при некоторых воздействиях в нормальных тканях и связан с развитием в них некротических изменений.
В процессе роста Опухоли интенсивность сигналов электронного парамагнитного резонанса в опухолевых клетках меняется. Концентрация свободных радикалов (смотри полный свод знаний), измеряемая методом электронного парамагнитного резонанса, в ряде Опухоли, например, рабдомиосаркоме, лимфосаркоме, выше, чем для гомологичных нормальных тканей, в других Опухоли, например, гепатоме, — ниже. Кинетика изменения концентрации свободных радикалов в Опухоли связана с закономерностями опухолевого роста.
Максимум концентрации свободных радикалов всегда по времени предшествует достижению максимальной скорости роста Опухоли
В опухолевой клетке наблюдается иная взаимосвязь между биофиз. характеристиками, чем в здоровых клетках, что может быть существенным в изменении чувствительности опухолевых клеток к регуляторным воздействиям. Важное значение имеют изменения липидобелковых взаимоотношений в мембранах опухолевых клеток, увеличение мембранного потенциала покоя, отрицательного заряда опухолевых клеток. Увеличение вязкости мембранных компонентов, изменение состава ганглиозидов и гликолипидов может быть одной из причин изменения контактного взаимодействия, узнавания клеток, чувствительности рецепторов к факторам, регулирующим рост.
Иммунология
Иммунологический отношения Опухоли и организма включают естественную резистентность организма к Опухоли, реакции приобретённого (специфического) иммунитета и иммунодепрессивное действие Опухоли на организм.
Естественная резистентность организма к Опухоли не обладает иммунологический специфичностью и не требует предварительной иммунизации. С помощью экспериментальных исследований установлено, что распознавание и отторжение единичных опухолевых клеток осуществляется иммунологический системой естественной резистентности. У животных и человека обнаружена особая разновидность лимфоцитов, оказывающих цитотоксическое действие на различные Опухоли Такие лимфоциты получили название NK-клеток или естественных киллеров. Природа их антигенсвязывающих рецепторов и механизм распознавания ими опухолевых клеток не выяснены. Эти лимфоциты присутствуют в организме в норме и не относятся к Т или В-лимфоцитам, количество их не увеличивается при росте Опухоли Другим важным фактором естественной резистентности организма к Опухоли являются макрофаги (смотри полный свод знаний). Активацией макрофагов, по-видимому, в основном обусловлен благоприятный эффект внутриопухолевого введения БЦЖ.
Реакции приобретённого (специфического) противоопухолевого иммунитета (смотри полный свод знаний Иммунитет противоопухолевый) вызываются специфическими опухолевыми антигенами, присутствующими в ряде Опухоли При этом иммуногенность Опухоли существенно зависит от её этиологии. Наиболее иммуногенными являются Опухоли, индуцированные экзогенными онкогенными вирусами. Геном этих вирусов, встраиваясь в геном клетки, индуцирует в ней синтез белков и гликопротеидов — собственно вирусных или не входящих в структуру вируса. Эти белки чужеродны для организма и потому иммуногенны. Если они присутствуют на клеточной мембране, то иммунологический реакция направлена не только против вируса, но и против опухолевой клетки и способна подавить её рост. Иммунитет осуществляется в этом случае иммунными лимфоцитами совместно с макрофагами, особыми лимфоцитами, распознающими клетки-мишени, покрытые антителами, и гуморальными антителами с участием комплемента. В разных системах преобладает тот или иной тип иммунологический воздействия на Опухоли Подобные иммунологический отношения Опухоли и организма распространены, например, при Опухоли, вызываемых вирусами папилломы и полиэмы у разных животных, вирусном лейкозе и саркоме кошек, лейкозах и саркомах мышей и крыс, вызываемых лабораторный штаммами соответствующих вирусов, вирусных лейкозах и саркомах кур, болезни Марека кур, эпизоотическом лейкозе крупного рогатого скота, вирусных лейкозах и саркомах обезьян. У человека к этой группе могут быть отнесены лимфома Беркитта и так паз. назофарингеальная карцинома. В образовании этих Опухоли принимает участие вирус группы герпеса (вирус Эпстайна—Барр), геном которого присутствует в клетках этих Опухоли Менее иммуногенны Опухоли, вызываемые вирусами, попадающими в организм с гаметами в форме про вируса (эндогенные вирусы) или с молоком матери, как, например, вирусы рака молочных желёз мышей. Антигены этих вирусов индуцируют в организме частичную или полную иммунологический толерантность (смотри полный свод знаний Толерантность иммунологическая), специфически подавляющую иммунный ответ на эти антигены.
При развитии подобных Опухоли обнаружена даже иммуностимуляция — усиление их роста при подавлении иммунной системы.
Особый вид противоопухолевого иммунитета выявлен при Опухоли животных, индуцированных сильными онкогенными веществами, например, метилхолантреном. Эти Опухоли, как правило, иммуногенны, но иммунитет к ним индивидуально специфичен, то есть направлен против данной опухоли со слабовыраженными перекрёстными реакциями по отношению к другим Опухоли Иммунитет осуществляется главным образом иммунными лимфоцитами — так называемый Т-киллерами. Природа и происхождение антигенов таких Опухоли не установлены.
Наиболее обширной группой являются спонтанные Опухоли неустановленной этиологии, возникающие вне явной зависимости от вирусных или других онкогенных факторов, характеризующиеся очень низкой иммуногенностью или даже её отсутствием. В спонтанных Опухоли чаще всего обнаруживаются эмбриональные антигены, слабоиммуногенные in vivo, но выявляемые с помощью реакций клеточного иммунитета in vitro. Эти антигены определяют перекрёстные иммунологический реакции между различными спонтанными Опухоли Природа антигенов иммуногенных спонтанных Опухоли не установлена. Исключение составляют клетки герминальных эмбриональных карцином мышей, в которых идентифицирован мембранный антиген, иммуногенный в сингенной системе.
В плазмоцитомах и В-лимфоцитарных лимфомах могут присутствовать моноклональные иммуноглобулины, связанные с клеточной мембраной. Каждый клон нормальных и соответственно опухолевых В-лимфоцитов продуцирует иммуноглобулин, содержащий уникальную детерминантную группу (идиотипическую детерминанту), являющуюся как бы специфическим иммунологический маркером данного клона. Идиотипические детерминанты иммуноглобулинов иммуногенны в сингенной системе и могут вызывать эффективный специфический противоопухолевый иммунитет.
В ряде случаев, например, при меланоме, у больных обнаруживают антитела, реагирующие с Опухоли, и специфическую реактивность лимфоцитов in vitro с клетками аутологичных Опухоли Эти реакции и возможность их использования для диагностических целей или иммунотерапии Опухоли усиленно изучается.
Прогрессия Опухоли, как правило, сопровождается иммуно депрессивным эффектом — ослаблением реакций повышенной чувствительности замедленного типа, снижением числа Т-лимфоцитов или их функциональный активности. В онкологическое практике используются иммуно л. тесты на гиперчувствительность замедленного типа и Т-лимфоциты, которые, помимо общей оценки иммунологический статуса больного, имеют и некоторое прогностическое значение.
Антигены, ассоциированные с Опухоли, в частности опухолево-эмбриональные антигены, используются для иммунологический диагностики и оценки эффективности лечения ряда Опухоли Так, при гепатоцеллюлярном раке печени, тератобластомах яичка и яичника определяют альфа-фетопротеин, при опухолях кишечника — раково-эмбриональный антиген, трофобластических опухолях — хориогенный гонадотропин и трофобластический бета-глобулин. Специфические антигены Т и В-лимфоцитов используют для дифференциации лимфом.
Влияние на организм злокачественных опухолей
Различают две основные взаимосвязанные формы системного действия на организм, общие для всех злокачественных Опухоли: конкуренцию с тканями организма за жизненно важные метаболиты и трофические факторы, а также влияние Опухоли на биологический характеристики различных тканей, приводящие к нарушению их дифференцировки и ослаблению регулирующего влияния со стороны организма.
Особенно существенны вызываемые Опухоли сдвиги в углеводном обмене. В злокачественных Опухоли человека в отличие от здоровых тканей не обнаруживается глюкоза. Благодаря этой особенности Опухоли способны «насасывать» глюкозу из крови. В этих условиях мобилизуются компенсаторные возможности организма — в первую очередь расходуются запасы гликогена печени и мышц. Основным же процессом, позволяющим организму в большинстве случаев покрывать убыль глюкозы, поглощаемой Опухоли, служит глюконеогенез, эндогенное образование глюкозы в печени и почках из не углеводных предшественников и в частности глюкогенных аминокислот и глицерина. В тех случаях, когда глюконеогенез не стимулирован или Опухоли имеют большие размеры, может наступить глубокая гипогликемия (смотри полный свод знаний). Описано около 150 случаев падения содержания сахара в крови до 6—15 миллиграмм на 100 миллилитров на фоне нормального или пониженного уровня инсулина в крови. Гипогликемическое влияние Опухоли можно выявить с помощью специальных приёмов даже в организме, поддерживающем нормогликемию, по напряжению компенсаторных процессов глюконеогенеза и расходованию гликогена. Как известно, глюконеогенез стимулируют глюкагон, гормон роста и особенно глюкокортикоиды. По данным многих исследователей, содержание глюкокортикоидов в крови и моче больных повышается в период интенсивного роста Опухоли Возможно, что сдвиг в гормональном балансе организма служит одной из причин иммунодепрессивного влияния Опухоли Повышение уровня фибриногена в крови онкол. больных можно объяснить действием глюкокортикоидов, стимулирующих синтез фибриногена в печени.
Опухолевая ткань является своеобразной ловушкой азота, как алиментарного, так и освобождающегося при распаде белков и нуклеиновых кислот. Введение в организм глюкозы сберегает азот, предупреждает возникновение отрицательного азотистого баланса, ослабляет катаболизм тканевых, в частности мышечных, белков. Эти факты свидетельствуют о роли гипогликемического влияния Опухоли как фактора, вызывающего сдвиги азотистого обмена. Часть аминокислот отвлекается в русло углеводного обмена (глюконеогенез), и в результате должен ослабляться синтез тканевых белков. В то же время их распад усиливается благодаря гиперфункции коры надпочечников, что способствует образованию свободных аминокислот как Материала для глюконеогенеза.
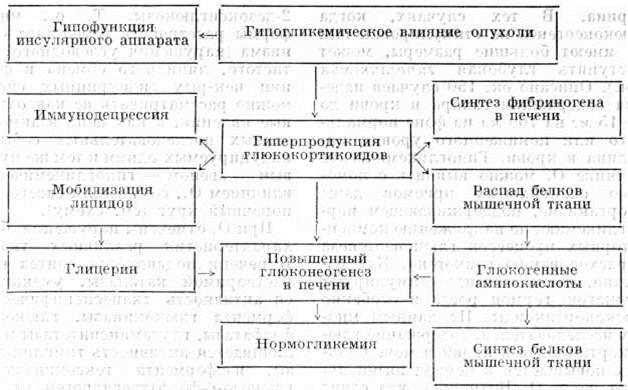
Рост Опухоли приводит к усиленной мобилизации липидов жировых депо и мышц. Этот процесс сопровождается гиперлипидемией (смотри полный свод знаний Jluneмия). Часть липидов ассимилируется Опухоли для образования мембран пролиферирующими опухолевыми клетками. Мобилизацию липидов рассматривают прежде всего как компенсаторную реакцию организма на гипогликемическое влияние Опухоли, позволяющую тканям при недостатке глюкозы использовать окисление жирных кислот как дополнительный источник энергии. Так, индуцированная гипергликемия останавливает мобилизацию липидов у лабораторный животных с экспериментальными Опухоли, в то же время её можно вызвать у здоровых животных введением в организм неассимилируемого структурного аналога глюкозы 2-дезоксиглюкозы. Таким образом, многие формы расстройств гомеостаза организма (нарушения углеводного, азотистого, липидного обмена и функции некоторых эндокринных систем) можно рассматривать не как отдельные явления, а как цепь взаимосвязанных последовательных событий, индуцируемых одним и тем же пусковым звеном — гипогликемическим влиянием Опухоли, создающим своего рода порочный круг (смотри полный свод знаний схему).
При Опухоли отмечены нарушения биологический характеристик различных тканей. В печени подавляется синтез водорастворимой каталазы, уменьшается активность тканеспецифического фермента глюкокиназы, глюкозо-6-фосфатазы, глутаминсинтетазы и увеличивается активность тимидинкиназы, изофермента гексокиназы-Ш, глюкозо-6-фосфатдегидрогеназы. В лизосомах печени повышается активность β-галактозидазы, арилсульфатазы, β-глюкуронидазы, катепсина и кислой рибонуклеазы. В лимфоидной ткани лабораторный животных с экспериментальными Опухоли, в лимфоцитах онкологическое больных понижена активность аденозиндезаминазы, что сопровождается накоплением крайне токсичного для лимфоцитов дезоксиаденозинтрифосфата.
В микросомах лабораторный животных с экспериментальными Опухоли резко ослабляется индуцируемость чужеродными соединениями ферментов. В результате такие животные становятся более чувствительными к действию некоторых фармакологических агентов. В микросомах и митохондриях этих животных усилено перекисное окисление ненасыщенных жирных кислот как результат обеднения печени антиоксидантом (а-токоферолом) и дисбаланса между ферментами, генерирующими перекиси липидов (NADР Н-зависимая диоксигеназа) и ферментами, ингибирующими этот процесс (О2-дисмутаза) и утилизирующими перекиси (глутатион-пероксидаза). В изолированных митохондриях клеток печени лабораторный животных с быстро растущими злокачественными Опухоли дыхание и фосфорилирование частично разобщено, но нормальное дыхательное фосфорилирование может быть восстановлено путём добавления в среду альбумина. Этот факт указывает на накопление в митохондриях высших ненасыщенных жирных кислот, которые являются эффективными разобщителями и легко связываются с альбумином. В печени лабораторный животных с некоторыми перевиваемыми Опухоли заметно повышен порог чувствительности к глюкокортикоидам. Например, у мышей с карциномой Эрлиха, у которых наступает гипогликемия, глюконеогенез остаётся на низком уровне и стимулируется лишь значительными дозами глюкокортикоидов.
 |
|  |
Схема расстройств гомеостаза, возникающих в организме при опухолевом росте. | ||
Пусковым звеном в расстройствах .гомеостаза, возникающих в организме при опухолевом росте, Служит гипогликемическое влияние опухоли. Оно вызывает гипофункцию инсулярного аппарата и стимулирует компенсаторные механизмы, обеспечивающие, как Правило, нормогликемию посредством гиперпродукции глюкокортикоидов которые стимулируют эндогенное образование глюкозы (глюконеогенез) из неуглеводных соединений (продуктов усиленного распада белков мышечной ткани — глюкогенных, аминокислот) и мобилизацию липидов С высвобождением глицерина. Гиперпродукция глюкокортикоидов вызывает также иммунодепрессию. Отвлечение части аминокислот в русло углеводного обмена нарушает синтез белков мышечной ткани, что наряду С другими изменениями приводит к мышечной дистрофии.
У больных раком желудка, лёгкого, молочной железы по мере распространения процесса наблюдается прогрессирующее снижение уровня иммунореактивного инсулина в сыворотке крови и нарушение зависимости между продукцией гормона передней доли гипофиза и гормонов других желёз внутренней секреции. В частности, резкое снижение содержания трийодтиронина происходит на фоне повышенного уровня содержания в крови тиреотропного гормона. При раке тела матки, молочной железы и прямой кишки нагрузка глюкозой не снижает уровня содержания гормона роста в крови, а в некоторых случаях эта нагрузка вызывает даже парадоксальную реакцию — гиперпродукцию гормона роста. У больных злокачественными Опухоли различной локализации повышен порог чувствительности гипоталамогипофизарной системы, регулирующий секрецию адреналостероидов.
Номенклатура, строение, классификация
Выделено большое количество отдельных форм Опухоли (в руководстве по патологоанатомической диагностике Опухоли под редакцией Н. А. Краевского и А. В. Смольянникова., 1976, упоминается около 500 различных форм Опухоли). В основу номенклатуры и классификации Опухоли положены гистогенетический и гистологический принципы, в связи с чем в названиях отражается их клеточная и тканевая принадлежность. Несмотря на значительный прогресс техники/ морфологический исследований, гисто и морфогенез некоторых Опухоли остаётся нераскрытым, что затрудняет их классификацию.
Названия большинства Опухоли состоят из двух частей: в первой части содержится указание на источник развития опухоли (клетки, ткань, орган), второй частью является суффикс «ома», означающий опухоль. Например, опухоль, развивающаяся из жировой ткани, называется липомой, из хрящевой ткани — хондромой, мышечной ткани — миомой и тому подобное
В наименовании Опухоли, помимо её гистогенетических особенностей, указывают на её связь с тем или иным органом (например, аденома щитовидной железы), или анатомической областью (например, липома бедра) и тому подобное В построении названий ряда Опухоли встречаются отклонения от указанного принципа; например, эпителиальная опухоль печени называется гепатомой, опухоль мозговых оболочек — менингиомой, опухоль вилочковой железы — тимомой и тому подобное Нередко в названии Опухоли подчёркивается её клеточный состав; например, опухоль из гистиоцитов называется гистиоцитомой, из клеток Лейдига — лейдигомой, из клеток Сертоли — сертолиомой.
Опухоли, возникающие из . элементов кроветворной системы, получили специальные названия — лимфомы, лейкозы и другие Структура Опухоли может напоминать ткани или органы и тогда говорят о гистиоидных или органоидных Опухоли В ряде случаев в Опухоли обнаруживают элементы эмбриональных тканей, что позволяет обозначать их как эмбриональные и тератоидные Опухоли, или тератомы. Вопрос о злокачественности таких Опухоли по морфологический данным решить иногда очень трудно. При наличии признаков злокачественности эпителиального и мезенхимального компонентов Опухоли употребляют термин «тератобластома».
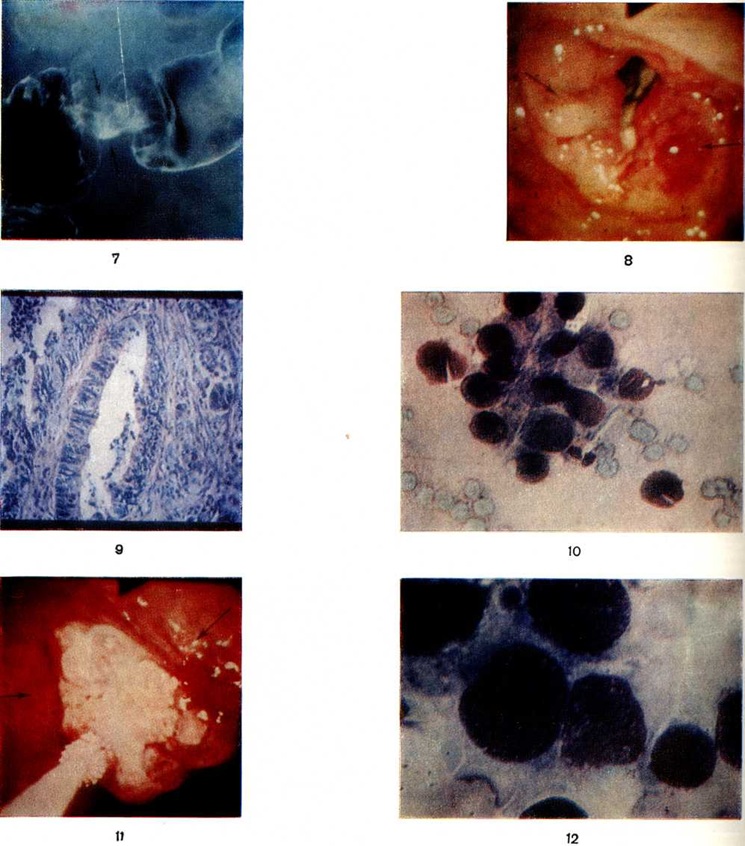
Исходя из представлений о возможных источниках развития, Опухоли распределяют по основным видам тканей: эпителиальные, соединительнотканные, мышечные и нейрогенные. В большинстве названий Опухоли подобная связь отражена, но есть и отклонения от этого правила. Например, злокачественные соединительнотканные Опухоли получили общее название саркома (смотри полный свод знаний) вследствие внешнего сходства их ткани с рыбьим мясом. Этот термин применяют также для обозначения злокачественных Опухоли мышечной и нервной тканей, однако сходство их с рыбьим мясом наблюдается не всегда. Термин «саркома», как правило, дополняется указанием на её тканевой источник, например Липосаркома, хондросаркома и другие Если тканевым источником саркомы является мышечная ткань, то в зависимости от её характера (гладкая или поперечнополосатая) говорят соответственно о лейомиосаркоме или рабдомиосаркоме (цветной рисунок 5—6). Терминологическое обозначение Опухоли, исходящих из эпителия, весьма разнообразно. Так, в наименованиях доброкачественных эпителиальных Опухоли учитывают не только исходный эпителий, но и особенности строения опухолевой ткани. Например, папилломами называют Опухоли с образованием сосочковых структур, развивающиеся из многослойного плоского или переходного эпителия, полипами и аденомами — Опухоли с образованием железистоподобных структур, исходящие из цилиндрического эпителия. Могут применяться и комбинированные названия, например, железистый полип. Злокачественные Опухоли, развивающиеся из эпителия, называются раком (смотри полный свод знаний).
Макроскопический вид Опухоли разнообразен. Они могут иметь форму округлого или овального узла, язвы, напоминать гриб или цветную капусту. Поверхность их бывает гладкой, бугристой, шероховатой и другие, По отношению к просвету полого органа рост Опухоли может быть эндо и экзофитным. Эндофитный рост направлен в глубь стенки, а экзофитный — в просвет полости, например, желудка, мочевого пузыря, глотки. В некоторых случаях. Опухоли как бы диффузно инфильтрируют весь орган. Макроскопически граница между Опухоли и окружающими тканями различима не всегда. В тех случаях, когда эта граница чётко различима, говорят о наличии капсулы Опухоли, хотя истинными капсулами Опухоли не обладают.
Основанием для установления диагноза Опухоли при гистологический её исследовании является наличие структурного атипизма формирующих её клеток и всего образования в целом. Структурных особенностей, свойственных только клеткам Опухоли, с помощью современных методов морфологический; исследования не обнаружено. Вместе с тем опухолевый атипизм реально существует, однако степень его выраженности колеблется в широких пределах. Эталоном определения степени атипизма для сравнения служат нормальные клетки и ткани, которые, как это свойственно и опухолевым клеткам, размножаются, растут, формируют те или иные структуры. Не случайно особенно часто Опухоли сравнивают с эмбриональными или регенерирующими тканями, а одним из основных признаков атипизма опухолевой ткани является отсутствие типовой завершённости циклов развития клеток и тканей, что проявляется в формировании, например, железистых образований без выводных протоков и тому подобное Клеточный атипизм ядер и цитоплазмы может выражаться в иных ядерно-цитоплазматических соотношениях, особенностях ядер и цитоплазмы, а также внеклеточных формирований. Микроскопическое исследование Опухоли показывает степень их отличия от исходных тканей, даёт представление о зрелых и незрелых Опухоли, .степени их дифференцировки, анаплазии и катаплазии. При сопоставлении структуры Опухоли с их биологический особенностями и клинические, картиной оказалось, что, как правило, менее зрелые и более катаплазированные Опухоли отличаются большей злокачественностью. Критерием злокачественности является также способность ) Опухоли к метастазированию. Метастазы обычно повторяют строение исходной опухоли, но могут и значительно отличаться от неё, например по степени дифференцировки. Поэтому установление первичного очага при морфологический исследовании метастазов не всегда возможно.
Структурный атипизм Опухоли распространяется на все её компоненты — и основной клеточный (паренхиму), и строму (соединительную ткань, включая межуточное вещество, сосуды и даже нервные элементы). Исходя из взаимоотношений стромы и паренхимы, например, в эпителиальных Опухоли, сложились представления о раке-мозговике (бедном стромой) и скирре с резким преобладанием соединительнотканной стромы над паренхимой. Строму эпителиальной опухоли (цветной рисунок 9) образуют элементы соединительной ткани, развитие и строение. Которой обусловлено Опухоли. Количество сосудов в Опухоли может быть, различным, а их структура атипичной с наличием тонкостенных, синусоидных, неправильной формы сосудов, Общая архитектоника сосудов в Опухоли резко отличается от их строения в нормальных тканях, что помогает клинические, диагностике, например, с помощью ангиографии. Нервные, элементы Опухоли могут образовывать вторичные атипичные структуры. Различные отклонения в формировании межуточного вещества отмечаются главным образом в саркомах, выражаются они в виде избыточного образования коллагена или остеоида, неправильного их распределения; скопления мукополисахаридов, образования очагов обызвествления и тому подобное В эпителиальных Опухоли можно наблюдать избыточную и атипичную секрецию слизи и даже гормонов.
Единой всеобъемлющей классификации Опухоли не существует. Многочисленные частные классификации нередко трудно сопоставимы между собой Вместе с тем для статистического учёта и анализа Опухоли необходимы такие классификации и номенклатура которые бы позволили получать сравнимые сводные данные по учреждениям, органам и географическим регионам. G целью устранения указанных трудностей ВОЗ приступила к изданию международных гистологический классификаций Опухоли, и в 1967 год была выпущена первая из них «Гистологические типы опухолей лёгких». К 1981 год опубликовано двадцать две гистологический классификации.
Существует целый ряд патологический процессов, пограничных с Опухоли, для обозначения которых вместо суффикса «нома» употребляют суффикс «оз», «например, фиброматоз, аденоматоз и тому подобное
Диагноз
Основу диагностики Опухоли составляет своевременное их распознавание на ранних стадиях заболевания грамм когда наиболее эффективно применение радикальных методов лечениям Поскольку онкологическое больные обращаются за помощью к врачам разных специальностей, то компетентным в вопросах своевременной диагностики Опухоли и предопухолевых . заболеваний должен быть каждый врач. Большое значение в раннем распознавании Опухоли имеет онкологическое настороженность врача, включающая не только знание симптомов онкологическое заболеваний, особенно в начальных стадиях, но и тщательное обследование больного, независимо от характера; предъявляемых им жалоб, а также коллегиальное решение вопросов в трудных для диагностики случаях. Особенно важна онкологическое настороженность врача при обследовании лиц старше 40 лет, когда риск заболевания злокачественными Опухоли повышается. К лиц. проявления опухолевых и предопухолевых заболеваний, часто бывают мало выражены, поэтому необходимо активное обследование больного. Использование клинические, методов (осмотра, пальпации, перкуссии, аускультации) даёт возможность последовательно выявить ряд .деталей, которые иногда имеют решающее значение для установления диагноза Опухоли.
Диагностику Опухоли разделяют на первичную, осуществляемую обычно в условиях поликлинического обследования или при проведении профилактических осмотров, и уточняющую, которую, как правило, проводят в стационаре. В диагностике Опухоли большое значение имеют клинические (анамнез и объективное исследование) и инструментальные (рентгенологический, эндоскопический, морфологический и радиоизотопный) методы исследования. При первичной диагностике Опухоли клинические, методы обследования позволяют заподозрить или диагностировать Опухоли и наметить рациональный план применения инструментальных методов исследования. Для распознавания ранних форм рака лёгкого используют крупнокадровую флюорографию органов грудной клетки (смотри полный свод знаний Флюорография), желудка и ободочной кишки фиброгастроскопию (смотри полный свод знаний Гастроскопия) и колопоскопию (смотри полный свод знаний) с прицельной биопсией (смотри полный свод знаний), рака шейки матки — цитологическое исследование (смотри полный свод знаний). Начальные формы Опухоли молочной железы в ряде случаев выявляются при осмотре и пальпации, а также с помощью рентгенологическое и морфологический методов исследования.
Уточняющая диагностика у больных с уже выявленной злокачественной Опухоли или с подозрением на неё направлена на оценку индивидуальных особенностей заболевания и состояния больного для выбора наиболее рационального вида лечения. При этом необходимо выявить местные и общие критерии заболевания. К местным критериям относят уточнённую локализацию первичной Опухоли, анатомические особенности её роста, гистологический, строение, степень., её дифференцировки и стадию заболевания; к общим — генетическую предрасположенность больного к тем или иным. Опухоли, его иммунологический статус, состояние обмена веществ и гормональный профиль. Местными критериями онкологическое заболевания в клинической медицине пользуются давно. Общие его критерии активно изучаются и приобрели практическое значение при раке молочной железы, ретинобластоме, пигментной ксеродерме, нейробластоме, феохромоцитоме, паратанглиоме, опухоли Вильмса и при других опухолях.
Наряду с оценкой местных и общих критериев в стационаре выясняют индивидуальные особенности заболевания, уточняют степень операционного риска. При этом учитывают сопутствующие заболевания, функциональный показатели и возраст больного. Для выявления индивидуальных особенностей заболевания используют различные диагностические методы. Самым распространённым является рентгенологическое исследование, позволяющее установить локализацию и границы Опухоли Оно включает бесконтрастные и контрастные методы исследования. Бесконтрастные методы рентгенологическое исследования (просвечивание, рентгенография и томография) используют главным образом для оценки состояния органов грудной и реже брюшной полости, конечностей, шеи. Многоосевое просвечивание с использованием функциональный проб позволяет составить план более сложного рентгенологическое обследования. Рентгеновские снимки выполняют при разной жёсткости рентгеновского излучения, что позволяет изучить структуру патологический теней, получить увеличенное изображение небольшого патологический очага и другие При рентгенографии некоторых органов используют естественный контраст—воздух, способствующий более чёткому выявлению границ и структуры патологический очага, например, в гортани, полых органах и тому подобное Большое практическое значение для установления предварительного диагноза имеет анализ флюорограмм лёгких и молочной железы. Томографию (послойное рентгенологическое исследование) часто используют для выявления Опухоли лёгких. Более сложные контрастные методы рентгенологическое исследования применяют по специальным показаниям, чаще для диагностики Опухоли органов желудочно-кишечные тракта. С этой целью используют жидкие контрастные вещества, например, бариевую взвесь и высококонцентрированные водные растворы органических соединений йода (для контрастирования сосудов, кровоснабжающих Опухоли или прилегающих к ней, и некоторых органов, например, щитовидной железы). Для контрастирования применяют также газовые среды, главным образом кислород, который вводят в средостение, забрюшинное пространство, желудок, кишечник и другие Нередко одновременно используют жидкие контрастные вещества и газовые среды, например, при так называемый двойном или тройном контрастировании (цветной рисунок 7).
Эндоскопические методы (смотри полный свод знаний Эндоскопия) позволяют обследовать с помощью специальных инструментов-эндоскопов полые органы (цветной рисунок 1, 4), брюшную и грудную полости, межтканевые пространства, произвести при этом биопсию или взять материал для цитологический исследования (цветной 10—12). Применение эндоскопических методов исследования позволяет диагностировать небольшие Опухоли, в том числе преинвазивный рак.
В каждом случае Опухоли или при подозрении на неё используют морфологический методы диагностики, чаще всего биопсию. Однако биопсию не производят при подозрении на меланому, так как травма может ускорить её рост. Биопсию остеогенных сарком производят только по абсолютным показаниям.
Радиоизотопные методы исследования основаны на способности многих Опухоли и их метастазов накапливать радиоактивные нуклиды и используются для определения локализации Опухоли, её границ, наличия метастазов, оценки результатов лечения, а также выявления функциональный сдвигов в органах и системах, вызванных Опухоли и её метастазами. С диагностической целью больному вводят обладающий коротким периодом полураспада радиоактивный нуклид, распределение которого в организме улавливается специальными счётчиками (смотри полный свод знаний Радиоизотопная диагностика).
Лабораторные методы диагностики злокачественных Опухоли менее информативны, то есть специальные лабораторный тесты для каждого вида Опухоли отсутствуют. Используют иммунологический пробы, с помощью которых выявляются эмбриональные антигены, характерные для некоторых Опухоли, например, альфа-фетопротеин — при первичном раке печени и тератобластоме яичка и яичников, карциноэмбриональный антиген — при раке кишечника, α2Н-фетопротеин — при лимфомах, Опухоли мозга и нейробластомах. Лабораторный исследования (клинические, биохимические, иммунологические) имеют большое значение для оценки общего состояния онкологическое больного, и их результаты часто служат косвенным подтверждением наличия Опухоли и изменений в организме, вызванных ею.
В тех случаях, когда комплекс методов уточняющей диагностики оказывается недостаточным, показано применение диагностической операции. Такие операции чаще применяют при подозрении на Опухоли органов брюшной полости.
Лечение
Лечение доброкачественных Опухоли в основном оперативное, хотя в ряде случаев применяют методы лучевой терапии, криодеструкцию и другие методы. Доброкачественные Опухоли должны подвергаться радикальному лечению, особенно в тех случаях, когда имеется риск их малигнизации. Лечение злокачественных Опухоли осуществляется различными методами в зависимости от характера роста и гистологический формы Опухоли, её локализации, клинические, стадии, возраста больного, наличия сопутствующих заболеваний и другие Лечение онкологическое больных может быть радикальным, при котором можно рассчитывать на полное излечение, паллиативным, обычно направленным на продление жизни больного, и симптоматическим. В связи с постоянным ростом числа больных, получающих радикальное лечение, приобретает большое значение организация их медицинский реабилитации, проведение противорецидивной и общеукрепляющей терапии. Основными методами лечения Опухоли являются оперативное лечение, лучевая терапия и лекарственное лечение с применением противоопухолевых средств, антибиотиков и гормональных препаратов. Интенсивно изучаются возможности иммунотерапии рака. Успехи современной клинические, онкологии в значительной мере связаны с разработкой и внедрением в широкую практику комбинированных и комплексных методов, лечения злокачественных Опухоли, в частности сочетания оперативного лечения и лучевой терапии, дополнения оперативного метода лечения назначением противоопухолевых средств, сочетания лучевого и лекарственного методов лечения. В связи с этим возрастает необходимость госпитализации большинства онкологическое больных в специализированные онкологическое учреждения, располагающие соответствующей технической базой и квалифицированными кадрами.
Оперативное лечение является основным при большинстве Опухоли Оно применяется самостоятельно или в комбинации с другими методами лечения при раке желудка, лёгкого, ободочной и прямой кишки, молочной железы, при различных формах сарком костей и мягких тканей и другие При оперативном вмешательстве по поводу злокачественной Опухоли важно уточнить степень распространения опухолевого процесса для решения вопроса о рациональном объёме операции и необходимости применения дополнительных методов лечения. Оперативное вмешательство может оказаться пробным (при далеко зашедшем процессе), радикальным или паллиативным. К паллиативным операциям по поводу Опухоли относят наложение обходных анастомозов при Опухоли, которые не могут быть удалены и грозят закрыть или уже закрыли просвет желудочно-кишечные тракта; гастроэнтеростомию в аналогичных случаях при раке привратника желудка, гастростомию при раке пищевода и другие
Радикальное оперативное вмешательство по поводу злокачественных Опухоли основано на принципе полного удаления Опухоли в пределах здоровых тканей. При значительном поражении злокачественной Опухоли какого-либо органа часто оказывается необходимым полное его удаление или обширная резекция. Применение так называемый экономных операций допускается лишь в ранних стадиях Опухоли и при использовании других эффективных методов лечения, в частности лучевой терапии. В ходе операций по поводу злокачественных Опухоли придерживаются принципа абластики, то есть такого проведения оперативного вмешательства, когда исключается возможность оставления в операционном поле опухолевых клеток. С этой целью разработаны типовые схемы операций по поводу Опухоли различных локализаций. В большинстве случаев считают необходимым не только удаление поражённого опухолью органа, но и иссечение регионарного лимфатических, аппарата, где могут уже быть метастазы или опухолевые клетки, способные в последующем оказаться источником метастазирования. Так, при тотальной или субтотальной резекции желудка по поводу рака иссекают единым блоком большой и малый сальники, желудочно-поджелудочную связку и клетчатку, в которых расположены регионарные лимфатических, узлы (смотри полный свод знаний Гастрэктомия). При раке матки производят её экстирпацию и удаление единым блоком обоих яичников вместе с маточными трубами и широкими связками матки, а при необходимости — и с параметральной клетчаткой (смотри полный свод знаний Экстирпация матки). При раке молочной железы её, как правило, удаляют вместе с большой и малой грудными мышцами, а также жировой клетчаткой и лимфатических, узлами подмышечной, подлопаточной, подключичной (а иногда и парастернальной) областей (смотри полный свод знаний Мастэктомия).
В ряде случаев считается оправданным производить так называемый комбинированные операции, когда вместе с поражённым органом производится частичная резекция соседних органов. Так, при раке желудка может быть произведена спленэктомия, резекция печени, поджелудочной железы, ободочной кишки или её брыжейки, при раке лёгкого — резекция грудной стенки и так далее Комбинированное оперативное вмешательство производят обычно в случаях прорастания или метастазирования опухоли в соседние органы и при отсутствии признаков отдалённого метастазирования, то есть в тех случаях, когда можно рассчитывать на радикальность операции. Некоторые хирурги являются сторонниками расширенных оперативных вмешательств, например, удаления селезёнки при раке желудка, что позволяет иссечь клетчатку с лимфатических, узлами, расположенными в области её ножки. К таким же операциям относится расширенная радикальная мастэктомия, когда типичная операция дополняется вскрытием грудной клетки и удалением клетчатки переднего средостения.
К специальным методам оперативного лечения злокачественных Опухоли относят электрохирургию (смотри полный свод знаний), криодеструкцию (смотри полный свод знаний Криохирургия) и разрушение опухоли лучами лазера (смотри полный свод знаний). Для электрохирургии применяют переменные токи высокой частоты, вызывающие локальный тепловой эффект, используемый для рассечения и коагуляции тканей. Этот метод довольно широко применяется с целью абластичного проведения оперативных вмешательств, например, резекции желудка, толстой кишки, иссечения опухолей кожи и другие. Криодеструкция осуществляется специальным аппаратом, при помощи которого к Опухоли подаётся жидкий азот. Этот метод получил распространение при лечении наружных форм рака, особенно кожи, и показан в тех случаях, когда оперативное вмешательство может привести к косметическим дефектам. Крио деструкцию применяют с паллиативной целью для восстановления проходимости при раке прямой кишки и пищевода, снятия болей, остановки кровотечения и другие
Результаты оперативного лечения Опухоли зависят от многих факторов, и прежде всего от стадии заболевания, локализации, степени зрелости и гистологический строения Опухоли Большое значение имеет наличие или отсутствие метастазов в регионарных лимфатических, узлах. Наиболее благоприятные результаты лечения получены при раке кожи (5-летняя выживаемость более 90% больных). При раке желудка и раке лёгкого 5-летняя выживаемость после радикальных операций составляет не более 30—35% .
Лучевая терапия заключается в использовании воздействия ионизирующего излучения на опухолевый очаг. Для лучевой терапии (смотри полный свод знаний) применяют различные виды электромагнитного или корпускулярного ионизирующего излучения: рентгеновское, гамма-, тормозное (мегавольтное) излучения, потоки электронов, нейтронов, протонов и другие
Терапевтический эффект при лучевой терапии злокачественных Опухоли обусловлен последовательным развитием в их ткани изменений физического, физико-химического, химического и биохимического характера, завершающихся летальным или сублетальным повреждением опухолевых клеток. В результате радиационных поломок ДНК и РНК, инактивации ряда ферментов, повреждения клеточных мембран возникают сложные нарушения в течении обменных процессов клетки, вследствие чего наступает её гибель в период интерфазы или во время других фаз митоза. Одновременно с развитием в Опухоли некротических и некробиотических процессов наблюдается регенерация соединительнотканных элементов, которая приводит к замещению деструктивных участков Опухоли рубцовой тканью.
Эффект повреждения опухолевых клеток зависит от величины поглощённой дозы излучения, фактора времени (в случаях фракционированного или непрерывного облучения), состояния оксигенации Опухоли, её репродуктивной способности и степени клеточной анаплазии, а также от фазы митотического цикла. Так, установлено, что клетки, находящиеся в фазе G1, G2 или М, характеризуются более высокой степенью радиочувствительности. В то же время клетки, пребывающие в фазе S, обладают устойчивостью к ионизирующему излучению.
Существующее различие в радиочувствительности (радиопоражаемости) Опухоли и нормальной ткани, получившее название радио терапевтического интервала (смотри полный свод знаний), обусловливает развитие после облучения более выраженных деструктивных изменений в Опухоли по сравнению с нормальными тканями. Этот феномен объясняется частично тем, что в нормальных тканях под влиянием регулирующих систем наступает более полная и быстрая репарация радиационных поломок клеточных структур. С целью расширения радиотерапевтического интервала используют различные средства, обладающие радиосенсибилизирующим действием (облучение Опухоли в условиях гипербарической оксигенации, гипертермии, применения электронакцепторных соединений) или вызывающие ингибирующий эффект в отношении восстановления лучевых повреждений опухолевых клеток. Представляют также интерес исследования по синхронизации деления опухолевых клеток и облучение их в радиочувствительные фазы клеточного цикла.
Лучевая терапия злокачественных Опухоли применяется как самостоятельный метод лечения или в комбинации с другими, например, оперативным лечением или назначением противоопухолевых средств. По статистическим данным, в СССР лучевая терапия применяется более чем у 70% онкологическое больных. В зависимости от цели лучевую терапию как самостоятельный метод лечения подразделяют на радикальную, паллиативную и симптоматическую. Радикальная лучевая терапия предусматривает облучение зоны расположения первичной Опухоли и её регионарных метастазов в лечебный дозах. Паллиативная лучевая терапия проводится с целью частичного разрушения Опухоли и стабилизации процесса. При этом очаговые дозы бывают ниже, чем при радикальном лечении. Симптоматическая лучевая терапия применяется при поздних стадиях развития опухолевого процесса и направлена на устранение отдельных симптомов, доминирующих в клинические, картине заболевания (боль, компрессионный синдром и другие). Достигаемый в результате симптоматической лучевой терапии эффект носит временный характер.
Разработаны различные способы облучения, которые в зависимости от расположения (ориентации) источника ионизирующего излучения по отношению к Опухоли называют наружным (дистанционным), аппликационным, внутриполостным и внутритканевым (внутриопухолевым). Дистанционное облучение осуществляется с помощью гамма-терапевтических установок, рентгенотерапевтических аппаратов, линейных или циклических ускорителей и является наиболее частым вариантом лучевой терапии. При глубоко расположенных Опухоли используют многопольное перекрёстное или подвижное облучение. Применение мегавольтного излучения (гамма-, тормозное излучение) позволяет резко снизить лучевую нагрузку на кожу в области входного поля и избежать её лучевых повреждений. Аппликационное облучение проводят с помощью аппликаторов, на поверхности которых размещаются радиоактивные препараты 60Со, 224Ra, 137Cs, 90Sr и другие Оно показано при относительно поверхностно расположенных Опухоли, например, кожи, нижней губы, глаза. Внутриполостное облучение используют при Опухоли полых органов, например, матки, прямой кишки и другие, и осуществляют путём введения в полости этих органов специальных эндостатов с радиоактивными нуклидами (60Со, 224Ra, 13Cs, 252Cf). Внутриполостное облучение часто сочетают с дистанционной лучевой терапией — так называемый сочетанное облучение. Внутритканевое или внутриопухолевое облучение осуществляют путём внедрения в ткань опухоли радиоактивных игл, найлоновых полых трубок с гранулами 60Со, 182Та, 192Ir, 252Cf, а также гранул 198Аи. Облучение Опухоли в ряде случаев может быть осуществлено путём инфильтрации её коллоидными растворами или путём эндолимфатического введения растворов радиофармацевтических препаратов. При некоторых Опухоли, например, щитовидной железы, используются их свойства избирательно накапливать радиоактивные соединения йода.
Лучевые методы лечения ,могут быть частью комбинированного или комплексного лечения онкологическое больных. Предоперационная лучевая терапия показана при Опухоли, наиболее часто рецидивирующих и метастазирующих, например, при меланоме, саркоме мягких тканей, раке верхней челюсти, языка, молочной железы, мочевого пузыря. Основная задача при этом сводится к снижению способности опухолевых клеток к имплантации в нормальных тканях и развитию метастазов или рецидивов Опухоли Послеоперационная лучевая терапия направлена на уничтожение опухолевых клеток как в первичной опухоли, так и в лимфатических, узлах в случае недостаточно радикального оперативного вмешательства.
Лучевую терапию Опухоли производят путём непрерывного облучения (при низкой мощности дозы) или с помощью подведения отдельных фракций (при высокой мощности дозы). В зависимости от размера Опухоли, её гистологический строения и радиочувствительности для полного разрушения необходимо подвести к Опухоли дозу 5000—7500 рад (50—75 Гр) при условии облучения пять раз в неделю в течение 5—8 недель. При этом большое значение имеет толерантность нормальных тканей, которая определяется многими факторами, и прежде всего состоянием больного, распространённостью опухолевого процесса, тяжестью осложнений и наличием сопутствующих заболеваний. Недостаточный учёт этих факторов может быть причиной возникновения лучевых повреждений (смотри полный свод знаний).
Применение мегавольтной лучевой терапии позволило улучшить результаты лечения многих Опухоли Пятилетняя выживаемость после лучевой терапии рака шейки матки (T1_2N0M0) наблюдается у 80—90% больных, рака гортани (T1N0M0) — у 80—85% , рака кожи (T1_2N0) — у 96—97%, лимфогранулематоза — у 60—70% больных в I — II стадии заболевания. Неудовлетворительными остаются результаты лечения рака пищевода, лёгкого. Пятилетняя выживаемость при этих локализациях опухолей при T2_3N1M0 не превышает 3—5%.
Лекарственное лечение, или химиотерапия, — применение лекарственных средств, оказывающих повреждающее действие на опухолевую ткань. В большинстве случаев химиотерапия является одним из компонентов комплексного лечения и используется на определённом этапе заболевания, дополняя и расширяя возможности оперативного лечения и лучевой терапии. При некоторых злокачественных Опухоли (чаще при гемобластозах) химиотерапия применяется как единственный метод лечения.
Чувствительность различных Опухоли к отдельным противоопухолевым средствам различна, и поэтому особое значение имеет правильный выбор метода лечения, особенно в связи с тем, что противоопухолевые средства (смотри, полный свод знаний) обладают определённой токсичностью, в той или иной степени повреждая нормальные органы и ткани организма. Лекарственные противоопухолевые средства гормонального типа (эстрогены) впервые с успехом были применены в 1941 год Ч. Хаггинсом и сотрудники для лечения рака предстательной железы. В 1942 год Гудмен, Гилмен и Филлипс (L. S. Goodman, A. Gilman, Phillips) обнаружили противоопухолевое действие азотистых аналогов иприта, или хлорэтиламинопроизводных, что послужило толчком к активному изучению препаратов этой группы с точки зрения их противоопухолевого действия. В СССР исследования по химиотерапии Опухоли были начаты в 1952 год Л. Ф. Ларионовым и сотрудники, изучавшими в основном препараты алкилирующего действия. Работы по созданию новых противоопухолевых средств и их апробации активно ведутся во многих странах мира.
Все средства, используемые для лекарственного лечения Опухоли, могут быть разделены на две группы — гормональные лекарственные средства и собственно противоопухолевые средства синтетического и природного происхождения. Гормональные лекарственные средства в основном используют для лечения Опухоли, в определённой степени сохранивших способность исходных тканей реагировать на гормоны, в норме регулирующие их рост, то есть при так называемый гормонозависимых Опухоли, например, раке предстательной железы, молочной железы, тела матки, щитовидной железы. Некоторые гормональные препараты, например, кортикостероиды, применяют также при лечении гемобластозов. Близки к гормональным средствам антиэстрогены — производные трифенилэтилена, одним из основных механизмов противоопухолевого действия которых является блокирование рецепторов стероидных гормонов.
Терапевтический эффект большинства противоопухолевых средств, обладающих цитостатическим действием, связан с подавлением ими обмена нуклеиновых кислот, прежде всего в опухолевых клетках. Одновременно они обычно оказывают влияние и на обмен нуклеиновых кислот в быстро размножающихся популяциях клеток костного мозга, желудочно-кишечного тракта и другие, с чем связано их побочное действие. Известно, что противоопухолевые средства могут непосредственно действовать на нуклеиновые кислоты, нарушая их способность нормально функционировать, а также могут взаимодействовать с ферментами, участвующими в биосинтезе и функции нуклеиновых кислот. Алкилирующие противоопухолевые средства непосредственно взаимодействуют с нуклеиновыми основаниями ДНК. Некоторые противоопухолевые антибиотики и алкалоиды блокируют ДНК-матрицу и затрудняют деятельность полимераз. Функция нуклеиновых кислот нарушается также в том случае, если в результате воздействия противоопухолевого средства природный компонент цепи ДНК или РНК заменяется модифицированным. Возможно включение (интеркаляция) препарата между нуклеиновыми основаниями в цепи ДНК или РНК, также препятствующее нормальным процессам репликации и транскрипции.
Действие многих противоопухолевых средств из группы антиметаболитов основано на взаимодействии с ферментами, участвующими в биосинтезе предшественников составных частей молекул ДНК или РНК, осуществляющими их катаболические превращения, а также синтез биополимеров из этих компонентов. Ингибитор может взаимодействовать с активным центром фермента, причём тип взаимодействия может быть различным.
Действие противоопухолевых лекарственных средств растительного происхождения связано с подавлением ими процессов митоза. Наибольшее значение в механизме действия подобных средств имеет взаимодействие с тубулином — белком микротрубочек, то есть структур, образующих веретено в процессе митотического деления. По-видимому, противоопухолевый эффект, проявляемый некоторыми алкалоидами — ингибиторами митоза, зависит также от подавления ими некоторых других биохимический процессов.
Ведётся интенсивный поиск противоопухолевых средств, способных избирательно разрушать вещества, в которых опухолевая клетка особенно нуждается. В этом отношении особенно интересны ферменты, разрушающие аминокислоты. Примером такого фермента, получившего практическое применение в качестве противоопухолевого средства, является L-аспарагиназа.
Многие закономерности действия противоопухолевых средств на рост злокачественных Опухоли, по данным Скиппера (Н. Е. Skipper) и сотрудники, объясняются особенностями кинетики их клоногенных клеток. Опухолевые клетки, так же как и клетки нормальных пролиферирующих тканей, проходят фазы митотического цикла, в разной степени чувствительные к воздействию различных противоопухолевых средств. Активно делящиеся клетки наиболее чувствительны к химиотерапевтическим воздействиям. Временно или постоянно покоящиеся клетки к ним практически нечувствительны. Изучение кинетики клеточных популяций позволило выяснить ряд закономерностей действия противоопухолевых средств. Все опухолевые заболевания, высокочувствительные к химиотерапевтическим воздействиям, например, лейкозы, лимфосаркома, ретикулосаркома, хорионэпителиома, относятся к числу быстрорастущих Опухоли, то есть опухолей, в которых большая часть клеток находится в состоянии активного роста. В этих Опухоли с большой фракцией роста в течение единицы времени значительное число опухолевых клеток вступает в фазу синтеза ДНК, и поэтому применение ингибиторов синтеза ДНК может оказывать значительный эффект. В противоположность этому медленно растущие Опухоли, например, дифференцированные формы рака лёгкого, желудка, толстой кишки, в которых фракция роста невелика, оказываются малочувствительными к веществам, влияющим на синтез ДНК. Нормальные ткани с большой фракцией роста, например, костный мозг, также высокочувствительны к ингибиторам ДНК. При этом в быстрорастущих Опухоли фракция роста больше, чем фракция роста стволовых клеток костного мозга, и при таких опухолевых заболеваниях проведение интенсивных прерывистых курсов химиотерапии позволяет получить выраженный клинические, эффект, давая в то же время возможность репарации повреждённого костного мозга. Для медленно растущих Опухоли перспективнее применение более длительных режимов с большими интервалами между повторными курсами лечения. Очевидно, что даже при высокочувствительных Опухоли результаты применения химиотерапии тем лучше, чем меньше общее количество опухолевых клеток в организме. Поэтому теоретически оправданы паллиативные операции в комбинации с химиотерапией при чувствительных к ней Опухоли Лучевая терапия радиочувствительных Опухоли также может уменьшить число опухолевых клеток в организме, повышая тем самым шансы на эффект химиотерапии.
Получила признание идея синхронизации клеток Опухоли обычно с помощью средств, действующих на клетку в фазе М митоза. Такие противоопухолевые средства, как винкристин, винбластин, колхамин, блокируя на определённый промежуток времени опухолевые клетки в фазе М митоза, способствуют тому, что после их применения большая часть опухолевых клеток синхронно вступает в следующие фазы клеточного цикла и, следовательно, назначение через определённый промежуток времени препаратов, действующих на клетки в фазах S или Gt митоза, оказывается более эффективным. Возможность синхронизации опухолевых клеток, так же как и целесообразность одновременного применения противоопухолевых средств, действующих на разные фазы клеточного цикла, является одним из обоснований комбинированной химиотерапии злокачественных Опухоли Другим её обоснованием является целесообразность использования препаратов с различным механизмом действия. При этом исходят из представления о том, что нарушения различных биохимический процессов в Опухоли уменьшают шансы на то, что уцелеют резистентные клоны опухолевых клеток. Рациональная комбинация препаратов с различной токсичностью позволяет суммировать противоопухолевое действие препарата без увеличения токсических проявлений. В этом отношении особенно перспективны для использования в комбинациях препараты, не угнетающие гемопоэз. Оправдавшая себя в лечении системных заболеваний кроветворной ткани комбинированная химиотерапия позволила сделать шаг вперёд и в лечении солидных Опухоли Использование комбинаций противоопухолевых средств позволило добиться выраженного клинические, эффекта при Опухоли, считавшихся устойчивыми к химиотерапевтическим воздействиям, таких, например, как тератобластома яичка. Однако одновременное применение различных противоопухолевых средств, как показали исследования Голдина (A. Goldin), может вести не только к усилению противоопухолевого эффекта, но и к его уменьшению. В связи с этим очень важно в предклинических исследованиях оценить эффективность планируемой для применения комбинации противоопухолевых средств.
Эффективность противоопухолевого средства в значительной мере зависит от оптимального режима его применения (доза, ритм введения). Для выбора оптимальных доз и интервалов между введением противоопухолевых средств важное значение имеет использование данных фармакокинетики. Вопрос о возможности применения противоопухолевых средств решается индивидуально. Это решение прежде всего определяется точным диагнозом, так как разные Опухоли проявляют различную чувствительность к противоопухолевым средствам, а некоторые из них резистентны ко всем существующим противоопухолевым лекарственным средствам. Следует учитывать распространённость процесса, общее состояние больного, наличие или отсутствие сопутствующих заболеваний, то есть должны быть взвешены показания и противопоказания к химиотерапии. Условно с учётом современных возможностей химиотерапии все опухолевые заболевания могут быть подразделены на четыре группы: Опухоли, при которых принципиально возможно излечение с помощью лекарственных методов лечения (хорионэпителиома матки, лимфома Беркитта, острый лейкоз у детей, лимфогранулематоз, семинома яичка); Опухоли, при которых химиотерапия даёт выраженный клинические, эффект (острый лейкоз у взрослых, хронические лейкозы, лимфосаркома, ретикулосаркома, миеломная болезнь, истинная полицитемия, опухоль Юинга и костная ретикулосаркома, рак молочной железы, предстательной железы, гортани, мелкоклеточный рак лёгкого, рак яичников, тела матки, тератобластомы яичка, опухоль Вильмса, нейробластома у детей, эмбриональная рабдомиосаркома, ангиогенные саркомы, рак кожи, рак полового члена, кортикостерома); Опухоли с невысокой чувствительностью к химиотерапевтическим воздействиям (раки желудочно-кишечные тракта, меланома, плоскоклеточный рак кожи головы и шеи, глиобластома, ретинобластома, рак мочевого пузыря, инсулома, рак влагалища, синовиальная саркома и лейомиосаркома, остеогенная саркома); Опухоли, практически нечувствительные к современным противоопухолевым средствам (например, дифференцированные формы рака лёгкого, рак шейки матки, фибросаркома).
Современная клинические, химиотерапия чаще всего строится на использовании повторных курсов комбинаций противоопухолевых средств для сохранения клинические, эффекта (поддержка ремиссии). При возникновении резистентности прибегают к смене терапевтических режимов с использованием средств, не обладающих перекрёстной устойчивостью. В ряде случаев оправдано введение высоких доз противоопухолевых средств.
Реабилитация онкологических больных
Реабилитация онкологических больных — многоэтапный процесс, позволяющий возвращать больных к полноценной жизни и труду. По возможности раннее начало лечения, его непрерывность, преемственность, комплексный характер, этапность и индивидуальный подход с целью восстановления утраченных функций и возвращения к активному общественно полезному труду являются основными принципами восстановительного лечения онкологическое больных. В определении объёма и целей реабилитации, как правило, принимают участие различные специалисты — врачи, психологи, социологи, юристы, работники органов социального обеспечения и другие Индивидуально для каждого больного разрабатывается программа восстановительного лечения, которая зависит от общего состояния больного, его возраста, состояния нервно-психической сферы, профессии, стадии развития, локализации и гистологический строения Опухоли, предполагаемых методов лечения, прогноза и другие Эта программа предусматривает максимальное восстановление трудоспособности, включая физическую, психологическую, социальную и профессиональную адаптацию. Врач предусматривает возможные причины утраты трудоспособности, которые могут появиться в результате болезни или проведённого лечения, чтобы суметь их уменьшить или предотвратить.
С целью профессиональной реабилитации осуществляются врачебно-трудовая экспертиза, профессиональное обучение больных, их рациональное трудоустройство, в том числе и на специализированных предприятиях. Началом профессиональной реабилитации является определение индивидуальных для каждого больного возможностей общественно полезной деятельности. Эта задача возложена на врачебно-консультационные комиссии (смотри полный свод знаний) и врачебно-трудовые экспертные комиссии (смотри полный свод знаний).
При трудоустройстве учитывают не только состояние здоровья, но и профессию, квалификацию, уровень общего и специального образования больного. Рациональное трудоустройство завершает реабилитацию онкологическое больного.
Профилактика
Современные данные по этиологии и патогенезу Опухоли позволяют наметить два пути их профилактики: предупреждение возникновения Опухоли, или так называемый первичную, гигиеническую, профилактику, и предупреждение их развития, или вторичную, клиническую, профилактику.
Основными принципами первичной гигиенические профилактики Опухоли являются: прекращение контакта с онкогенными веществами путём изъятия их из промышленного производства и замены безвредными веществами (или процессами), введение безотходной технологии или установление предельно допустимых выбросов (ПДВ) вредных соединений, гигиенические лимитирование (установление ПДК) тех онкогенных веществ, которые повсеместно распространены и не могут быть полностью изъяты из окружающей человека среды; создание гигиенические условий труда и соблюдение личной гигиены работающими. Первичная гигиенические профилактика Опухоли основывается на представлении об онкогенных агентах, в первую очередь онкогенных веществах (смотри полный свод знаний) и ионизирующем излучении (смотри полный свод знаний). Онкогенный эффект, как правило, зависит от дозы и времени контакта с онкогенным агентом. Чем меньше доза и период его воздействия, тем, как правило, реже и позже возникают Опухоли Устранение или снижение количества вредных воздействий и уменьшение контакта с ними способствуют профилактике возникновения Опухоли Улучшение условий труда, внедрение новой технологии, в частности герметизация опасных процессов производства, внедрение защитных мероприятий, соблюдение правил гигиенические обстановки на предприятиях и личной гигиены, способствуют устранению действия на организм онкогенных агентов.
В СССР проводится систематическая работа по профилактике профессиональных Опухоли мочевого пузыря (например, прекращено производство 2-нафтиламина и 3,3-дихлорбензидина, внедрён герметизированный метод получения бензидина, разработан метод синтеза аминотобиаскислоты, при котором не возникает онкогенный 2-нафтиламин, и другие). Ярким примером возможности первичной профилактики рака лёгких является борьба с курением, так как, прекращение курения приводит к снижению риска онкологическое заболевания.
Вещества, обладающие онкогенным действием, могут встретиться среди красителей и консервантов, употребляемых при изготовлении пищевых продуктов. Например, в некоторых капиталистических странах в качестве красителя для масла, маргарина, муки и другие использовали онкогенное вещество диметиламиноазобензол (Buttergelb, или butter-yellow). Онкогенные вещества, в частности полициклические ароматические углеводороды (ПАУ),могут попасть в пищевые продукты при их обработке, например, при копчении или сушке. Изменение технологии копчения, в частности применение так называемый коптильных жидкостей, может значительно снизить количество ПАУ в продуктах.
Необходимым звеном в цепи мероприятий по профилактике рака является охрана окружающей среды (смотри полный свод знаний). Онкогенные вещества, содержащиеся, например, в дыме отопительных систем, выбросах промышленных предприятий и двигателей внутреннего сгорания, загрязняют водоёмы и почву, могут переходить в растения, попадать в корма, пищевые продукты и организм человека. Снижение загрязнения атмосферного воздуха онкогенными веществами возможно путём подбора топлива, улучшения режима его сжигания, совершенствования методов и аппаратуры улавливания дымов и выхлопов. В СССР ведётся активная борьба за снижение загрязнения атмосферного воздуха путём реконструкции старых промышленных предприятий, введения безотходной технологии, рационального планирования городов и так далее
Клиническая профилактика Опухоли основывается на знании закономерностей развития предопухолевых заболеваний (смотри полный свод знаний). Своевременное их выявление и эффективное лечение являются основой клинические, профилактики Опухоли Важное значение имеют представления о фазности развития предопухолевых заболеваний, их обратимости в ранних периодах развития. Знание клинические, проявлений фаз диффузной или очаговой гиперплазии доброкачественной Опухоли в различных органах и тканях позволяет своевременно их выявить и с помощью рационального воздействия предупредить развитие злокачественной Опухоли На этом основана клинические, профилактика рака молочной железы, желудка, шейки матки и других органов. Так, при диффузных формах фиброаденоматоза молочной железы и мастопатий, соответствующих фазе диффузной гиперплазии в развитии предопухолевых состояний, рациональная гормональная терапия в ряде случаев позволяет ликвидировать патологический проявления и предупредить развитие Опухоли При узловых формах дисгормональных гиперплазий, соответствующих фазе развития очаговых пролифератов, с профилактической целью чаще всего применяют оперативное лечение.
Существенное значение для профилактики Опухоли имеют данные о факторах, способствующих развитию злокачественных Опухоли на фоне предопухолевых заболеваний. С целью их устранения, например, при пигментной ксеродерме, являющейся облигатным предраком, наряду с применением фотозащитных мазей производят иссечение изменённых участков кожи с пластикой дефектов.
В профилактике злокачественных Опухоли важным является своевременное выявление больных с предопухолевыми заболеваниями или состояниями, например, при профилактических осмотрах. В выявлении предопухолевых состояний и рациональной клинические, профилактике Опухоли большое значение имеют эндоскопические методы, особенно в сочетании с морфологический методами исследования. Они позволяют установить характер и степень предопухолевых изменений в верхних дыхательных путях, пищеводе, желудке, кишечнике и другие и провести лечение, например, удалить полипы желудка или кишечника с помощью эндоскопа.
Хорошие результаты даёт клинические, профилактика таких Опухоли, предопухолевые изменения при которых своевременно распознаются, например Опухоли кожи, губы, полости рта, гортани, шейки матки, молочной железы и другие
Опухоли у детей
Снижение детской смертности в экономически развитых странах, особенно связанное с резким уменьшением летальности от инфекционные болезней, привело к тому, что на передний план выступает смертность от злокачественных Опухоли По данным ВОЗ (1976), в 23 экономически развитых странах смертность детей от злокачественных Опухоли занимает второе место, уступая лишь смертности от несчастных случаев. Выборочные статистические исследования (ВОЗ, 1978), проведённые в некоторых странах Европы, показали, что ежегодно злокачественными Опухоли заболевают 15—16 детей на 100 ООО детского населения. В структуре заболеваемости злокачественными Опухоли у детей, по данным Блума (Н. Bloom, 1975), Джонса, Кемпбелла (P. Jones, P. Campbell, 1976), 31% занимают лейкозы, 18% — опухоли центральная нервная система, 11% — злокачественные лимфомы, 7% — опухоли почек (опухоль Вильмса), по 6% приходится на нейробластому, опухоли костей, глаз и орбиты, мягких тканей, 9% составляют прочие Опухоли, среди которых у детей крайне редко встречаются рак желудка, пищевода, молочной железы, матки, прямой кишки, кожи.
В возникновении Опухоли у детей, по данным большинства исследователей, имеют значение заболевания матери и различные неблагоприятные воздействия, перенесённые ею во время беременности, в том числе частые рентгенологическое исследования, проведённые во время беременности, увеличивают в дальнейшем риск возникновения Опухоли у ребёнка. Большое внимание уделяется изучению трансплацентарного онкогенеза — передаче плоду через плаценту онкогенных веществ. Опухоли у детей нередко сочетаются с различными пороками развития. Так, при опухоли Вильмса часто встречаются гемигипертрофия, аниридия, пороки развития мочеполовой системы; лимфомы сочетаются нередко с врождённой агаммаглобулинемией; опухоли костей — с экзостозами, энхондромами, несовершенным остеогенезом; лейкоз — с болезнью Дауна. Известны генетически обусловленные синдромы, которые предрасполагают к развитию Опухоли в детском возрасте. Возникновение Опухоли у детей также связывают с неравномерным ростом некоторых органов и тканей в определённые возрастные периоды, резко выраженной пролиферативной реакцией клеток и тканей на воздействие, например, такого фактора, как ионизирующее излучение.
В морфологический отношении Опухоли у детей являются главным образом саркомами и лишь приблизительно в 2% случаев — раками. Критерии злокачественности Опухоли у детей весьма относительны. Так, злокачественные Опухоли, например, опухоль Вильмса и нейробластома, длительное время ведут себя как доброкачественные (окружены капсулой, не прорастают в окружающие органы и ткани), а доброкачественные Опухоли, например, гемангиомы, нередко обладают местным инфильтрирующим ростом.
Клинически Опухоли у детей чаще обнаруживаются в возрасте от двух до пяти лет, однако при тщательном изучении анамнеза нередко оказывается, что они возникли гораздо раньше. Развитие Опухоли происходит на фоне процесса физиологический роста ребёнка, с чем связан ряд особенностей клинические, течения Опухоли у детей. У заболевшего ребёнка изменяется поведение, отмечается вялость, слабость, снижение аппетита, бледность кожи, субфебрильная температура, боли различной локализации. Некоторые Опухоли у детей протекают клинически как острые инфекционные болезни.
Распознавание Опухоли у детей затруднено, и, по данным ряда исследователей, свыше 75% больных поступает на стационарное лечение в поздних стадиях заболевания. Это объясняют, в частности, тем, что в детском возрасте реже встречаются Опухоли визуально наблюдаемых локализаций, имеется множество «масок», за которыми они скрываются, например, детские инфекции и ряд детских болезней. При диагностике Опухоли у детей обращают внимание на симптомы, которые нельзя объяснить другими заболеваниями, например, увеличение лимфатических, узлов при отсутствии регионарных поражений. Во всех случаях при осмотре ребёнка, в том числе и профилактическом, должна быть проведена пальпация живота с целью исключения Опухоли забрюшинного пространства. Урография, ангиография и другие методы рентгенологическое исследования позволяют распознать наиболее часто встречающиеся Опухоли у детей. Перспективна диагностика Опухоли у детей с помощью радиоизотопных методов исследования.
Лечение Опухоли у детей главным образом комплексное. Оперативное лечение проводят с учётом абластики и радикальности, а также максимального щажения тканей. Методы обезболивания и коррекции гомеостаза позволяют при необходимости производить расширенные операции, а способность к быстрой регенерации резецированных органов, например, печени, даёт возможность получать обнадёживающие результаты. Лучевую терапию в ряде случаев используют как самостоятельный метод лечения, например, при лимфогранулематозе, а также для комбинированного лечения, в предоперационном и послеоперационном периоде. Особенно часто лучевую терапию используют в послеоперационном периоде в сочетании с назначением противоопухолевых средств. Опухоли у детей, как правило, чувствительны к лечению противоопухолевыми средствами, из которых наиболее эффективны циклофосфан, винкристин и актиномицин D.
Результаты лечения злокачественных Опухоли у детей более благоприятны, чем у взрослых. Лечение опухоли Вильмса в I —II стадии приводит к выздоровлению свыше 80% детей, в III—IV стадиях — около 20%.
|
Блохин Н.Н.; Абелев Г.И.; Бурлакова Е.Б.; Васильев Ю.М.; Герасименко В.Н.; Дурнов Л.А.; Краевский Н.А.; Мерабишвили В.М.; Павлов А.С.; Переводчикова Н.И.; Петерсон Б.Е.; Трапезников Н.Н.; Фалилеев Г.В.; Чаклин А.В.; Шабад Л.М.; Шапот В.С. |

|
⇐ Перейти на главную страницу сайта |
⇑ Вернуться в начало страницы ⇑ |
Библиотека Ordo Deus ⇒ |
⇐ Оптохиазмальный арахноидит |
⇓ Полный свод знаний. Том первый А. ⇓ |
Органические психозы ⇒ |
|
Все статьи в полном изложении, Вы можете найти в большой медицинской энциклопедии — Главный редактор: академик АН СССР (РАН) и АМН СССР (РАМН) Б.В. Петровский. — Москва издательство «Советская энциклопедия» 1989г. |
|
Внимание! Вы находитесь в библиотеке «Ordo Deus». Все книги в электронном варианте, содержащиеся в библиотеке «Ordo Deus», принадлежат их законным владельцам (авторам, переводчикам, издательствам). Все книги и статьи взяты из открытых источников и размещаются здесь только для чтения. |
|
Вся информация на сайте Ordo Deus находится в свободном доступе. Ordo Deus не предоставляет информацию на платной основе. |
|
Все авторские права сохраняются за правообладателями. Если Вы являетесь автором данного документа и хотите дополнить его или изменить, уточнить реквизиты автора, опубликовать другие документы или возможно вы не желаете, чтобы какой-то из ваших материалов находился в библиотеке, пожалуйста, свяжитесь с нами по e-mail: |
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы не желаете закончить свой жизненный путь в виде омерзительной гниющей органической массы пожираемой копошащимися в ней могильными червями? Вы желаете вернувшись в молодость прожить ещё одну жизнь? Начать всё заново? Исправить совершённые ошибки? Осуществить несбывшиеся мечты? Перейдите по ссылке: «главная страница».
|
© Ordo Deus, 2010. При копировании ссылка на сайт http://www.ordodeus.ru обязательна. |