Гемофилия |
||
 |
 |
Оглавление
|
ГемофилияГемофилия (haemophilia; греческий haima кровь + philia склонность) — наследственное заболевание, связанное с нарушением первой фазы свёртывания крови, обусловленное дефицитом либо фактора VIII, либо фактора IX и проявляющееся частыми и длительными кровотечениями. Заболевание, вызванное дефицитом фактора VIII свёртывания крови (антигемофильного глобулина), называют гемофилией А, а заболевание, вызванное дефицитом фактора IX свёртывания крови (плазменного компонента тромбопластина), — гемофилией В или болезнью Кристмаса. Недостаточность фактора XI, которую некоторые авторы называют гемофилией С, фактора V (парагемофилия) и болезнь Виллебранда (ангиогемофилия) не являются истинной Гемофилия. Гемофилия известна с древних времён. Сведения о Гемофилия можно найти в Талмуде (2 в. нашей эры), в котором описаны смертельные кровотечения у мальчиков после ритуального обрезания. Гемофилия как самостоятельное заболевание описана Отто (J. С. Otto) в 1803 год. Родословную семьи больного Гемофилия впервые опубликовал Гей (J. Нау, 1813). Нассе (Ch. Nasse, 1820) сформулировал закон о наследственной передаче заболевания — от деда к внуку через внешне здоровую мать кондуктора. На увеличение времени свёртывания крови у больных с Гемофилия указал Райт (I. Wright, 1893). Термин «гемофилия» предложен Хопффом (F. Hopff, 1828) — учеником И. Шенлейна. СтатистикаЗаболевание редкое. На 50 000 жителей Дании, Швейцарии, Англии, Польши приходится один больной [Андреассен (М. Andreassen), 1943; Фонио (A. Fonio), 1954; Невяровский (S. Niewiarowski), 1961]. Частота рождаемости больных Гемофилия детей в каждой стране постоянна. По данным ВОЗ (1972), заболеваемость гемофилией А составляет в среднем ½—1 на 10 000 новорожденных мальчиков, заболеваемость гемофилией В — ½ — на 100 000. Полагают, что Гемофилия одинаково распространена среди различных рас и национальностей, однако имеются сведения, что среди африканцев и китайцев она обнаруживается редко. Утрата мутантных генов, обусловливающих Гемофилия, вследствие смерти больных компенсируется новыми мутациями, что поддерживает баланс генов Гемофилия, а следовательно, и число больных на определённом уровне. Этиология не известнаЗаболевание обусловлено, по-видимому, мутацией расположенного на Х-хромосоме гена, ответственного за биосинтез антигемофильного фактора. Частоту мутации генов, ответственной за развитие Гемофилия, суммарно определяют в 2—3,2 мутантных гена на 100 000 гамет [Стерн (С. Stern), 1965], или 1,3—4,2. × 10-5 для гемофилии А и 0,6—4,6 × 10-6 для гемофилии В. Генетика. Заболевание наследуется по сцепленному с полом рецессивному типу (смотри Наследование). Гены, регулирующие синтез факторов VIII и IX, локализуются в Х-хромосомах репродуктивных клеток. Предполагают, что формам гемофилии (А и В) соответствуют по крайней мере два различных локуса, расположенных на различных концах Х-хромосом. Однако имеются данные о возможном участии в регуляции синтеза фактора VIII и аутосомных локусов. Согласно современным представлениям, Гемофилия не только «дефицитное состояние». По аналогии с гемоглобинопатиями полагают, что причинами Гемофилия могут быть количественные и качественные изменения факторов свёртывания крови. О такой возможности свидетельствует выявление у больных мутантных фенотипов факторов VIII и IX. Генетику Гемофилия изучали на собаках [Бринкхаус (К. Brinkhous) и другие], у которых это заболевание идентично болезни человека. В соответствии с гипотезой Лайон (М. F. Lyon, 1962) женщина с одной поражённой Х-хромосомой (гетерозигота) является только кондуктором (носителем) патологический гена, но сама не заболевает, так как вторая непоражённая X-хромосома обеспечивает достаточный синтез соответствующего фактора (VIII или IX) свёртывания крови (чаще у кондукторов гемофилии В). |
У женщин-носителей патологический гена обнаруживают иногда незначительную кровоточивость и уменьшение содержания фактора VIII или IX. У женщин Гемофилия возникает только при наличии двух поражённых Х-хромосом: от больного Гемофилия отца и от матери носителя патологический гена. Описано 24 достоверных случая Гемофилия у женщин [Уинтроб (М. Wintrobe), 1967]. Следовательно, гипотеза Бауэра (К. Н. Bauer, 1922) об отсутствии потомства от больного Гемофилия мужчины и женщины-носителя патологический гена вследствие формирования так наз. летального гена не получила подтверждения.
С помощью клинико-генетических исследований различают наследственную, семейную и спонтанную (спорадическую) форму Гемофилия; последняя является следствием вновь возникших мутаций и составляет около 28% для гемофилии А и 9% для гемофилии В. При гемофилии обнаруживают также сопряжённое нарушение функции близлежащих в X хромосоме генов: глюкозо-6-фосфатдегидрогеназы, цветовой слепоты и другие.
Патогенез связан с нарушениями в первой фазе свёртывания крови вследствие недостатка продукции факторов VIII или IX, которые участвуют в образовании тромбопластина. При Гемофилия нарушен внутренний механизм образования тромбопластина, что проявляется удлинением времени свёртывания крови.
Фактор VIII является гликопротеидом, содержится в плазме, концентрация его у здоровых людей составляет 10 миллиграмм/литров. Структура фактора окончательно не установлена. Фактор VIII быстро разрушается при консервировании крови и нагревании. В процессе свёртывания фактор VIII потребляется и поэтому в сыворотке не содержится. При фракционировании плазмы по методу Кона фактор VIII выделяется с I фракцией. Предполагаемое место синтеза — печень, селезёнка, лейкоциты. Период полураспада 6—8 часов.
Фактор IX — белок плазмы и сыворотки — относится к группе β2-глобулинов, молекулярный вес около 80 000, стабилен при консервировании крови и нагревании. Из плазмы адсорбируется с помощью BaSO4, Al(ОН)3 и другие. В процессе свёртывания не потребляется и потому содержится в сыворотке. При фракционировании плазмы по методу Кона выделяется с фракциями III и IV. Период полураспада — 24 часа.
Патологическая анатомия
Изменения во внутренних органах, костно-суставной системе и так далее являются следствием массивных кровотечений и кровоизлияний (ишемия органов, изменения в костях, суставах, мышцах в результате образования осумкованных, оссифицированных гематом, кист и другие).
В межмышечных гематомах быстро (включается внешний механизм свёртывания) образуются сгустки. Такие гематомы плохо рассасываются и в дальнейшем подвергаются организации, а при повторных кровоизлияниях образуются псевдоопухоли, достигающие больших размеров. Повторные кровоизлияния в суставы являются причиной нарушения их функции.
Клиническая картина гемофилии А и гемофилии В характеризуется кровоточивостью. Кровотечения возникают периодически, как правило, через 1 — 2 часа после травмы, причём травма может быть ничтожной, а кровотечение обильным. У некоторых больных выявляют цикличность таких кровотечений, нередко зависимых и от времени года. Кровотечения могут иметь различную локализацию, чаще кровь изливается в мягкие ткани и суставы. Наружные кровотечения возникают после перерезки пуповины, при прорезывании или экстракции зубов, после травм и оперативных вмешательств. Внутренние кровотечения могут быть забрюшинные, в органы грудной и брюшной полости, центральной нервной системы.
Симптомы Гемофилия могут проявляться в момент рождения (кефалогематомы, кровотечения из пупочной ранки). С возрастом локализация кровотечения меняется. Если на первом году жизни у детей более часты кровотечения из слизистых оболочек носа и ротовой полости (вследствие прикуса языка, ранения щек, прорезывания молочных зубов), кровоизлияния под кожу и подкожную клетчатку, то у 2—3-летних детей обнаруживаются кровоизлияния в суставы и мягкие ткани. У детей 7—9 лет наряду с гемартрозами (смотри) нередко наблюдаются кровотечения из дёсен при смене зубов, гематурия (смотри) и кровоизлияния во внутренние органы. Периоды ремиссии у больных Гемофилия детей короче, чем у взрослых.
Тяжесть клинической, течения не зависит от формы Гемофилия (А или В), а определяется уровнем дефицитного фактора. Гемофилия протекает с периодами относительного благополучия, неодинаковыми у нескольких членов одной семьи.
Различают три формы клинической, течения Гемофилия: тяжелит, среднюю и лёгкую. Многие авторы выделяют четвертую форму — скрытую.
Для тяжёлой формы Гемофилия характерно раннее проявление кровоточивости и осложнений (остеоартрозы, контрактуры и так далее). Уровень дефицитного фактора у этих больных составляет до 3% от нормы. Для средней и лёгкой формы Гемофилия характерно более позднее появление кровоточивости. Содержание дефицитного фактора до 4—6% от нормы. Скрытую форму Гемофилия (уровень фактора VIII 6—10%) обычно выявляют случайно или при проведении семейных исследований у больных, у которых обнаруживают избыточную кровоточивость после травм, при экстракции зубов, тонзиллэктомии и других хирургических вмешательствах.
Для тяжёлой формы Гемофилия характерны кровоизлияния в суставы, причём обычно суставы поражаются в 2 — 3-летнем возрасте. Гемартроз сопровождается болевыми ощущениями, припуханием, защитной контрактурой мышц, местным и общим повышением температуры. Продолжающееся кровотечение вызывает перерастяжение тканей с последующим некрозом их и вскрытием гематомы. Нередки кровоизлияния в поясничные мышцы, в полость брюшины. Кишечные кровоизлияния протекают с развитием симптомов острого живота. Почечные кровотечения могут проявляться почечной коликой. При упорных кровотечениях из желудочно-кишечного тракта нередко развивается тяжёлая анемия. У больных Гемофилия возникают обильные кровотечения после удаления зубов (описаны случаи смертельных кровотечений). Чрезвычайно опасны для жизни больного кровоизлияния в головной мозг, мозжечок, мозговые оболочки, спинной мозг.
Осложнения
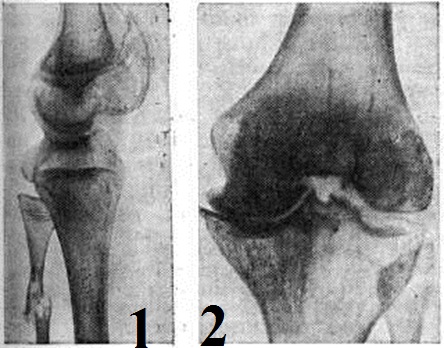
При Гемофилия лёгкой и средней тяжести осложнения возникают редко. Повторные кровоизлияния в сустав вызывают утолщение капсулы, узурирование хряща и остеопороз. При кровоизлияниях в коленный сустав, который поражается чаще, кровь скапливается в верхнем завороте, вызывая резкие боли и вторичную рефлекторную атрофию четырёхглавой мышцы. При отсутствии лечения развивается стойкая контрактура. Характерно образование кровяных кист в метафизе, реже в диафизе трубчатых костей. Иногда кисты локализуются в тазовых, пяточных костях. Наличие деструктивных процессов в костях нередко приводит к патологический переломам (рисунок 1). При обширных подкожных, внутримышечных, забрюшинных кровотечениях может наступить сдавление сосудов и нервов с последующим развитием некрозов, параличей и ишемической контрактуры.
Локализация значительных по размеру псевдоопухолей и геморрагических кист в брюшной полости может симулировать картину кишечной непроходимости. Забрюшинная локализация их может вести к сдавлению мочеточников. При локализации гематом по ходу магистральных сосудов и нервных стволов возможно сдавление их, что ведёт к развитию параличей, ишемии органов, гангрены конечностей и другие. Гематурия при Гемофилия нередко ведёт к образованию сгустков в мочевыводящих путях (особенно на фоне антифибринолитической терапии) с окклюзией мочевыводящих путей и нарушением функций почек.
Диагноз основывается на данных анамнеза, клин, картины и лабораторных исследований. Важное значение имеет тщательный сбор анамнеза (кровоточивость у мужчин в семье по линии матери, кровотечения с преимущественным поражением суставов, связанные с предшествующей травмой, их длительность и рецидивы). При осмотре больных обращают внимание на наличие кровоизлияний, гематом, изменения в суставах. При коагулологическом исследовании крови (смотри Коагулограмма) наличие у больного Гемофилия можно заподозрить на основании удлинения времени свёртывания крови (смотри) и времени рекальцификации плазмы, снижения потребления протромбина, что указывает на нарушение тромбопластинообразования. Характерны изменения тромбоэластограммы (смотри Тромбоэластография). Но окончательный диагноз Гемофилия ставят по результатам исследования парциального тромбопластинового времени и теста генерации тромбопластина по Биггс — Дугласу. При гемофилии А этот тест корригируется добавлением плазмы, адсорбированной BaSO4 или Al(ОН)3; при гемофилии В — добавлением сыворотки. Однако и он является недостаточно чувствительным. Наиболее точная диагностика основывается на количественном определении факторов VIII и IX.
Дифференциальный диагноз
Некоторые симптомы, характерные для Гемофилия, наблюдаются и при других заболеваниях. При ангиогемофилии (смотри) кровоточивость встречается у лиц обоего пола, чаще у женщин; выявляется чрезмерное удлинение времени кровотечения (смотри); кроме дефицита фактора VIII, в крови уменьшено содержание сосудистого фактора. При болезни Стюарта — Прауэр (смотри Геморрагические диатезы) кровоточивость (преимущественно у женщин молодого возраста) обусловлена дефицитом фактора X. Одновременно с нарушением первой фазы свёртывания крови выявляют нарушение парциального тромбопластинового времени и уменьшение протромбинового индекса (смотри Протромбиновое время).
При коллагенозах, туберкулёзе, злокачественных новообразованиях, воздействии ионизирующей радиации, медикаментозных и других интоксикациях в крови появляются циркулирующие антикоагулянты, чаще к фактору VIII, имитирующие клинику Гемофилия При дифференциации их с Гемофилия большое значение имеют данные анамнеза: отсутствие указаний на кровоточивость у других членов семьи, появление первых признаков кровоточивости в зрелом возрасте на фоне возникшего заболевания.
Важными для дифференциального диагноза тестами являются так называемый. Перекрёстные пробы: добавление к исследуемой крови или плазме 0,1 объёма крови или плазмы здорового человека нормализует время свёртывания крови у больных Гемофилия; при наличии в крови любого антикоагулянта проба отрицательна. Наоборот, добавление 0,1 объёма крови с антикоагулянтом к нормальной крови увеличивает время её свёртывания. Дополнительными исследованиями являются проба Биггс — Бидуэлл на антитела к фактору VIII, определение содержания свободного гепарина и титрование с протаминсульфатом. При иммуноэлектрофоретическом исследовании со специфическими антисыворотками к фактору VIII (IX) выявляется типичная дуга преципитации; количественное определение антикоагулянта проводят методом радиальной иммунодиффузии.
Рентгенодиагностика изменений костей и: суставов характеризуется признаками поражения опорно-двигательного аппарата вследствие кровоизлияний в полости суставов, в костномозговые пространства и в мягкие ткани.
Однократные кровоизлияния в суставы могут быстро и бесследно рассасываться. В острый период гемартроза рентгенологическое. Картина не специфична. На рентгенограммах иногда обнаруживается небольшое расширение суставной щели, обусловленное скоплением крови.
Повторные кровоизлияния в суставы приводят к гемофилическому остеоартрозу. Рентгенологическим признаком повторных кровоизлияний, начавшихся в детском возрасте, является изменение размеров и формы сустава.
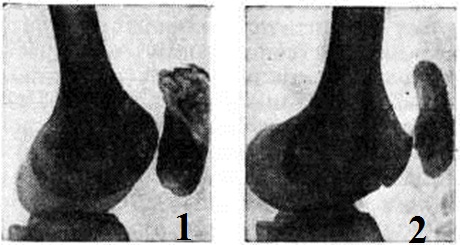
Рентгенологически различают четыре стадии гемофилического остеоартроза. На рентгенограммах в I стадии обнаруживают остеопороз суставных концов и утолщение суставной капсулы. II стадия характеризуется уменьшением объёма движений в суставе за счёт утолщения капсулы и образования внутри сустава организующихся гематом. В III стадии выявляют сужение суставной щели и изменение конфигурации суставных концов костей вследствие разрушения подхрящевых отделов эпифизов, костных разрастаний (рисунок 2), кистовидной перестройки эпифизов. В IV стадии суставная щель на рентгенограммах не видна или резко сужена. Подхрящевые отделы эпифизов значительно склерозированы.
Имеются некоторые особенности в рентгенологическое картине различных суставов с гемофилическим остеоартрозом: в коленном суставе часто разрушаются межмыщелковая ямка бедра, боковые поверхности мыщелков и надколенник; в локтевом — полулунная выемка локтевой кости; в плечевом — вдоль анатомической шейки образуются краевые узуры, иногда напоминающие сухую костоеду; в тазобедренном — развивается остеохондропатия.
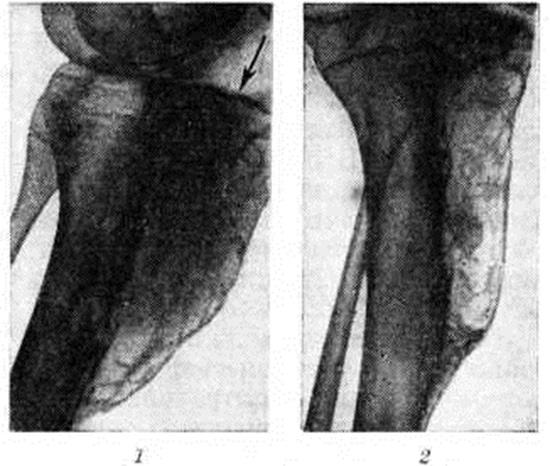
При внутрикостных кровоизлияниях крупные кистозные полости обнаруживаются чаще в эпифизах, но встречаются и в диафизах. Организующаяся гематома рентгенологически может дать картину так называемый гемофилической псевдоопухоли кости (рисунок 3). При формировании геморрагических кист в прилежащих отделах скелета обнаруживаются атрофические процессы с почти полным рассасыванием обширных участков кости. По краям кист выявляются экзостозные костные образования, свидетельствующие о репаративных процессах в костной ткани. В области дефекта кости можно видеть костные и известковые включения, которые при дефекте, расположенном в краевом отделе кости, могут дать картину «козырька» (рисунок 4), как при остеогенной саркоме. При Гемофилия могут наблюдаться также внутрикостные очаги склероза, субпериостальные оссифицированные гематомы, параоссальные оссификаты. Почти у половины больных выявляют оссифицирующие гематомы в мягких тканях. Гемофилия может быть причиной прогрессирующего оссифицирующего миозита.
Правильная интерпретация клинико-рентгенологическое симптоматики поражений опорно-двигательного аппарата при Гемофилия позволяет провести дифференциальную диагностику с артрозами и изменениями костей другой этиологии и определить показания к различным видам лечения (хирургическое, ортопедическое, лучевое).
Лечение
Основным методом лечения больных Гемофилия является возмещение недостающего фактора свёртывания крови. Лечение осложнений, вызванных кровотечениями и кровоизлияниями (гематомы, гемартрозы, контрактуры и так далее), иногда связано с хирургическими вмешательствами. Хирургические вмешательства как по поводу осложнений Гемофилия, так и в связи с заболеваниями, требующими хирургического лечения (аппендицит, непроходимость кишечника, язва желудка, травмы и так далее), имеют свои особенности.
Лечение Гемофилия важно начать с первых проявлений кровоточивости. Позднее начало лечения, как правило, приводит к тяжёлым осложнениям и, кроме того, удлиняет курс лечения.
Больным назначают цельную кровь, плазму (нативную замороженную, лиофилизированную) и антигемофильные препараты (концентраты факторов VIII и IX), а также ингибиторы фибринолиза. Свежую кровь или плазму необходимо вводить в больших объёмах (до доведения концентрации антигемофильного фактора в крови до требуемого уровня); это ограничивает их применение, так как наибольший объем переливаемой крови и плазмы за 24 часа не должен быть более 25 миллилитров на 1 килограмм веса тела, и повторные инфузии больших объёмов могут привести к перегрузке в системе циркуляции, образованию антител к фактору VIII (или IX), анафилактической и температурной реакции, гематурии, нарушению функции почек и так далее.
В антигемофильных препаратах концентрацию фактора VIII (или IX) выражают единицами активности. За 1 единиц активности фактора VIII (или IX) принято его количество, содержащееся в 1 миллилитров нормальной плазмы, полученной при смешивании плазмы от многих доноров.
Расчёт дозы антигемофильного препарата производят в единицах активности фактора VIII (или IX). При введении больному 1 единиц антигемофильного препарата на 1 килограмм веса тела уровень фактора VIII повышается на 1—2%. Дозу препарата рассчитывают по исходному уровню дефицитного фактора в крови больного, а также по периоду его полураспада. Период полураспада фактора VIII после однократного введения больному антигемофильного глобулина составляет 6—8 часов, после остановки кровотечения период полураспада удлиняется до 13—26 часов. [Бринкхаус (К. Brinkhous), 1970; Ю. И. Андреев с соавторами, 1972]. Период полураспада фактора IX колеблется от 12 до 24 часов [Биггс (R. Biggs), 1970; Султан (Y. Sultan), 1970]. Концентрированные препараты вводят внутривенно, струйно, с помощью шприца или системы для переливания крови.
Методы приготовления антигемофильных препаратов. При хранении консервированной крови и плазмы при плюсовой температуре фактор VIII инактивируется в течение нескольких часов. Поэтому свежую плазму, быстро отделённую от эритроцитов, замораживают при t° —25—40°. Эту плазму готовят следующим образом. Кровь от донора набирают в пластмассовый мешок (один из двух спаренных) с консервантом. Оба мешка (с пережатой соединительной трубкой между ними) центрифугируют 20 минут. Затем слой плазмы перемещают во второй мешок путём лёгкой внешней компрессии, герметизируют соединительную трубку, которую затем перерезают. Оставшиеся в первом мешке форменные элементы крови используют для переливания. Полученная плазма используется для переливания или является исходным сырьём для приготовления антигемофильных препаратов: криопреципитата и концентрата фактора VIII.
Антигемофильная плазма содержит в 1 миллилитров 0,2—1,6 единиц фактора VIII. Хранят её при t° —30°. Гемостатическая доза — 10 миллилитров на 1 килограмм веса тела. Суточная доза 20 миллилитров на 1 килограмм веса тела.
Криопреципитат впервые получен Пул (I. Pool, 1965), широко используется во всем мире. Представляет собой белковый препарат изогенной плазмы человека, в малом объёме содержит от 5 до 15 единиц/миллиметров фактора VIII. Хранится при t° — 30° или в высушенном виде, растворим при t° 35—37°. Применяется с учётом совместимости по АВ0-группам крови.
Известны также высокоочищенные лиофилизированные концентраты фактора VIII с активностью до 30—50 единиц/миллилитров.
Фактор IX адсорбируют на трикальцийфосфате, гидроокиси алюминия, сернокислом барии и других адсорбентах, на чем основаны методы выделения его. Выбор адсорбента и другие методические особенности приготовления указанных концентратов зависят от вида консерванта, стабилизирующего плазму. Одновременно с фактором IX адсорбируются факторы II, VII и X, вместе составляющие так наз. комплекс PPSB (по первым буквам названий факторов Р-протромбин (II), Р-проконвертин (VII), S — фактор Стюарта, В — антигемофильный фактор IX. Фактор IX устойчив при хранении плазмы при плюсовой температуре и выделение его не требует таких предосторожностей, как при работе с фактором VIII.
Протромбиновый комплекс РРSВ впервые получен Ж. Сулье, в СССР — Л. В. Минаковой. При получении комплекса PPSB важно правильно выбрать стабилизатор, предотвращающий свёртывание крови. Первоначальное предложение об использовании с этой целью ионообменных смол не получило применения в промышленных масштабах выделения комплекса PPSB.
Использование в качестве стабилизатора лимонной кислоты и её солей резко снижает возможность адсорбции комплекса PPSB из плазмы крови, поскольку цитраты растворяют PPSB с поверхности адсорбентов (например, гидроокиси алюминия). Кроме того, при большом содержании в полученных препаратах цитрата натрия у больных возникают боли.
Распространённым стабилизатором крови при получении комплекса PPSB является этилендиаминтетрауксуснокислый натрий (ЭДТА-Na), который имеет, однако, сравнительно высокую токсичность, ограничивающую непосредственное применение PPSB.
Метод выделения PPSB заключается в следующем: к плазме добавляют гель трикальцийфосфата (около 5 весовых %) и после перемешивания центрифугируют. Осадок трикальцийфосфата с адсорбированным на нем PPSB дважды обрабатывают 2 — 3% раствором цитрата натрия, отделяя осадок центрифугированием. Центрифугат объединяют и высушивают в замороженном состоянии (лиофилизация). Таким образом, достигают примерно 20-кратной концентрации фактора IX. Превращение протромбина в тромбин предотвращают добавлением гепарина и кофактора гепарина.
Возможно выделение PPSB из цитратной плазмы путём адсорбции его на диэтиламиноэтилцеллюлозе с последующим растворением цитратно-фосфатным буфером. Промышленного применения метод пока не имеет.
При промышленном получении препарат PPSB выделяют из фракции III Кона. Главная трудность состоит в сложности отделения PPSB от липопротеинов, составляющих основную массу фракции III.
Комплекс PPSB содержит в 1 миллилитров 10 — 60 единиц фактора IX. Вводят его после проверки на наличие тромбина. Срок хранения до 1 года. Хранят в лиофилизированном виде при t° 4°.
Ингибиторы фибринолиза вводятся с целью угнетения фибринолитических процессов. 5% раствор эпсилонаминокапроновой кислоты вводят внутривенно в дозе до 400 миллилитров в сутки или 4—8 грамм сухого порошка внутрь. Противопоказанием для назначения ингибиторов фибринолиза являются почечные кровотечения.
При обширных кровоизлияниях в мягкие ткани, полости, органы, в центральной нервной системы из гемостатических средств предпочтительнее введение концентратов фактора VIII (IX). Вводят гемостатические средства до полной остановки кровотечения.
Лечение осложнений гемофилии
Важна правильная тактика ведения больных Гемофилия с гемартрозами. При острых гемартрозах необходимо прежде всего снять болевой синдром назначением аналгезирующих средств; однако длительное применение ацетилсалициловой кислоты, бутадиона может усилить кровоточивость, а широкое назначение наркотиков — привести к развитию у больных Гемофилия наркомании.
Лечение гемартрозов необходимо начинать в первые часы или сутки от начала кровоизлияния, так как только при этом условии можно рассчитывать на восстановление функции сустава. На фоне трансфузии антигемофильных препаратов аспирируют из полости сустава кровь с последующим введением гидрокортизона и иммобилизацией сустава на 1—2 дня.
При хронический гемофилических остеоартрозах в фазе организации гематом в ряде случаев показана местная рентгенотерапия (рисунок 3 и 4). Кроме того, она способствует уплотнению сосудистой стенки.
При развитии стойких контрактур с целью их коррекции показаны: липкопластырное вытяжение, этапные гипсовые повязки. При сопутствующем синовите рекомендуется вводить гидрокортизон.
При отсутствии эффекта от консервативного лечения (запущенные формы синовита) производится синовэктомия. Операция иссечения синовиальной оболочки сустава способствует восстановлению функции сустава, прекращению повторных кровоизлияний. Операция резекции суставов и корригирующая остеотомия производятся при дегенеративных формах поражения.
Пунктирование глубоких межмышечных гематом эффекта не даёт вследствие быстрого свёртывания в них крови; длительно сохраняющаяся гематома является показанием для оперативного опорожнения её на фоне введения антигемофильных препаратов.
Обширные гемофилические псевдоопухоли, располагающиеся внутрибрюшинно или вблизи жизненно важных органов, удаляют с полным иссечением их капсулы; подлежат удалению и малые гематомы при появлении признаков их нагноения.
Для полной остановки наружного кровотечения вводят 20 единиц антигемофильного препарата на 1 килограмм веса тела, чтобы повысить уровень фактора VIII до 40% от нормы.
При желудочно-кишечного кровотечениях лечебный мероприятия должны быть направлены на остановку кровотечения и на ликвидацию анемии. Некупирующиеся при активной гемостатической терапии желудочно-кишечного кровотечения являются показанием для лапаротомии с последующей перевязкой кровоточащего сосуда или, если это невозможно, резекцией органа.
Особенности ведения больных гемофилией при хирургических вмешательствах. Всякое хирургическое вмешательство у больных Гемофилия связано с опасностью тяжёлого кровотечения, особенно в послеоперационном периоде.
При подготовке больных Гемофилия к хирургическим вмешательствам уровень фактора VIII (или IX) должен быть доведён до 50% от нормы и более.
При необходимости, в зависимости от характера предстоящих хирургических вмешательств, содержание дефицитного фактора повышают до 100% и поддерживают этот уровень в течение 3—5 дней. Перед операцией вводят 30—60 единиц антигемофильного препарата на 1 килограмм веса тела.
В послеоперационном периоде после больших операций более рационально одномоментно вводить всю суточную дозу препарата либо по 20 единиц на 1 килограмм веса через 8 часов.
В течение 10 дней после операции уровень дефицитного фактора необходимо повышать до 30—40% нормы, а затем, в зависимости от состояния, можно переводить больного на профилактические дозы препарата до полного выздоровления. Длительность гемостатической терапии при больших операциях, в том числе и костнопластических, составляет 7—14 дней. Одновременно применяют антифибринолитические средства (5% раствор эпсилон-аминокапроновой кислоты 300—500 миллилитров или 40% раствор ацепрамина 60—80 миллилитров в сутки); кортикостероидные гормоны (преднизолон внутривенно 20—30 миллиграмм, гидрокортизон 50—100 миллиграмм в сутки); сосудоукрепляющие средства (препараты кальция, аскорбиновая кислота, рутин и так далее).
При экстракции зубов за 30 минут до операции вводят 30—40 единиц на 1 килограмм веса тела антигемофильного препарата (чтобы повысить уровень дефицитного фактора до 30—40%); повторно препарат вводят через 12 — 24 часа в дозе 10—15 единиц (для поддержания дефицитного фактора не ниже 15—25%). Длительность антигемофильной терапии зависит от характера заживления раны.
Прогноз в отношении выздоровления неблагоприятный, однако система диспансеризации и профилактическое введение антигемофильных препаратов значительно улучшают течение заболевания. Заместительная терапия в момент кровотечений позволяет во многих случаях предупредить развитие осложнений, в том числе тяжёлых гемартрозов, и сохранить трудоспособность больных.
Профилактика
Существуют активная и пассивная формы профилактики. Активная — систематическое введение препаратов, содержащих факторы VIII и IX, 2 раза в месяц детям с 1 года до 14 лет. Пассивная — своевременное введение удвоенных доз препаратов, содержащих факторы VIII и IX, в момент начавшегося осложнения. Проводится всем больным. Как профилактику Гемофилия можно рассматривать медико-генетическое консультирование мужчины, больного Гемофилия, или женщины-кондуктора (доказанного, возможного или даже потенциального) перед вступлением в брак. Супруги должны быть предупреждены о возможности иметь больного ребёнка (смотри Медико-генетические консультации).
Большое значение имеет выявление женщин-кондукторов, что возможно путём количественного определения фактора VIII или IX. Содержание фактора VIII (IX), исследованного различными методами, в крови здоровых женщин оказывается нормальным а у женщин-кондукторов сниженным; биохимический методом выявляется низкий его уровень, а при иммунологический исследовании — высокий.
Имеет значение внутриутробное определение пола плода в семьях, где можно предполагать наличие женщин-кондукторов. Для этого предложен метод трансабдоминального амниоцентеза на 14—16-й недель беременности (смотри Амниоцентез). В извлечённой амниотической жидкости изучают плодные клетки для определения Х-хромосомы. Если плод мужского пола, ставят вопрос о прерывании беременности.
Больным Гемофилия регулярно вводят концентрированные антигемофильные препараты амбулаторно при гематологические стационаре. Для предупреждения кровотечений и их осложнений профилактическое лечение следует начинать с раннего детского возраста. Даже в тяжёлых случаях Гемофилия кровоточивость непостоянна; это позволяет проводить прерывистый курс лечения с учётом возраста больного и тяжести течения заболевания, что даёт ему возможность сохранить трудоспособность и вести нормальный образ жизни.
Профилактическое лечение приводит к повышению исходного уровня дефицитного фактора до значений, характерных для лёгкой формы Гемофилия, способствует более спокойному течению болезни, уменьшает частоту и интенсивность геморрагий. Профилактика осложнений Гемофилия состоит в предупреждении кровотечений и кровоизлияний в суставы и мышцы, что часто является причиной инвалидизации больных. Наиболее эффективно заместительное переливание крови при обострении заболевания или при учащении появления геморрагий.
Необходим охранительный режим, особенно для больных Гемофилия детей школьного возраста, так как в этот период особенно часто возникают кровоизлияния в суставы и мышцы.
Профилактические и лечебный мероприятия осуществляются гематологические отделениями республиканских, областных и городских многопрофильных больниц. В основу профилактики должно быть положено диспансерное обслуживание больных гемофилией.
В задачу диспансерного обслуживания больных Гемофилия входит: учёт и выявление больных Гемофилия, периодическое медицинский и лабораторное обследование их, проведение профилактики и лечение кровотечений и их осложнений. На больного Гемофилия, взятого на диспансерное обслуживание, заполняется специальная карта пробанда (история болезни), содержащая паспортные, краткие анамнестические и генетические сведения, а также данные, отражающие состояние больного: форма Гемофилия, тяжесть течения, групповая и резус-принадлежность крови, наличие в крови антител к клеткам крови, гемограммы, коагулограммы, рентгенограммы суставов и костей.
Каждому больному Гемофилия выдаётся «Книжка больного гемофилией», где указывается группа крови, её резус принадлежность, форма Гемофилия, её тяжесть, проводимые лечебно-профилактические мероприятия и рекомендации на случай обострения.
Помимо гематологические отделений, лечебно-профилактические работу проводят центры гемофилии на базе институтов гематологии и переливания крови, а также на базе республиканских, областных и городских больниц.
Центры гемофилии осуществляют лечебно-профилактические, консультативную, организационно-методическую и научно-исследовательскую работу. Научные исследования направлены на разработку и внедрение в практику лечебный учреждений новых эффективных методов и средств профилактики и лечения больных гемофилией.
В некоторых странах для больных Гемофилия детей созданы специальные школы, в которых, кроме общего образования, они получают навыки к посильной профессии.
Лечебный гимнастика и физиотерапия в комплексе со специфической терапией укрепляют мышечную и костно-суставную системы, предупреждают рецидивы геморрагий.
Смотри также Свёртывающая система крови.
|
Андреев Ю.Н.; Новикова Э.З.; Покровский П.И.; Токарев Ю.Н.; Фром А.А. |

|
⇐ Перейти на главную страницу сайта |
⇑ Вернуться в начало страницы ⇑ |
Библиотека Ordo Deus ⇒ |
⇐ Гемоторакс |
⇓ Полный свод знаний. Том первый А. ⇓ |
Гемофтальм ⇒ |
|
Все статьи в полном изложении, Вы можете найти в большой медицинской энциклопедии — Главный редактор: академик АН СССР (РАН) и АМН СССР (РАМН) Б.В. Петровский. — Москва издательство «Советская энциклопедия» 1989г. |
|
Внимание! Вы находитесь в библиотеке «Ordo Deus». Все книги в электронном варианте, содержащиеся в библиотеке «Ordo Deus», принадлежат их законным владельцам (авторам, переводчикам, издательствам). Все книги и статьи взяты из открытых источников и размещаются здесь только для чтения. |
|
Библиотека «Ordo Deus» не преследует никакой коммерческой выгоды. |
|
Все авторские права сохраняются за правообладателями. Если Вы являетесь автором данного документа и хотите дополнить его или изменить, уточнить реквизиты автора, опубликовать другие документы или возможно вы не желаете, чтобы какой-то из ваших материалов находился в библиотеке, пожалуйста, свяжитесь с нами по e-mail: |
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы не желаете закончить свой жизненный путь в виде омерзительной гниющей органической массы пожираемой копошащимися в ней могильными червями? Вы желаете вернувшись в молодость прожить ещё одну жизнь? Начать всё заново? Исправить совершённые ошибки? Осуществить несбывшиеся мечты? Перейдите по ссылке: «главная страница».
|
© Ordo Deus, 2010. При копировании ссылка на сайт http://www.ordodeus.ru обязательна. |