Лейшманиозы |
||
 |
 |
Оглавление
|
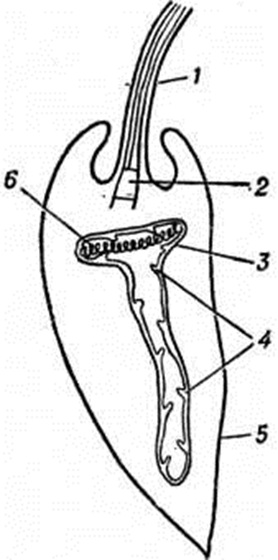
ЛейшманиозыЛейшманиозы (leishmanioses) — группа трансмиссивных протозойных болезней человека и животных, возбудители которых (лейшмании) передаются двукрылыми кровососущими насекомыми — москитами. Различают две формы Лейшманиозы человека: висцеральный Лейшманиозы (leishmaniosis visceralis), характеризующийся поражением лимфогистиоцитарной системы, ремиттирующей лихорадкой, кахексией, прогрессирующей анемией, лейкопенией, резким увеличением селезёнки, и кожный Лейшманиозы (leishmaniosis cutanea), при котором преимущественно поражается кожа (слизистые оболочки); процесс проявляется изъязвлением с последующим рубцеванием. Обе формы включают различные географические и клинико-эпидемиологические варианты. Оглавление Кожный лейшманиоз Старого Света Кожный лейшманиоз Нового Света ЭтиологияВозбудители Лейшманиозы — лейшмании — одноклеточные паразитические жгутиконосцы (тип Protozoa, надкласс Mastigophora, отряд Kinetoplastida, семейство Trypanosomatidae, род Leishmania). Впервые возбудителя Лейшманиозы (кожного) открыл в 1898 год П. Ф. Боровский в Ташкенте; он отнёс его к простейшим. У. Лейшман (1900) и частей Донован (1903) обнаружили в селезёнке больных кала-азаром паразитов, морфологически идентичных описанным П. Ф. Боровским. Р. Росс в 1903 год отнёс возбудителей Лейшманиозы к новому роду простейших — Leishmania. Возбудителя висцерального Лейшманиозы назвали Leishmania donovani Laveran а. Меsnil 1903; возбудителя кожного Лейшманиозы Старого Света L. tropica (Wright, 1903), Luhe (1906); возбудителя кожного Лейшманиозы Нового Света L. braziliensis Vianna, 1911. В. Лейшманиозы Якимов (1915) выделил два подвида возбудителей кожного Лейшманиозы в Средней Азии: L. tropica major и L. tropica minor. Возбудителей различных клинико-эпидемиологические вариантов Лейшманиозы рассматривают как самостоятельные виды (или подвиды). Различают несколько подвидов L. donovani — возбудителей висцерального Лейшманиозы. В Старом Свете выделяют L. donovani donovani Laveran a. Mesnil, 1903,— возбудитель индийского висцерального Лейшманиозы (калаазара); L. d. infantum Ch. Nicolle, 1908, L. d. sinensis Nicoli, 1953,—возбудители средиземноморско-среднеазиатского висцерального Лейшманиозы; L. d. archibaldi Castellani a. Chalmers, 1918,— возбудитель восточноафриканского висцерального Лейшманиозы В Новом Свете (в Центральной и Южной Америке) выделяют L. d. chagasi Cunha a. Chagas, 1937,— возбудитель висцерального Лейшманиозы, клинически и эпидемиологически близкого средиземноморско-среднеазиатскому. К возбудителям кожного Лейшманиозы в Старом Свете относят L. tropica Wright, 1903 (синонимы L. tropica minor),— возбудитель антропонозного поздноизъязвляющегося городского кожного Лейшманиозы (цветной рисунок 1 ,2), L. major Jakimov, 1915 (синонимы L. tropica major),— возбудитель зоонозного остронекротизирующегося сельского кожного Лейшманиозы Средней Азии н Ближнего Востока (цветной рисунок 1,6), а также L. aethiopica Bray, 1973,— возбудитель кожного Лейшманиозы и так называемый диффузного кожного Лейшманиозы в Эфиопии и Кении. Остаются неидентифицированными возбудители зоонозного кожного Лейшманиозы в Индии, Западной и Южной Африке. В Новом Свете возбудителей различных клинико-эпидемиологические вариантов кожного Лейшманиозы объединяют в два комплекса видов (или подвидов): комплекс теxicana — L. т. mexicana mexicana (Biagi, 1953) — возбудитель язвы чиклеров в Центральной Америке, L. т. атаzonensis Lainson a. Shaw, 1972,— возбудитель кожного Лейшманиозы в некоторых районах бассейна реки Амазонки; комплекс braziliensis — L. braziliensis braziliensis (Vianna, 1911) — возбудитель эспундии в лесных районах Бразилии, Боливии, Эквадора, Парагвая, L. Ь. guyanensis (Floch, 1954)— возбудитель «лесной фрамбезии», L. B. panamensis Lainson a. Shaw, 1972, — возбудитель панамского кожного Лейшманиозы и L. peruviana (Velez, 1913) — возбудитель уты — кожного Лейшманиозы в высокогорьях Перу и Боливии. |
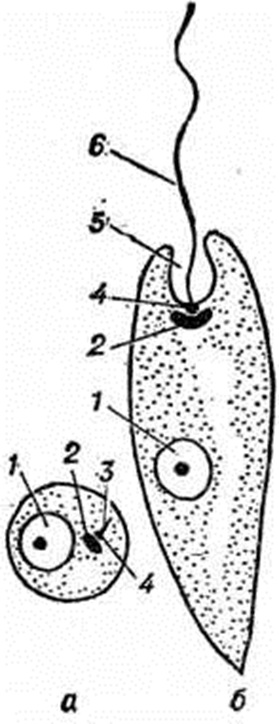
В своём жизненном цикле лейшмании проходят две стадии, изменяя при этом форму (рисунок 1). Безжгутиковая стадия (устар. лейшманиальная стадия) лейшманий — амастиготы (рисунок 1 ,а) паразитируют внутриклеточно в организме позвоночного хозяина (в макрофагах и других фагоцитирующих клетках кожи, слизистых оболочек, селезёнки, печени, костного мозга, лимфатических, узлов). Жгутиковая стадия (устар. лептомонадная стадия) лейшманий — промастиготы (рисунок 1, б) паразитируют в просвете кишечника беспозвоночного переносчика.
Амастиготы овоидной или округлой формы, размером 2—5,5 микрометров. В мазках, окрашенных по методу Романовского — Гимзы, видна серо-голубая цитоплазма, иногда вакуолизированная, крупное красно-фиолетовое ядро и темно-фиолетовый палочковидный кинетопласт; иногда обнаруживается тонкая розоватая нить — ризопласт — внутриклеточная рудиментарная часть жгута (цветной рисунок 1, а и б). При попадании амастигот в кишечник москита происходит их быстрая (в течение нескольких часов) трансформация: тело удлиняется, вырастает жгут.
Промастиготы (цветной рисунок 2) подвижны, имеют веретеновидную форму, длина тела 12—20 микрометров, ширина 1,5—3,5 микрометров, ядро расположено центрально, кинетопласт — на переднем конце тела, жгут начинается от базального тела, лежащего вблизи кинетопласта, длина его свободной части 16 — 20 микрометров. Размножаясь в кишечнике москита, промастиготы удлиняются и продвигаются вперёд; через 4—5 дней скапливаются в преджелудке, часто прикрепляясь концом жгута к его стенкам, а к 9 —10-му дню — в глотке. При повторном кровососании, через 5 —10 дней после заражающего кормления, москит способен передавать возбудителей.
Лейшмании размножаются продольным делением надвое. Деление начинается с появления нового базального тела и расщепления кинетопласта, затем митотически делится ядро, картина веретена наблюдается внутри ядра без нарушения его оболочки (эндомитоз). Цитокинез у промастигот начинается с переднего конца. Жгут остаётся у одной из дочерних клеток, у другой — вырастает из вновь образовавшегося базального тела.
Тело промастигот покрыто трёхслойной мембраной толщиной 10— 12 нанометров, под которой расположен слой из 100—200 микротрубочек, на поперечном срезе имеющих вид двухконтурных колец диаметром 20—25 нанометров. Число микротрубочек и размер амастигот у разных видов лейшманий достоверно различаются. Крупное ядро окружено двойной пористой мембраной, имеется 1—2 ядрышка. Двигательный аппарат включает ряд органелл: кинетопласт, состоящий из двух частей (одна содержит ДНК, другая имеет митохондриальную структуру), базальное тело (блефаропласт) с отходящим от него жгутом, который выходит из тела промастиготы через жгутиковый карман, образованный инвагинацией клеточной мембраны (рисунок 2). В стенках кармана видны пиноцитарные вакуоли.
 |
|  |
Рис. 1. | ||
Большинство видов лейшманий легко культивируются in vitro; в культурах клеток (при 15° 37°) размножаются в виде амастигот, на бесклеточных средах (при t ° 22—25°) — в виде промастигот, при t° 40° погибают через 15— 30 минут. Широко употребительна среда NNN, предложенная Ш. Николлем (агара 14 г., хлористого натрия 6 г., дистиллированная, воды 900 миллилитров, 10—25% дефибринированной крови кролика, pH среды 7,4—7,6). Модификации, позволяющие получить более обильный рост, заключаются в добавлении к кровяному агару жидкой фазы, содержащей растворы солей, 0,5—1% раствор глюкозы, дрожжевой экстракт, 0,5% раствор гидролизата лактальбумина, эмбриональные экстракты и другие
При культивировании in vitro вирулентность лейшманий постепенно снижается. Типовые штаммы поддерживаются пассажами на животных (главным образом золотистых хомяках) или сохраняются в замороженном состоянии при температуре жидкого азота — 196°. Первичное выделение штаммов лейшманий легко осуществляется внутрибрюшинным заражением хомяков материалом от больных людей или диких животных. В связи с отсутствием чётких морфологический признаков у лейшманий большинства видов (подвидов) для идентификации культур, выделенных от позвоночных животных и москитов, применяют биологический характеристику (характер процесса у экспериментальных животных). Кроме того, используют серологический методы (реакция гемагглютииации, тест Адлера в количественной модификации В. М. Сафьяновой, основанный на различиях в характере роста промастигот с гомологичными и гетерологичными сыворотками, серотипирование экзоантигенов промастигот в реакции иммунодиффузии в геле, иммуноферритиновый тест в сочетании с электронной микроскопией) и биохимический методы (определение плавучей плотности в хлористом цезии ядерной и кинетопластной ДНК, электрофоретическое типирование изоферментов и так далее). Вирулентность штаммов определяется на золотистых хомяках, белых мышах.
Висцеральный лейшманиоз
Висцеральный Лейшманиозы (синонимы: внутренний Лейшманиозы, детский Лейшманиозы, кала-азар и другие) представлен тремя основными видами: средиземноморско-среднеазиатским, индийским и восточноафриканским; имеются также географические варианты этих видов, различающиеся особенностями клиники и эпидемиологии.
История. Периодически повторяющиеся тяжёлые эпидемии висцерального Лейшманиозы (кала-азара) в Индии известны с начала 19 век. В 1900—1903 годы здесь был открыт возбудитель болезни, а в 1942 год экспериментально доказана передача возбудителей от человека человеку через москитов Phlebotomus argentipes (Ph. argentipes). Первый случай висцерального Лейшманиозы на территории России описан в 1909 год врачами Слукой и Царфлем (Е. Sluka, М. Zarfle) у больного из Ташкента, второй и третий случаи — в 1910 год Е. И. Марциновским и М. Н. Никифоровым.
В 1908 год Ш. Николль обнаружил лейшманий у собак в Тунисе, а в 1909 год Е. П. Джунковский и И. М. Лус — в Закавказье. В 1913 год экспедиция В. Лейшманиозы Якимова доказала широкое распространение висцерального Лейшманиозы среди людей и собак в Туркестанском крае. Обширные исследования в 20-х годы проводили Н. И. Ходукин и М. С. Софиев в Ташкенте, Лейшманиозы М. Исаев в Бухаре и Самарканде. Была установлена роль собак как источника инвазии и москитов — как переносчиков возбудителя в среднеазиатских городских очагах висцерального Лейшманиозы. В 1947 год Н. И. Латышев впервые установил природную очаговость висцерального Лейшманиозы, обнаружив на Ю. Таджикистана заражённых лейшманиями шакалов. Позднее лейшмании у шакалов были обнаружены в Туркмении и в Казахстане, у лисиц — в Грузии, Армении, а также в Бразилии и Франции. Мансон-Бар (Ph. Н. Manson-Bahr) в 1910 год предложил для лечения висцерального Лейшманиозы препараты сурьмы.
Географическое распространение.
Висцеральный Лейшманиозы распространён в тропическом, субтропическом и частично умеренном поясе всех континентов за исключением Австралии, от 47° с. ш. до 15° южной широты — в Восточном полушарии и от 19—22° северной широты до 29—30° южной широты — в Западном полушарии. По статистике ВОЗ, на 1968 год Лейшманиозы (без указания формы) зарегистрирован в 76 странах с многомиллионным населением. Однако уровень заболеваемости известен лишь для отдельных территорий, где проводились специальные обследования. Заболеваемость висцеральным Лейшманиозы подвержена колебаниям, которые определяются как природными, так и социальными факторами. Большие эпидемии наблюдались в 40—50-х годы 20 век в Индии (сотни тысяч больных), в Китае, Судане (десятки тысяч больных), Кении (тысячи случаев). До проведения борьбы в среднеазиатских очагах ежегодно регистрировались тысячи случаев висцерального Лейшманиозы. После широкого применения инсектицидов для борьбы с малярией повсеместно снизилась и заболеваемость Лейшманиозы, особенно теми формами висцерального Лейшманиозы, которые передаются эндофильными видами москитов (смотри полный свод знаний). После прекращения противомалярийных обработок с конца 60-х и в 70-х годы в некоторых странах наблюдается увеличение численности москитов и рост заболеваемости Лейшманиозы. В СССР ежегодно регистрируются отдельные случаи висцерального Лейшманиозы
Эпидемиология. Средиземноморско-среднеазиатский висцеральный лейшманиоз — зооноз; распространён в странах Южной Европы, Северной Африки, на Ближнем Востоке, в Средней Азии, в Северо-Западном Китае, встречается в южных республиках СССР.
По классификации Г. М. Маруашвили (1968) и А. Я. Лысенко (1972), имеется три типа очагов средиземноморско-среднеазиатского висцерального лейшманиоза, встречающегося и на территории СССР: природные очаги с циркуляцией возбудителя среди диких животных; сельские очаги, где основной источник возбудителей — собаки, но в циркуляции возбудителя участвуют и дикие животные, которые в определённых условиях становятся эпидемически значимым источником заражения людей; городские (синантропные) очаги, где основной источник возбудителей — собаки. В природных очагах возбудитель обнаружен у диких животных, например, у шакалов, лисиц, сусликов (Citellus citellus) и другие, в синантропных очагах — у крыс (Rattus rattus); в большинстве городских и сельских очагов основным источником и резервуаром возбудителей являются собаки, заражённость которых в очагах значительно превосходит заболеваемость людей. У собак болезнь, вызываемая L. d. infantum, протекает длительно с поражением не только внутренних органов, но и кожи, что резко повышает возможность заражения москитов. Переносчики — различные виды москитов: Ph. perniciosus, Ph. ariasi, Ph. major, Ph. perfiliewi, Ph. chinensis, Ph. kandelakii, Ph. caucasicus. У больных людей возбудитель в крови и в коже (первичный аффект) встречается очень редко, поэтому люди представляют меньшую эпидемический опасность как источники инфекции.
Заболеваемость этим типом Лейшманиозы обычно спорадическая. В эндемических очагах болеют главным образом дети, но нередко и взрослые — приезжие из неэндемичных районов. У детей болезнь, как правило, имеет характерную клинику, а у взрослых наряду с типичным течением наблюдается и бессимптомное. Наибольшее число заболеваний приходится на ноябрь—апрель месяцы.
В Западном полушарии также встречается висцеральный Лейшманиозы, клинически и эпидемиологически близкий средиземноморско-среднеазиатскому. Основной источник возбудителей — собаки, заражённость которых достигает 14%; возбудитель обнаружен также у лисиц, но их эпидемиологические роль, по-видимому, не-велика. Возбудитель — L. d. chagasi, переносчик — москит Lutzomyia longipalpis. Регистрируется главным образом в Бразилии и Венесуэле, а также в Мексике, Гватемале, Гондурасе, Сальвадоре, Колумбии, Суринаме, Боливии, Парагвае, Аргентине и другие. Встречается спорадически в сельской местности и в небольших городах, болеют преимущественно дети, значительных эпидемий не наблюдается.
Индийский висцеральный лейшманиоз (калаазар) распространён в восточных штатах Индии, в Бангладеш, Непале, спорадически встречается на востоке Китая и в странах Индокитайского полуострова. У животных возбудитель не обнаружен. Источником заражения москитов являются больные люди, у которых возбудитель часто находится в периферической крови, а в поздней стадии болезни (посткалаазарный кожный лейшманоид) — в коже. Возбудитель — L. d. donovani, переносчик Ph. argentipes. Болезнь распространена преимущественно в сельской местности, периодически даёт большие эпидемии, пик заболеваемости приходится на ноябрь—февраль. Болеют подростки и молодые люди (10—30 лет), основная заболеваемость приходится на возраст 20— 25 лет. Описаны казуистические случаи передачи кала-азара половым путём и внутриутробно.
Восточноафриканский висцеральный лейшманиоз распространён в зоне саванн в Судане, Сомали, Кении, Эфиопии, Уганде, Чаде, встречается также к югу и к западу от этих основных очагов. Источник возбудителей — различные дикие животные. Переносчики — Ph. orientalis, Ph. martini. Среди людей отмечается спорадическая заболеваемость и периодические вспышки, связанные как с природными (обильные дожди), так и с социальными факторами (миграция населения). В густонаселённых северо-восточный районах Кении и в Судане распространяется эпидемически (источник — больной человек), образуя семейные микро-очаги. Болеют люди всех возрастов. Для этого типа висцерального Лейшманиозы характерны первичные кожные поражения в виде узлов, нередко с изъязвлением, напоминающие кожный Лейшманиозы и содержащие возбудитель; на ранней стадии болезни лейшмании обнаруживаются также в крови.
Патогенез, патологическая анатомия. На коже через несколько дней или недель после укуса москита образуется первичный аффект — папула, в которой обнаруживаются лейшмании; при расчёсах может появиться поверхностная корочка.
Папула рассасывается, не оставляя следа (при восточноафриканском висцеральном Лейшманиозы кожная стадия выражена больше, часто наблюдается изъязвление). Болезнь может ограничиться кожными поражениями, однако чаще в дальнейшем наступает генерализация процесса и развивается системный эндотелиоз с размножением возбудителя в клетках гистофагоцитарной системы внутренних органов (селезёнки, печени, костного мозга, лимфатических, узлов, стенки кишечника, иногда надпочечников, почек, лёгких и так далее). При этом возникают нарушения, общие для всех форм висцерального Лейшманиозы. Наблюдается гиперплазия ретикулярной ткани, приводящая к увеличению паренхиматозных органов, особенно селезёнки (смотри полный свод знаний Спленомегалия). В результате усиленной пролиферации эндотелиальных клеток отмечается атрофия пульпы селезёнки, зародышевых центров в лимфатических, узлах; печёночные балки сдавливаются резко гипертрофированными купферовскими клетками. Выявляются скопления макрофагов с огромным количеством лейшманий. Характерна последовательность клеточной реакции: в ранние сроки болезни преобладает пролиферация гистиоцитов, на более поздних стадиях обнаруживается лимфоплазмоцитарная инфильтрация. Иногда возникают некротические очаги, инфаркты в селезёнке. При длительном процессе в печени развивается интерлобулярный фиброз (смотри полный свод знаний Печень). Развивается прогрессирующая гипохромная анемия и лейкопения. Патогенез их не вполне выяснен: возможно, он связан с нарушением обмена белков и железа, с повышенным разрушением клеток в результате гиперфункции селезёнки, с аутоиммунными механизмами. Резко нарушается белковый состав крови: гипоальбуминемия, гипергаммаглобулинемия, что приводит к развитию Отёков (смотри полный свод знаний Отёк). Все изменения обратимы и при успешном лечении исчезают.
Иммунитет. После самопроизвольного или медикаментозного излечения развивается стойкая невосприимчивость к Лейшманиозы; повторные заболевания не описаны. Уже на ранней стадии болезни обнаруживаются антитела. Высокие титры их определяются в течение всей активной фазы, а после успешного лечения титры снижаются и антитела исчезают через несколько месяцев. Накапливающиеся иммуноглобулины, сначала 1 IgM (19 S), затем IgG (7S), составляют до 50% общего белка. Гипериммуноглобулинемия и титры специфических антител при висцеральном Лейшманиозы не коррелируют. Лишь небольшая часть иммуноглобулинов образуется в ответ на паразитарные антигены и значительно большая — на аутоантигены. По-видимому, иммунопатологические механизмы играют при висцеральном Лейшманиозы значительную роль, в частности в патогенезе анемии и нейтропении. Кожная проба с лейшманином становится положительной через 6—8 недель после излечения при восточноафриканском висцеральном Лейшманиозы и ещё позднее при других вариантах. В эндемичных очагах Судана большое число взрослых людей положительно реагирует на введение лейшманина (от 35 до 85%), что, повидимому и объясняется не только тем, что они перенесли заболевание в клинические, или стёртой форме, но и сенсибилизацией непатогенными штаммами лейшманий от грызунов и рептилий.
Клиническая картина. Начальный признак болезни — первичный аффект (смотри полный свод знаний Аффект первичный). Общие явления развиваются после инкубационного периода продолжительностью от 10—21 дня до 10— 12 месяцев, чаще 3—6 месяцев; известен случай Лейшманиозы с инкубацией до 9 лет.
Начало чаще постепенное, в продромальном периоде нарастает бледность покровов, снижается аппетит, начинает увеличиваться селезёнка. Внезапное начало с резким подъёмом температуры более характерно для детей младшего возраста. Нередко началу явных клинические, проявлений предшествует какое-либо острое инфекционные заболевание. Описаны наблюдения, в которых провоцирующим фактором служила беременность.
 |
|  |
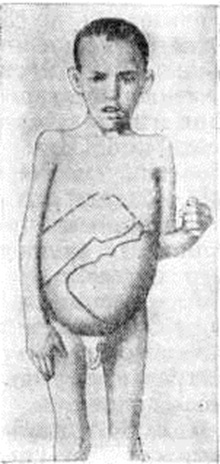
Рис. 3. | ||
Одним из основных симптомов является волнообразная неправильного типа лихорадка (смотри полный свод знаний), иногда с 2—3 пиками в течение суток. Волны подъёма температуры (субфебрильной или очень высокой) сменяются периодами ремиссии от нескольких дней до 1—2 месяцев Прогрессивно увеличивается селезёнка, особенно резко на 3—6-м месяцев болезни, несколько меньше — печень (рисунок 3) в разной степени — лимфатических, узлы как периферические, так и висцеральные (бронхиальные, мезентериальные и другие). Величина селезёнки зависит, как правило, от давности заболевания: за 9 —10 месяцев она может занять значительный объем брюшной полости. Селезёнка плотная, но эластичная, с гладкой поверхностью, ограниченно подвижная, периспленит не развивается. Увеличенные лимфатических, узлы плотноваты, всегда подвижны, безболезненны. В период разгара болезни кожа у больных бледная, восковидная, иногда с землистым оттенком, а при индийском висцеральном Лейшманиозы— очень тёмная (в связи с гиперфункцией надпочечников). Больные теряют в весе, постепенно развивается кахексия (смотри полный свод знаний). Нарастают изменения в крови: анемия (смотри полный свод знаний), лейкопения (смотри полный свод знаний) с тенденцией к агранулоцитозу (смотри полный свод знаний), тромбоцитопения (смотри полный свод знаний). Число эритроцитов может снизиться до 1—2 миллионов в 1 микролитров, лейкоцитов — до 1—2 тысяч в 1 микролитров. Наблюдается абсолютная и относительная нейтропения, абсолютное число лимфоцитов и моноцитов также снижается, эозинофилы, как правило, отсутствуют. У детей до 1 года в начале болезни может наблюдаться лимфоцитарный лейкоцитоз, резко уменьшено число тромбоцитов, РОЭ ускорена, у тяжелобольных она может достигать 90 миллиметров в часов. В костном мозге явления торможения эозино и мегакариоцитопоэза. Появление эозинофилов в пунктате костного мозга имеет благоприятное прогностическое значение. Со стороны сердечно-сосудистой системы — приглушенные тоны сердца, анемические шумы, тахикардия, пониженное артериальное давление, электрокардиографически выявляются диффузные изменения мышцы сердца. В поздней (кахектической) стадии болезни появляются Отёки, нередко развивается геморрагический синдром — петехии, кровотечения из носа и дёсен.
Различают острое и хронический течение болезни. Острое течение чаще наблюдается у маленьких детей; характерны высокая температура (39—40 °), тяжёлая интоксикация, быстро прогрессирующее ухудшение общего состояния и состава крови. Продолжительность болезни 3—6, редко 8—12 месяцев. При хронический течении, которое наблюдается у старших детей и взрослых, температура обычно держится в пределах 37,5—38° , изредка повышаясь до 39—39,5° . Наблюдается ремиссия лихорадки продолжительностью несколько недель или месяцев. Ухудшение общего состояния и показателей крови происходит медленно. При отсутствии лечения болезнь может продолжаться до 1½—3 лет. У взрослых наряду с типичным проявлением болезни описаны случаи безлихорадочного течения её с умеренным увеличением селезёнки и печени или только лимфатических, узлов и миндалин. По всей вероятности, стёртые формы болезни встречаются чаще, чем это считалось ранее.
Осложнения особенно часты в поздней стадии болезни и при выраженной лейкопении. Они возникают в результате присоединения вторичной бактериальной инфекции и имеют характер воспалительно-гнойных и некротических процессов — пиодермия (смотри полный свод знаний), бронхопневмония (смотри полный свод знаний Пневмония), катаральная и фолликулярная ангина (смотри полный свод знаний), может быть также флегмона миндалины и некротическая ангина, отит (смотри полный свод знаний), изредка синдром агранулоцитарной ангины, а также энтерит и энтероколит (смотри полный свод знаний Энтерит, энтероколит, нефропатия).
Диагноз основывается на характерной клинические, картине и эпидемиологические анамнезе. Решающее значение имеет обнаружение возбудителя; в селезёнке лейшмании выявляют в 100% случаев. При пункции лимфатических узлов находят лейшмании у 40—75% больных. Наиболее предпочтительно исследование костного мозга, дающее положительные результаты в 95 — 100% случаев. В мазках костного мозга, фиксированных спиртом и окрашенных по методу Романовского—Гимзы, лейшмании (амастиготы) обнаруживаются в макрофагах и вне клеток (цветной рисунок 3), иногда, особенно на ранней стадии болезни, в очень небольшом количестве. В редких случаях лейшмании можно обнаружить в крови (при индийском висцеральном Лейшманиозы — часто). Применяют и серологические методы диагностики, наиболее часто — реакцию связывания комплемента (смотри полный свод знаний) как с гомологичным, так и с гетерологичным антигеном (палочка Кедровского либо BCG) и реакцию иммунофлюоресценции (РИФ) с антигеном из промастигот или амастигот L. donovani. Эти тесты выявляют антитела уже на ранней стадии болезни (в течение первого месяца), когда обнаружение паразита не всегда возможно. Реакцию иммунофлюоресценции применяют и для выявления Лейшманиозы у собак; диагностическим является титр 1 : 100 у людей и 1 : 320 — у собак. Для диагноза имеют значение повторные исследования крови и костного мозга.
Дифференциальный диагноз. На ранней стадии болезни её дифференцируют с бронхопневмонией, брюшным тифом (смотри полный свод знаний), паратифами (смотри полный свод знаний), малярией (смотри полный свод знаний), бруцеллезом (смотри полный свод знаний), сепсисом (смотри полный свод знаний).
Обычно к 3—4-й недель выявляются характерные для висцерального Лейшманиозы увеличение селезёнки, изменения крови, серологический тесты, подтверждаемые результатами исследования костного мозга. Спленомегалию при системных заболеваниях крови, ретикулезах, гепатолиенальном синдроме дифференцируют со спленомегалией при Лейшманиозы на основании результатов стернального пунктата, данных Реакцию иммунофлюоресценции. В странах Латинской Америки висцеральный Лейшманиозы дифференцируют с помощью серологический методов также с глубокими микозами, например, с гистоплазмозом (смотри полный свод знаний). В неэндемичных районах следует помнить о возможности завоза болезни и в неясных случаях изучать эпидемиологические анамнез.
Лечение. Основное специфическое средство лечения — органические соединения пятивалентной сурьмы: отечественный препарат солюсурьмин (натриевая соль комплексного соединения сурьмы и глюконовой кислоты) — аналог солюстибозана (ФРГ), глюкантим, пентостам, уреастибаминут Препараты вводят внутривенно в виде 10—20% раствора ежедневно, детям суточную дозу в один приём, взрослым по г/2 суточной дозы утром и вечером. На курс лечения при дозе 0,1—0,15 грамм на 1 килограмм веса больного требуется 10—12 инъекций. В 1-й и 2-й день лечения вводят соответственно 1/3 и 2/3 полной лечебный дозы. Сильно ослабленным детям при тяжёлом течении болезни и осложнениях лечение начинают с дозы 0,01—0,02 грамм на 1 килограмм веса тела, ежедневно увеличивая её на 0,01 грамм (0,02 г) на 1 килограмм, доводят до 0,06—0,1 грамм на 1 килограмм на 6—10-й день лечения. После улучшения состояния больного дозу повышают до 0,12—0,15 грамм на 1 килограмм. Детям до 5 лет 10% раствор вводят под кожу, старшим детям и взрослым — 20% раствор внутривенно. Длительность курса лечения зависит от эффективности и, как правило, составляет 10—20 дней.
Эффективность лечения контролируют повторными исследованиями крови. Снижение числа нейтрофилов и ухудшение общего состояния указывают на необходимость повторного курса. Редко требуется третий курс. При недостаточном лечении рецидивы могут быть в течение ½—1 года, поэтому больные должны находиться под диспансерным наблюдением 12 месяцев Сокращение селезёнки и печени происходит постепенно в течение 2—4 месяцев Большое значение имеет лечение осложнений и сопутствующих заболеваний антибиотиками, сульфаниламидами, а также патогенетическая и симптоматическая терапия (витамины, антианемические препараты, гемотрансфузии, сердечные средства, хлористый кальций). Общеукрепляющие средства и полноценное питание необходимы в период лечения и до полного выздоровления. Критерии выздоровления: значительное нарастание веса, хорошее самочувствие, нормализация цвета кожи и слизистых оболочек, сокращение до нормы размеров селезёнки и печени, нормализация показателей крови. Для лечения висцерального Лейшманиозы, особенно в случае устойчивости к препаратам сурьмы, применяют также ароматические диамидины: пентамидин-изотионат (ломидин), стильбамидин и другие. Однако эти препараты обладают значительной токсичностью, а после лечения ими часты рецидивы.
Прогноз. Заболевание висцеральным Лейшманиозы с выраженной клиникой без специфического лечения обычно заканчивается смертью больного. При своевременном лечении, как правило, наступает полное выздоровление.
Профилактика включает меры, направленные на обезвреживание источника возбудителей, на уничтожение переносчика и на защиту людей от заражения. Мероприятия и тактика их применения зависят от эпидемиологические особенностей очагов.
Раннее выявление и лечение больных в очагах антропонозного типа имеет важное эпидемиологические значение. В эндемичных районах среди лиц, обращающихся в лечебный учреждения, больных выявляют активно и при профилактических осмотрах (во время подворных обходов). В неэндемичных районах обследование проводят особенно тщательно в педиатрических и гематологические учреждениях.
В очагах, где основным источником возбудителей являются собаки, проводят отлов бродячих собак, учёт и систематический ветеринарный осмотр домашних и дворовых собак, уничтожение или лечение больных животных. В стойких очагах, где ежегодно регистрируются заболевания людей, необходима диспансеризация всего поголовья собак с организацией паразитология и серологические их обследования 1—2 раза в год, независимо от того, имеются или отсутствуют клинические, проявления болезни. У 5 — 7% больных собак Лейшманиозы может протекать бессимптомно или с незначительными кожными поражениями.
Борьба с москитами ведётся как против преимагинальных фаз (яйцо, личинка, куколка), так и против окрылённых москитов: благоустройство и очистка территории усадеб, ликвидация мест выплода москитов, применение пологов, а также занавесей на окнах, двери из широкоячеистой сетчатой ткани, импрегнированной репеллентами (ДЭТА) для защиты от залёта москитов, уничтожение москитов в жилых и нежилых помещениях хлорорганическими и фосфорорганическими инсектицидами. При обработках следует учитывать экологические особенности основных переносчиков. При эндофильных переносчиках более эффективна внутренняя обработка жилых помещений, при экзофильных — обработка наружных стен жилых и надворных построек. Меры в отношении переносчика, в том числе применение механических и химических средств защиты от укусов москитов, должны в полном объёме проводиться и в природных очагах.
Кожный лейшманиоз
Имеется множество местных названий болезни, происходящих большей частью от географических наименований (ашхабадская, кокандская, багдадская, восточная язва, алеппский прыщ, пендинская язва, годовик, солек и другие), в прошлом эта болезнь нередко называлась болезнью Боровского.
Кожный лейшманиоз Старого Света
В восточном полушарии имеются два основных клинико-эпидемиологические варианта кожного Лейшманиозы: антропонозный (городской, поздноизъязвляющийся, сухая форма) и зоонозный (сельский, остронекротизирующийся, мокнущая форма). Их возбудителей большинство исследователей рассматривают как самостоятельные виды. Зоонозный кожный Лейшманиозы в свою очередь имеет географические типы со своими клинические, особенностями, позвоночными хозяевами, переносчиками возбудителя и возбудителями, например, кожный Лейшманиозы в Эфиопии.
История. Болезнь впервые стала известна в середине 18 век. В России первое описание болезни, сделанное Н. А. Арендтом, появилось в 1862 год В 80-х годы 19 век в русских войсках в Туркестане наблюдались вспышки кожного Лейшманиозы, которые поражали до 85% личного состава. При их изучении Л. Л. Гейденрейх в 1888 год И. И. Рапчевский в 1889 год впервые отметили отличие пендинской язвы в Мургабском оазисе от заболеваний в других местах Средней Азии.
Иммунитет при кожном Лейшманиозы экспериментально изучали в 1924 год Е. И. Марциновский и А. И. Щуренкова. В 1 929—1933 годы И. И. Гительзон описал туберкулоидный Лейшманиозы и впервые широко применил метод профилактических прививок живым возбудителем, в последующем детально разработанный Туркменским ин-том кожных болезней. Крупным открытием в области эпидемиологии болезни явилось обнаружение в 1939—1940 годы Н. И. Латышевым природной очаговости кожного Лейшманиозы сельского типа. В 1941 год П. В. Кожевников и Н. И. Латышев обосновали нозологический самостоятельность двух типов кожного Лейшманиозы Роль москитов в передаче кожного Лейшманиозы заподозрил в 1911 год частей Веньон, а Е. Сержан (Е. Sergent), Парро (L. Parrot), Донатьен (F. Donatien) в 1921 год экспериментально подтвердили эту роль москитов. Передачу возбудителя через укус москита у песчанок впервые наблюдали в эксперименте Н. И. Латышев и А. П. Крюкова в 1940 год
Географическое распространение.
Антропонозный кожный Лейшманиозы распространён в основном в городах Средиземноморья, Ближнего и Среднего Востока, в западный части Индостанского полуострова. Наиболее активные и мощные очаги известны в азиатской части нозо-ареала — в городах Алеппо, Багдад, Дели, Герат, где ежегодно насчитывались сотни тысяч больных. Во время массовых противомалярийных обработок ДДТ резко снизилась численность москитов, и к началу 60-х годы 20 век снизилась заболеваемость кожным Лейшманиозы; после отмены обработок она вновь стала нарастать.
В СССР в прошлом существовали очаги антропонозного кожного Лейшманиозы в Закавказье (Кировабад, Агдам и другие) и в Средней Азии (Ашхабад, Мары, Андижан, Коканд, Ленинабад и другие). Описаны изолированные очаги в старых сельских населённых пунктах горных районов Памира и Армении. В результате борьбы, проводившейся в 60-х годы в наиболее стойких очагах, а также общего снижения численности москитов в городах свежие случаи антропонозного кожного Лейшманиозы в СССР не регистрируются с 1964—1966 годы
Зоонозный кожный Лейшманиозы широко распространён среди сельских жителей оазисов в пустынных и полупустынных районах Ближнего Востока, Средней Азии, Индии, Северной Африки, в саваннах Западной Африки и в горных районах Восточной Африки. В Эфиопии, например, поражённость населения в некоторых пунктах достигала 20%. В СССР отдельные заболевания зоонозным кожным Лейшманиозы наблюдаются в долинах некоторых рек Марыйской, Ашхабадской, Чарджоуской и Ташаузской областей Туркменской ССР и в Сурхандарьинской, Кашкадарьинской, Бухарской, Сырдарьинской и Джизакской областях Узбекской ССР.
Эпидемиология. Кожный Лейшманиозы — трансмиссивная болезнь, эндемичная в странах с тёплым и жарким климатом. Сезон заражения связан с периодом лёта москитов (в СССР май — октябрь). Среди местного населения болеют главным образом дети, среди приезжих — люди всех возрастов.
Источником возбудителей антропонозного кожного Лейшманиозы являются больные люди. В некоторых очагах Ирана, Ирака, Афганистана болеют также собаки, но эпидемиологические роль, их не выяснена. Возбудитель — L. tropica. Переносчики в большинстве очагов — Ph. sergenti. Заболеваемость не имеет выраженной сезонности из-за большой вариабельности инкубационного периода и обычно не даёт больших вспышек. Резкое увеличение численности переносчика обычно ведёт к росту заболеваемости.
Источником возбудителей зоонозного (сельского) кожного Лейшманиозы с природной очаговостью в разных частях ареала являются многие виды мелких млекопитающих, главным образом грызунов. В большинстве очагов в республиках Средней Азии, в Северном Афганистане, Иране основным источником возбудителей является большая песчанка (Rhombomys opimus), заражённость которой лейшманиями (L. major) достигает 30—100% на всем протяжении её ареала вплоть до Монголии. В некоторых очагах основное значение может иметь краснохвостая песчанка (Meriones libycus), а в Малой Азии, Индии, Северной Африке и другие виды родов Meriones и Psammomys. Среди животных возбудителя переносят москиты разных видов рода Phlebotomus, для которых норы грызунов могут служить местом обитания и выплода. Основной эпидемиологически опасный переносчик в азиатских очагах — Phlebotomus papatasii, численность которого высока в оазисах, низка в засушливых пустынных районах и резко возрастает при обводнении и освоении пустынь.
Заболеваемость зоонозным кожным Лейшманиозы имеет сезонный характер: начинается в мае — июне, достигает максимума в августе — сентябре и заканчивается в ноябре — декабре. Характерна неравномерность распределения заболеваемости на территории природных очагов, а также большие колебания её уровня по времени, связанные с природными и социальными факторами. Холодная зима может повести к резкому снижению численности грызунов и москитов, а следовательно, и к снижению заболеваемости. В период обводнения и освоения пустынь происходит резкое усиление эпидемический опасности природных очагов зоонозного кожного Лейшманиозы Миграция неиммунного населения на территорию природных очагов может приводить к вспышкам Лейшманиозы среди приезжих. Эпидемиологический характеристика очагов зоонозного кожного Лейшманиозы проводится по величине и динамике заболеваемости (возрастной структуре иммунного населения), которую определяют обследованием местного населения на наличие рубцов, а в некоторых странах и с помощью реакции Монтенегро — кожной пробы с лейшманином (взвесь убитых промастигот лейшманий в изотоническом растворе хлорида натрия с 0,25% формалином).
Патогенез. Патологический процесс начинается первично в коже на месте внедрения возбудителя, в результате чего развивается гранулема, названная но П. В. Кожевникову лейшманиомой. Лейшманиома развивается циклически и заканчивается самопроизвольным заживлением: стадия инкубации, пролиферации (папула, бугорок, инфильтрат), деструкции (язва) и репарации (рубцевание). Множественные очаги поражения объясняются как суперинфекцией, в результате которой вслед за первичной возникают так называемый последовательные лейшманиомы, так и многочисленностью одновременных уколов при кровососании самок москитов.
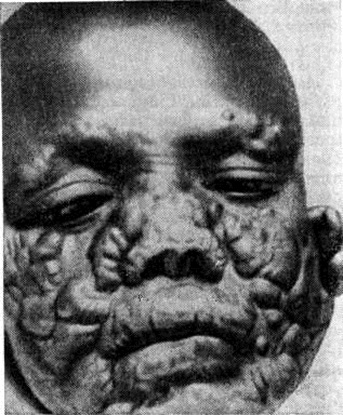
Из первичных очагов поражения лейшмании могут распространяться по лимфатических, путям (до регионарного лимфатических, узла), приводя к образованию бугорков обсеменения, лимфангиитам, лимфаденитам. При кожном Лейшманиозы Старого Света поражение слизистых оболочек наблюдается редко и только при распространении процесса per continuitatem. При кожном Лейшманиозы заболевание может приобретать хронический рецидивирующее течение в виде высыпания мелких сливающихся бугорков в области рубца (туберкулоидный Лейшманиозы). В Эфиопии, а также Венесуэле встречается диффузный (лепроматоидный) кожный Лейшманиозы, при котором процесс из первичного очага поражения распространяется на другие участки кожи, образуя распространённые неизъязвляющиеся и трудно поддающиеся лечению узловатые кожные поражения (рисунок 4).
 |
|  |
Рис. 4. | ||
Патологическая анатомия. Патоморфология двух вариантов кожного Лейшманиозы наряду с общими чертами имеет и особенности. Мощный инфильтрат, развивающийся в толще дермы, имеет характер гранулемы с полиморфным клеточным составом, изменяющимся по ходу процесса.
При антропонозном кожном Лейшманиозы основой процесса является продуктивное воспаление. В первые 6— 8 месяцев инфильтрат состоит из эпителиопдных и гистиоцитарных элементов, имеются гигантские клетки и много лейшманий. Эпителиальный покров постепенно разрушается у верхушки гранулемы, над ней формируется корка. Некроза не наблюдается. При изъязвлении в инфильтрате появляются нейтрофильные лейкоциты, в поздней стадии преобладают лимфоидные и плазматические клетки, лейшманий становится мало, однако в поздних последовательных лейшманиомах с самого начала преобладают лимфоидные и плазматические клетки, лейшмании редки.
При зоонозном кожном Лейшманиозы инфильтрат обширный, диффузный в центре и мелкоузелковый по периферии, захватывает придатки кожи и крупные сосуды, распространяясь вглубь до подкожной клетчатки. Развивается некроз (смотри полный свод знаний), вокруг которого образуется лейкоцитарный вал и узелковые инфильтраты, эпителиоидные или гистиоцитарные с микроабсцессами; паразиты обнаруживаются преимущественно по периферии инфильтрата под сохранившимся эпителием. Наблюдаются акантоз эпителия, роговые жемчужины и кисты. Некротические массы верхних некоторое инфильтрата отторгаются, образуя язву (смотри полный свод знаний). Заживление идёт из глубоких некоторое, формируется грануляционная ткань (смотри полный свод знаний). На 2—3-м месяцев появляется множество пиронинофильных плазматических клеток, фибробластов. Инфильтрат прорастает пучками волокнистой ткани. Количество лейшманий уменьшается. Очаговые лимфогистиоцитарные периваскулярные инфильтраты в дерме сохраняются и после полной эпителизации язвы. Лейшмании в рубце обнаруживались и через 2 года после заживления язвы. Диффузно-инфильтративная форма отличается наличием диффузного инфильтрата в дерме с резкой перифокальной экссудацией сосочкового слоя и более глубоких некоторое соединительной ткани. При туберкулоидном лейшманиозе инфильтрат имеет узелковую структуру с эпителиоидными, лимфоидными и плазматическими клетками, отличающимися слабой пиронинофилией. В соединительной ткани обнаруживаются признаки дезорганизации коллагена, что указывает на значение аутоаллергии в патогенезе этой формы Лейшманиозы Для диффузного кожного Лейшманиозы характерна гистиоцитарная инфильтрация кожи с массой паразитов и отсутствием лимфоидно-плазмоклеточной реакции.
Иммунитет. Естественная невосприимчивость к кожному Лейшманиозы у человека неизвестна. Заболевание ведёт к развитию стойкого, практически пожизненного иммунитета. Повторные заболевания наблюдаются редко (в среднем в 1,7% случаев), но при антропонозном кожном Лейшманиозы почти в 6 раз чаще, чем при зоонозном. Недостаточно напряжённым иммунитет может быть в случаях, когда процесс купируется под влиянием лечения на ранних стадиях. Повторные заболевания кожным Лейшманиозы наблюдались также после длительного применения кортикостероидов. Иммунологический перестройка при антропонозном кожном Лейшманиозы происходит значительно медленнее, чем при зоонозном. Гиперчувствительность замедленного типа при антропонозном кожном Лейшманиозы обнаруживается с 6-го месяцев заболевания; внутрикожная проба с лейшманином становится положительной (гиперемия, отёк и инфильтрат на месте инъекции становятся максимально выраженными через 48 часов). Невосприимчивость к суперинфекции становится полной лишь ко времени рубцевания язвы — к 10—12-му месяцев болезни, то есть после завершения первичного процесса. Суперинфекция, наступившая раньше, вызывает образование последовательных лейшманиом, тем менее выраженных, чем ближе к завершению основного процесса они возникли. Поздние последовательные лейшманиомы могут развиваться абортивно, без изъязвления. Точные сроки исчезновения лейшманий из организма после рубцевания неизвестны. В 2,5—20% случаев антропонозного кожного Лейшманиозы, чаще у детей в возрасте до 12 лет, иммунитет оказывается все же недостаточным; после рубцевания очага первичных поражений в области рубца развивается хронический вяло текущий процесс (туберкулоидный Лейшманиозы).
 |
|  |
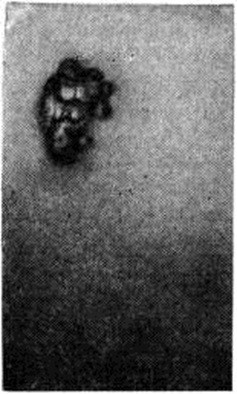
Рис. 5. | ||
При зоонозном кожном Лейшманиозы, протекающем более остро, иммунитет вырабатывается быстрее. Кожная проба становится положительной примерно с 10—15-го дня, а полную невосприимчивость к суперинфекции можно наблюдать уже на стадии язвы, на 3—4-м месяцев заболевания. Циркулирующие антитела при кожном Лейшманиозы обнаруживались нерегулярно и, как правило, в низких титрах в РСК, Реакцию иммунофлюоресценции, реакции преципитации в агаре и лишь в случаях с поражением лимфатических, узлов. Перекрёстный иммунитет между антропонозным и зоонозным кожным Лейшманиозы Старого Света существует. В то же время клинические и экспериментальные данные свидетельствуют об отсутствии перекрёстного иммунитета между болезнями, вызываемыми L. mexicana и L. Braziliensis.
Для большинства форм кожного Лейшманиозы характерно клинической выздоровление при практическом отсутствии антител в крови и раннее появление гиперчувствительности замедленного типа в то время, когда невосприимчивость к повторному заражению ещё не развилась. При экспериментальном изучении на моделях in vivo и in vitro в культурах тканей установлено, что экскретируемые факторы (EF) лейшманий подавляют переваривающую активность макрофагов, благодаря чему паразит имеет возможность размножаться, приводя клетку хозяина к гибели. Иммунные макрофаги способны угнетать размножение лейшманий и даже убивать их. Клеточный иммунитет играет важную роль в защите от паразита.
Клиническая картина. Кожный Лейшманиозы. протекает циклично. Н. Ф. Родякин указывает на общие для обоих вариантов кожного Лейшманиозы клинические, проявления: первичная лейшманиома (стадия бугорка, изъязвления и рубцевания), последовательная лейшманиома (ранняя, поздняя), диффузно-инфильтрирующая лейшманиома и туберкулоид.
При антропонозном кожном Лейшманиозы инкубация составляет 2—8 месяцев, редко дольше (до 3—5 лет), поражение появляется в виде папулы-бугорка, увеличивающегося медленно (к 5— 6-му месяцу до 1—2 сантиметров). Бугорок гладкий, буровато-красный, через 3—5 месяцев появляются чешуйки, через 5—10 месяцев поверхностное изъязвление (рисунок 5). Язва чаще круглая с неровными краями, окружена мощным приподнятым инфильтратом, увеличивающимся до 10—13-го месяцев. Отделяемое скудное, серозно-гнойное, ссыхается в бурую корку. Вокруг язв иногда появляются воспалительные узелки — бугорки обсеменения, изредка лимфангииты. Постепенно инфильтрат уплощается, эпителизация язвы обычно начинается с краёв, рубец красноватый, впоследствии бледнеет. Длительность болезни чаще около 1 года, иногда до 2 лет и более. Число язв 1—3, редко больше.
Клинические, картина последовательных лейшманиом зависит от времени их появления: ранние развиваются параллельно с первичной, поздние — абортивно, без изъязвления. При локализации поражений на лице, стопах и кистях, чаще у пожилых, развиваются диффузно-инфильтрирующие лейшманиомы с небольшим поверхностным изъязвлением, которые, рассасываясь, как правило, не оставляют заметных рубцов.
Туберкулоидная форма клинически напоминает туберкулёзную волчанку, процесс локализуется в основном на лице, в области постлейшманиозного рубца. Основным элементом является желтовато-бурый бугорок (1—3 м), изолированный или сливающийся в бугорковые инфильтраты; одновременно существуют и изъязвляющиеся бугорки, покрытые коркой, и свежие. Начинается процесс чаще в детском возрасте и, периодически обостряясь, может тянуться десятилетиями.
Общее состояние больного при кожном Лейшманиозы, как правило, удовлетворительное, болевые ощущения непостоянны. Нераспавшаяся или покрытая коркой лейшманиома обычно мало беспокоит больного.
При зоонозном кожном Лейшманиозы инкубация не превышает 2 месяцев (чаще 4 недель), бугорок быстро растёт и превращается в фурункулоподобный инфильтрат, красный с нечёткими границами и воспалительной отёчностью кожи вокруг. Рано развивается некроз, распад центральной части бугорка ведёт к образованию кратерообразной язвы, которая быстро увеличивается. В окружающем мощном инфильтрате возникают новые очаги некроза, сливающиеся с основной язвой. Форма и размеры язв разнообразны, края подрытые, отделяемое — серозно-гнойное обильное (цветной рисунок 4). На 3-м месяцев дно язвы очищается и начинают активно расти грануляции, эпителизация идёт обычно с середины, одновременно в нескольких местах. Рассасывание инфильтрата продолжается после полной эпителизации язвы. Бугорки обсеменения, лимфангииты (смотри полный свод знаний) и лимфадениты (смотри полный свод знаний) наблюдаются очень часто. Весь процесс заканчивается к 3—6-му месяцев Поражения обычно множественные (2—5, иногда более десятка), размеры язв варьируют, на туловище язвы обычно крупнее. Локализуются поражения при кожном Лейшманиозы чаще на открытых частях тела — лице, верхних конечностях. Некротизирующиеся язвы при зоонозном кожном Лейшманиозы бывают очень болезненны.
Осложнения. При локализации поражений на нижних конечностях наличие лимфангиитов способствует развитию значительных Отёков стопы, голени из-за нарушения лимфооттока. Бывают рожеподобные явления в области язв и лимфангиитов. Присоединение вторичной инфекции усиливает воспалительные явления, болезненность и может задерживать рубцевание язв.
Диагноз. В эндемичных районах диагноз обычно не представляет затруднений, вне эндемичных зон диагностические ошибки часты. Диагноз основывается на анамнезе (пребывание в эндемических очагах с мая по октябрь), характерной клинические, картине с циклическим развитием поражений и обнаружении возбудителя. Материал для паразитология исследования берут из нераспавшегося бугорка или инфильтрата вокруг язвы. Сдавив участок инфильтрата двумя пальцами для обескровливания, тонким скальпелем поверхностно надрезают эпидермис, берут со дна и краёв надреза соскоб ткани и делают из него мазок на предметном стекле. Мазок высушивают на воздухе, фиксируют спиртом и окрашивают по методу Романовского—Гимзы. Лейшмании обнаруживаются в макрофагах и внеклеточно, при антропонозном кожном Лейшманиозы— в большом количестве, при зоонозном кожном Лейшманиозы— в меньшем. К концу заболевания количество паразитов уменьшается. При туберкулоидном Лейшманиозы они обнаруживаются с большим трудом, в этом случае метод выделения культуры лейшманий и биопроба (внутрикожное заражение белых мышей или хомяков) более эффективны.
Дифференциальный диагноз. Кожный Лейшманиозы может имитировать многие дерматозы: фурункулёз (смотри полный свод знаний), хронический пиодермию (смотри полный свод знаний), паропихию (смотри полный свод знаний), туберкулёзную волчанку (смотри полный свод знаний Туберкулёз кожи) и красную волчанку (смотри полный свод знаний), бугорковый сифилис (смотри полный свод знаний), сосочковый рак (смотри полный свод знаний Кожа, опухоли) и другие
Лечение. Выбор способа лечения зависит от формы и стадии болезни. При антропонозном кожном Лейшманиозы на стадии бугорка (до 3 месяцев) хорошие результаты даёт метод, предложенный Н. В. Добротворской (1941): обкалывание бугорка 3—5% раствором акрихина в 0,5—1% растворе новокаина 2—3 раза с интервалом в 3 недель Инъекции делают строго внутрикожно, при неполном пропитывании инфильтрата возможны рецидивы. Обкалывание изъязвляющихся лейшманиом неэффективно. В ряде зарубежных стран применяют обкалывание одиночных поражений берберинсульфатом.
Для лечения зоонозного кожного Лейшманиозы широко применяют мономицин, который вводят внутримышечно, взрослым по 250 000 ЕД, детям из расчёта 4000—5000 единиц на 1 килограмм веса больного в 4—5 миллилитров 0,5% раствора новокаина, 3 раза в сутки с интервалом между введениями 8 часов Длительность лечения 10—12 дней, курсовая доза 7 — 9 миллионов единиц для взрослых. Обязательны анализ мочи и контроль состояния слуха. В редких случаях рецидивов лечение можно повторить через 2 недель Внутримышечное лечение можно сочетать с местным применением мономицина в виде 2—3% мази на ланолиново-вазелиновой основе. Туркменский ин-т кожных болезней получал выраженный лечебный эффект при пероральном введении аминохинола увеличенными дозами. Институт также рекомендует метациклин, оказывающий, помимо специфического, бактерицидное действие на сопутствующую микробную флору лейшманиозных язв. Наружное лечение с частой сменой сначала влажно-высыхающих дезинфицирующих повязок, а затем повязок с различными дезинфицирующими мазями способствует более быстрому очищению язв и их эпителизации. При кожном Лейшманиозы и особенно при туберкулоидной форме применяют также лечение солюсурьмином, которое проводят в условиях стационара. Солюсурьмин вводят ежедневно внутривенно в виде 20% раствора, доза зависит от возраста. Полная суточная доза 0,35—0,5 миллилитров на 1 килограмм веса, в 1-й и 2-й день вводят соответственно 1/3 и 2/3 лечебный дозы. Курсовая доза в зависимости от возраста 7—9 миллилитров на 1 килограмм веса, длительность курса в среднем 3—4 недель
Прогноз. Кожный Лейшманиозы не представляет опасности для жизни. При антропонозном кожном Лейшманиозы может развиться туберкулоидный Лейшманиозы, длительно протекающий и трудно поддающийся лечению. При локализации процесса на лице, особенно на носу, долго протекающие большие уродующие инфильтраты, язвы и деформирующие рубцы оставляют значительный косметический дефект. При зоонозном кожном Лейшманиозы самопроизвольное полное выздоровление наступает через 3—6 месяцев. На стадии язвы, особенно при множественных поражениях и локализации на нижних конечностях, в области суставов и на пальцах рук, заболевание может вызвать длительную потерю трудоспособности (2—2½ месяцев).
Профилактика. При выборе мероприятий учитывают характер очага, условия контакта людей с природными очагами, эффективность и экономические возможности их проведения. В СССР в очагах антропонозного кожного Лейшманиозы полное выявление и лечение больных, противомоскитные обработки инсектицидами в течение нескольких лет, благоустройство территории для ликвидации мест выплода москитов привели практически к полной ликвидации свежей заболеваемости антропонозным кожным Лейшманиозы. С целью предупреждения возможной активизации ликвидированных очагов необходимы выявление, диспансеризация и повторное лечение небольшого числа оставшихся больных туберкулоидным кожным Лейшманиозы, а при наличии москитов — очаговая дезинсекционная обработка (дома, усадьбы больного).
В сельской местности при борьбе с зоонозным кожным Лейшманиозы противомоскитные мероприятия мало эффективны. Основной мерой борьбы в этих случаях является истребление большой песчанки. Впервые такой опыт был поставлен Н. И. Латышевым в 1939 — 1940 годы в Туркмении. Уничтожение большой песчанки на территории радиусом l½ километра вокруг посёлка Ташкепри при обработке нор хлорпикрином снизило заболеваемость в ближайшем эпидемический сезоне с 70 до 0,4%. В 60-е годы 20 век в Узбекистане проводили многократные затравки нор (пшеница с 10— 15% фосфида цинка) в 2—3-километровой зоне вокруг поселков. Прекращение мероприятий обычно вело к быстрому заселению территории грызунами и возобновлению заболеваемости. Эффективность профилактики достигается полной ликвидацией природных очагов болезни на достаточно больших территориях в пределах старых оазисов и на осваиваемых участках пустынь. Это стало возможным при широком мелиоративном благоустройстве территории в процессе её хозяйственного освоения; истребление же песчанок ведётся лишь на тех ограниченных неосваиваемых участках, которые изолированы от пустыни естественными или искусственными преградами (каналы, пашни), препятствующими миграции грызунов.
Индивидуальная профилактика включает механическую и химическую защиту от нападения москитов (пологи, занавеси и сетки из крупноячеистой ткани, обработанные репеллентами). Иммунопрофилактика разработана в СССР на основе исследований Е. И. Марциновского и А. И. Щуренковой, А. П. Лаврова и П. А. Дубовского, А. Н. Соколовой, Н. Ф. Родякина. Для прививок применяют живую вирулентную культуру возбудителя зоонозного кожного Лейшманиозы. Прививают обычно лиц, подвергающихся высокому риску заражения. Прививки проводят в осенне-зимний период, но не позднее чем за 3 месяцев до выезда в очаги. Прививочный материал вводят внутрикожно, на закрытом участке тела (плечо, бедро), после чего развивается местное поражение (цветной таблица, т. 13, рисунок 5), протекающее обычно легче и несколько быстрее, чем естественное заболевание. В результате к 3-му месяцев после начала прививочного процесса вырабатывается прочный, практически пожизненный иммунитет.
Кожный лейшманиоз Нового Света
Кожный Лейшманиозы Нового Света включает следующие клинико-эпидемиологические варианты: ута, язва чиклеров, кожный Лейшманиозы в бассейне р. Амазонки, эспундия, «лесная фрамбезия» и другие Эспундию, «лесную фрамбезию» и некоторые другие варианты, при которых могут возникать поражения слизистых оболочек, часто называют кожно-слизистым Лейшманиозы
Географическое распространение. Кожные варианты Лейшманиозы распространены в засушливых долинах на западный склонах Анд в Перу (ута); во влажных низменных лесах Центральной Америки: Мексика, Гватемала, Гондурас и другие (язва чиклеров); в Северной Бразилии; единичные случаи описаны на юге США (в штате Техас). Кожно-слизистые варианты Лейшманиозы встречаются к востоку от Анд, в лесистых районах Бразилии, Перу, Эквадора, Венесуэлы, Боливии, Парагвая (эспундия), в Гайане, Суринаме («лесная фрамбезия»). В Панаме известны оба варианта. Заболеваемость обычно спорадическая, при освоении лесных массивов, строительстве дорог перерастает в эпидемии. По данным ВОЗ, за 1950—1965 годы за-регистрировано более 10 тысяч случаев кожного Лейшманиозы в Бразилии, более 3,5 тысяч — в Колумбии, 7 тысяч— в Парагвае.
Эпидемиология изучена лишь для некоторых вариантов кожного Лейшманиозы западного полушария.
Ута — синантропный зооноз; источник возбудителя собаки, заболеваемость резко снижена в результате обработки усадеб инсектицидами.
Все остальные варианты кожного Лейшманиозы западного полушария — природноочаговые зоонозы. Хранителями возбудителей являются мелкие лесные млекопитающие (главным образом грызуны, а также опоссумы, ленивцы, древесные дикобразы). Люди заражаются через антропофильных москитов. Источником возбудителей кожного Лейшманиозы в Бразилии и Тринидаде являются лесные грызуны рода Oryzomys, возбудитель — L. m. amazonensis, переносчик — москиты Lutzomyia flaviscutellata. В Панаме имеется два варианта кожного Лейшманиозы: на востоке перешейка — кожный Лейшманиозы, возбудителем которого является L. теxicana, позвоночными хозяевами — мелкие лесные грызуны, переносчиком Lutzomyia olmeca; в лесах остальной части страны распространён кожный Лейшманиозы, при котором иногда вторично поражаются слизистые оболочки, возбудитель — L. braziliensis раnamensis, а позвоночные хозяева — разные виды древесных млекопитающих, в том числе хищники, приматы, неполнозубые, переносчики — 4 вида москитов.
Эпидемиология эспундии мало изучена. Источниками возбудителей, возможно, являются ленивцы, агути, пака и другие. Поражаются люди всех возрастов, обычно заболевание связано с работой в лесу (сборщики каучука, заготовители леса), охотой и освоением новых земель.
Патогенез. Заболевание протекает циклически, подобно кожному Лейшманиозы Старого Света, с образованием язвы и самопроизвольным рубцеванием за 6—12 месяцев и развитием невосприимчивости к повторным заражениям; при поражении хрящевой ткани (локализация процесса на ушах) течение становится хроническим. При эспундии, «лесной фрамбезии» и другие вариантах первичные кожные поражения также рубцуются, а затем возбудитель метастатически поражает слизистые оболочки, вызывая прогрессирующий трудно-излечивающийся процесс.
Патологическая анатомия. Патологоанатомическая картина — как при кожных Лейшманиозы Старого Света.
Иммунитет. Шо и Лейнсон (J. Shaw, R. Lainson) в 1975 год показали, что экзоантиген (антиген, выделяемый паразитом в окружающую среду) вызывает как немедленную, так и замедленную реакцию, причём первая наблюдается чаще на ранней фазе болезни (до 6 месяцев), поэтому кожная проба с экзоантигеном может применяться для диагностики ранних стадий кожного Лейшманиозы Нового Света.
Клиническая картина. Ута — единичные язвы, рубцующиеся в течение года. Язва чиклеров — единичные поражения, быстро заживающие; в 50% случаев локализуются на ушах, при этом процесс развивается длительно, приводя к разрушению ушной раковины. Амазонский кожный Лейшманиозы — самоизлечивающиеся кожные язвы на нижних конечностях.
При «лесной фрамбезии», эспундии появляются одиночные или множественные поражения (узлы, язвы) чаще на конечностях, заживающие рубцом, после чего в разные сроки обнаруживаются поражения слизистых оболочек с изъязвлением, образованием полипов («нос тапира») или с глубокими разрушениями мягких тканей и хрящей носоглотки, гортани, трахеи. До 50% случаев поражения слизистых оболочек наблюдается при «лесной фрамбезии», до 80% — при эспундии. Диффузный кожный Лейшманиозы — хронический процесс, развивающийся на фоне иммунодефицита, начинается с одиночного поражения и медленно распространяется по лицу и конечностям в виде лепроматоидных неизъязвляющихся узлов, при этом кожная проба с лейшманином отрицательная.
Диагноз ставят на основании обнаружения возбудителя в поражённых коже и слизистых оболочках и положительной кожной пробы с лейшманином (реакция Монтенегро). Результаты серо л. реакций разноречивы.
Дифференциальный диагноз проводят с сифилисом (смотри полный свод знаний), лепрой (смотри полный свод знаний), фрамбезией (смотри полный свод знаний), туберкулёзом кожи (смотри полный свод знаний), фузоспириллезом слизистых оболочек, споротрихозом (смотри полный свод знаний), южноамериканским бластомикозом (смотри полный свод знаний), эпителиомой (смотри полный свод знаний).
Лечение. Эспундия трудно поддаётся лечению; применяют препараты пятивалентной сурьмы (глюкантим), а также амфотерицин В. При диффузном процессе назначают пентамидин изотионат и амфотерицин В.
Прогноз. При кожных формах — спонтанное выздоровление, при эспундии прогноз неблагоприятный, течение тяжёлое длительное с обезображиванием лица и, как правило, с летальным исходом.
Профилактика. При работе в лесу необходима индивидуальная защита от нападения москитов (защитные сетки, репелленты). Специфическая профилактика не разработана.
|
Неллина О.И. |

|
⇐ Перейти на главную страницу сайта |
⇑ Вернуться в начало страницы ⇑ |
Библиотека Ordo Deus ⇒ |
⇐ Лейомиосаркома |
⇓ Полный свод знаний. Том первый А. ⇓ |
Лекарственная аллергия ⇒ |
|
Все статьи в полном изложении, Вы можете найти в большой медицинской энциклопедии — Главный редактор: академик АН СССР (РАН) и АМН СССР (РАМН) Б.В. Петровский. — Москва издательство «Советская энциклопедия» 1989г. |
|
Внимание! Вы находитесь в библиотеке «Ordo Deus». Все книги в электронном варианте, содержащиеся в библиотеке «Ordo Deus», принадлежат их законным владельцам (авторам, переводчикам, издательствам). Все книги и статьи взяты из открытых источников и размещаются здесь только для чтения. |
|
Вся информация на сайте Ordo Deus находится в свободном доступе. Ordo Deus не предоставляет информацию на платной основе. |
|
Все авторские права сохраняются за правообладателями. Если Вы являетесь автором данного документа и хотите дополнить его или изменить, уточнить реквизиты автора, опубликовать другие документы или возможно вы не желаете, чтобы какой-то из ваших материалов находился в библиотеке, пожалуйста, свяжитесь с нами по e-mail: |
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы не желаете закончить свой жизненный путь в виде омерзительной гниющей органической массы пожираемой копошащимися в ней могильными червями? Вы желаете вернувшись в молодость прожить ещё одну жизнь? Начать всё заново? Исправить совершённые ошибки? Осуществить несбывшиеся мечты? Перейдите по ссылке: «главная страница».
|
© Ordo Deus, 2010. При копировании ссылка на сайт http://www.ordodeus.ru обязательна. |