Вальденстрема болезнь |
||
 |
 |
Оглавление
|
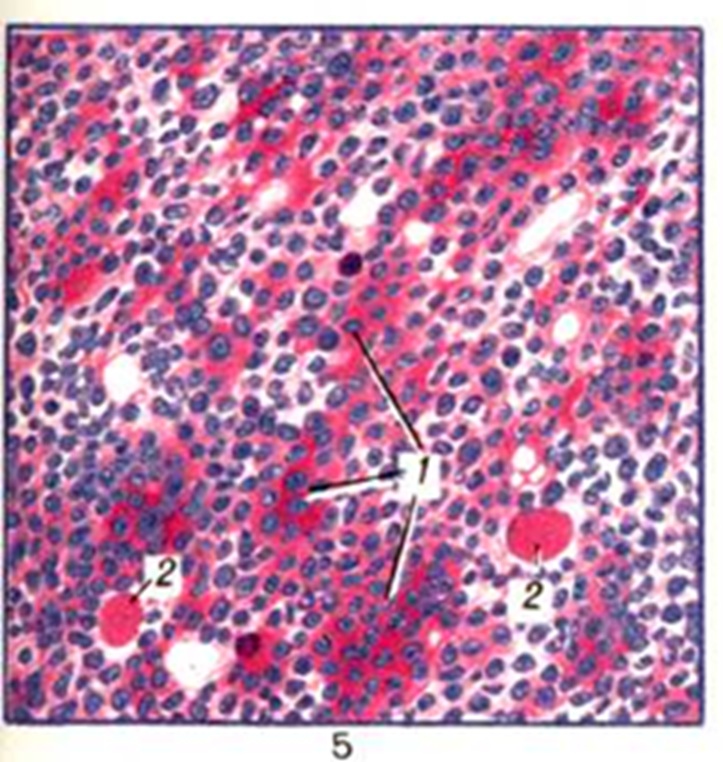
Вальденстрема болезньВальденстрема болезнь (J. G. Waldenstrom, род. в 1906 г., шведский терапевт; синонимы: Вальденстрема макроглобулинемия, макроглобулинемический ретикулёз, макроглобулинемический ретикулолимфоматоз, макроглобулиновый ретикулёз) — системное заболевание органов кроветворения, характеризующееся неопластической пролиферацией лимфоидных элементов иммунокомпетентной клеточной системы в костном мозге, лимфатических, узлах, селезёнке а также в других органах и тканях и сопровождающееся гиперпродукцией иммуноглобулина класса IgM (макроглобулина). Заболевание развивается в возрасте 40—70 лет, преимущественно у мужчин. Частота его среди населения не уточнена. Этиология и патогенез Вальденстрема болезнь рассматриваются в общем аспекте этиологии и патогенеза лейкозов (смотри Лейкозы). В сообщениях последних лет о семейной предрасположенности к диспротеинемиям (в числе которых описывается и Вальденстрема болезнь) приводятся данные о нарушении генетической регуляции синтеза иммуноглобулинов и наличии мутации в иммунокомпетентной клеточной системе. Кариологические исследования не выявляют специфических геномных нарушений, хотя некоторые авторы [Боттура (С. Bottura)] обнаруживают в клетках костного мозга больных большую экстрахромосому (Mg-хромосома); последнюю рассматривают как маркер макроглобулинсекретирующего клеточного клона. Патологическая анатомия. Характерна распространённая пролиферация клеток, наиболее выраженная в лимфатических, узлах, костном мозге, селезёнке, печени, желудке, кишечнике, а также в подкожной и жировой клетчатке, веществе и оболочках головного мозга и в других органах. При аутопсии обнаруживается умеренное увеличение лимфатических, узлов, чаще глубоких, размер которых редко превышает 20 миллиметров; иногда — их универсальное увеличение. Встречаются узловатые разрастания в области средостения, в брыжейке. Часто отмечают гепатоспленомегалию, множественные кровоизлияния в головном мозге, слизистых оболочках и серозных покровах, лёгких и других органах. При микроскопии в лимфатических, узлах наблюдается стирание рисунка в связи с массивной пролиферацией клеток типа лимфоидных, число фолликулов резко уменьшено; при обзорных окрасках фолликулы полностью не различимы; капсула лимфатических, узла и окружающая жировая клетчатка также инфильтрированы лимфоидными клетками. При импрегнации серебром по Папу, Гомори или Футу выявляется относительно сохранённая строма, представленная утолщёнными ретикулиновыми волокнами с резко выраженной аргентофилией, особенно по периферии лимфатических, узлов. В участках инфильтрации выявляются лимфоциты разной зрелости, лимфоидно-ретикулярные (по классификации Рора) и плазматические клетки. Обнаруживаются также гистиоциты, тучные клетки, макрофаги (цветной рисунок), в цитоплазме последних нередко содержатся шаровидные коагуляты, окрашивающиеся гематоксилин-эозином и при ШИК-реакции в розовый, а иногда в зеленоватый цвет. Характерны глыбчатые и аморфные ШПК-положительные включения в ядрах и цитоплазме лимфоцитов, плазматических и ретикулярных клеток. Пролиферация клеток в костном мозге и селезёнке носит очаговый или диффузный характер. В отличие от миеломы, массивное разрушение костной ткани при Вальденстрема болезнь наблюдается редко. Пролиферация клеток в строме почек сочетается с утолщением мембран клубочков, наличием аморфных белковых масс, иногда закрывающих просвет капилляров. В таких случаях при флюоресцентной микроскопии со специфическими сыворотками в области сосудистых петель клубочков обнаруживается свечение. В просветах канальцев — белковые цилиндры; в клетках эпителия — выраженные дистрофические изменения. В сосудах различных органов можно видеть белковые преципитаты с пропитыванием сосудистой стенки и окружающих тканей белком. Клиническая картина заболевания слагается из признаков системной гиперплазии лимфоидной ткани и симптомов, связанных с циркуляцией в кровеносном русле избытка высокомолекулярного белка — JgM. Больные часто отмечают кровоточивость из носа, дёсен, кровоизлияния в кожу, ослабление зрения, чувство тяжести в голове. Иногда жалобы ограничиваются указанием на общую слабость и недомогание. Обнаруживается умеренное увеличение подкожных лимф, узлов, увеличение селезёнки и печени. Костные изменения редки. |
Рентгенологически иногда выявляются мелкие очаги деструкции в плоских и трубчатых костях на фоне общего пороза; редко деструктивный процесс напоминает множественную миелому. Картина крови не типична: часто наблюдается нормохромная, нормоцитарная анемия, нерезкий лейкоцитоз с лимфоцитозом и умеренным моноцитозом; в ряде случаев — лейкоцитарная формула нормальна. Характерна резко ускоренная РОЭ: 50—70 мм/час.
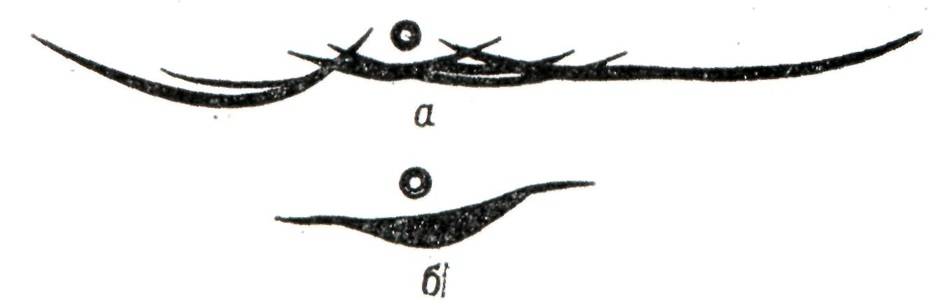
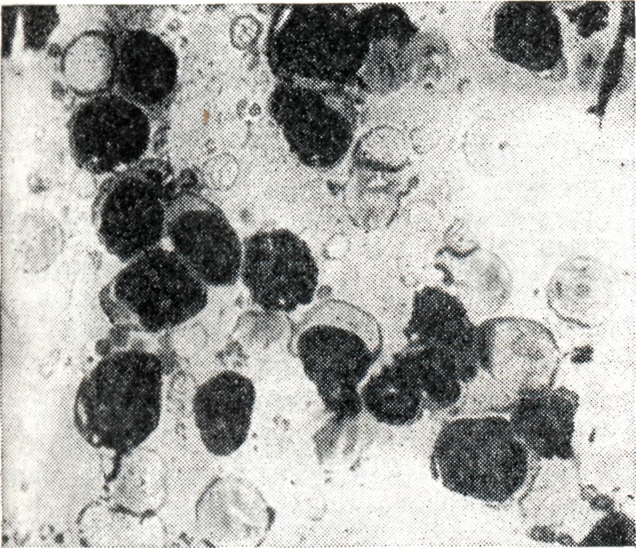
В пунктате костного мозга — до 40—70% клеток лимфоидного ряда, которые под световым микроскопом не отличимы на первый взгляд от нормальных лимфоцитов. Однако многие из них характеризуются эксцентрично расположенным ядром (рисунок 1) с нежнопетлистой сетью хроматина. Цитоплазма клеток резко базофильна, с наличием зоны просветления; в ней часто видны мелкие вакуоли, иногда светлые включения; если последние занимают почти всю цитоплазму, оттесняя ядро к периферии, клетка приобретает вид виноградной грозди (grape cell).
 |
 |
 |
Рис. 1. | ||
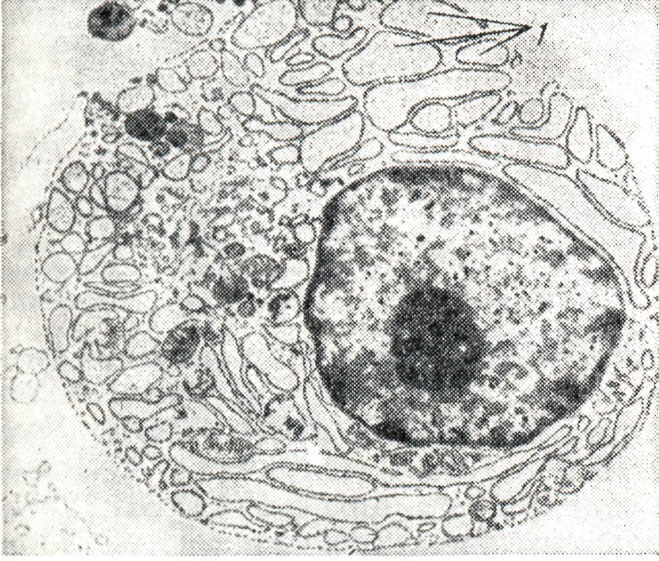
Сочетание в одной клетке морфологических признаков ретикулярной, плазматической клетки и лимфоцита дало основание некоторым авторам обозначить ее как лимфо-ретикулярную клетку, лимфоплазмоцит, гистолимфоплазмоцит, протеинлимфоцит. При исследовании под электронным микроскопом в указанных лимфоидных элементах обнаруживают развитые структуры эндоплазматической сети (рисунок 2) с «сидящими» на мембранах полирибосомами, что свидетельствует об активной белковообразующей функции этих клеток. Зрелость ядер (по распределению хроматина и наличию нуклеол) неодинакова в различных клетках. Характерно увеличение в сыворотке крови общего белка (до 9—12 г%), однако это увеличение не достигает уровня гиперпротеинемии при миеломной болезни.
Циркуляция в кровяном русле большого количества (до 4—5 г%) грубодисперсного белка обусловливает повышенную вязкость крови, что ведёт к замедлению скорости кровотока и развитию стазов в мелких сосудах с последующим тромбообразованием и разрывом сосудистой стенки. Последнее клинически проявляется возникновением ретинопатии, церебропатии, кровоточивости и другие. При офтальмоскопировании глазного дна можно увидеть расширенные извитые сосуды с перетяжками, микроаневризмами и множественными кровоизлияниями по их ходу (fundus paraproteinaemicus). Аналогичные стазы в сосудах головного мозга могут привести к так наз. макроглобулинемической парапротеинемической коме — развитию сопорозного состояния при отсутствии очаговой неврологической симптоматики. Обычно при этом состоянии усиливаются проявления геморрагического синдрома. Кровоточивость может быть обусловлена как функциональной неполноценностью тромбоцитов, окутанных «муфтой» из белка, так и торможением активности отдельных факторов свёртывающей системы избытком макроглобулина.
По течению заболевания Мак-Каллистер (В. D. McCallister) с соавторами выделяет три формы Вальденстрема болезнь: прогрессирующую, медленно прогрессирующую и бессимптомную. Для первых двух форм характерна вся вышеизложенная симптоматика, различается она только по времени появления их. Продолжительность заболе¬вания составляет в среднем 3—5 лет (Мак-Каллистер с соавторами), по отдельным наблюдениям — до 10 и более лет. Бессимптомная форма наблюдается, как правило, у лиц в возрасте старше 60 лет и отличается отсутствием клинических признаков заболевания, сравнительно невысоким содержанием макроглобулина IgM. В крови выявляется ускорен¬ная РОЭ, иногда умеренная анемия. В костном мозге — незначительное увеличение количества лимфоцитов и плазматических клеток. Длительное доброкачественное течение позволяет некоторым авторам выделить эту форму Вальденстрема болезнь под названием эссенциальной доброкачественной макроглобулинемии. Однако иногда, после более чем 10 лет бессимптомного течения, развивается типичная картина Вальденстрема болезнь, что даёт основание считать эту форму преклинической стадией заболевания. Некоторые авторы выделяют злокачественную форму Вальденстрема болезнь, продолжительность которой не превышает 2½ лет.
Осложнения возникают на фоне и в связи со специфической инфильтрацией органов лейкозными (лимфоидными) клетками, нарушением микроциркуляции крови в кровеносных сосудах и дефицитом нормальных иммуноглобулинов. Последнее обусловливает так называемый синдром недостаточности антител (иммунодефицитный синдром, «иммунный парез» по Пенни).
Поражение почек выражается в нарушении клубочковой фильтрации и канальцевой реабсорбции. Редко наблюдается почечная недостаточность с уремической интоксикацией. Поражение дыхательного аппарата связано с лимфоидными инфильтрациями, лёгочным диспротеинозом и присоединяющимися инфекциями. Боллинелли (R. Bollinelli) различает специфические инфильтративные, инфекционные и смешанные пневмопатии
Часто поражается печень (гепатомегалия, желтуха), что, возможно, связано с агломерацией макроглобулинов в сосудах печени в сочетании с лимфоидной интерстициальной инфильтрацией. Нередко отмечают генерализацию инфекционного процесса с развитием общего сепсиса.
Диагноз. При наличии клинических симптомов и увеличении количества общего белка сыворотки решающим в диагностике является выявление М-градиента на электрофореграмме сывороточных белков.
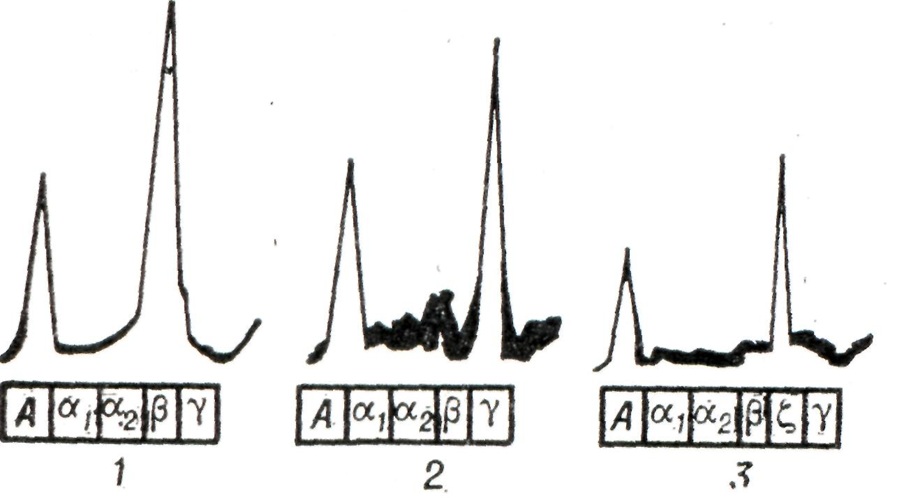
При электрофорезе белков (смотри Электрофорез) на бумаге или поли-акриламидном геле выявляется узкая полоса (рисунок 3), а при электрофорезе со свободной границей — узкий высокий пик (М-градиент) в зоне γ-, (β-глобулинов или между ними (рисунок 4). Идентификация макроглобулина (IgM) производится с помощью иммунного электрофореза с моноспецифической антисывороткой против IgM (рисунок 5) или методом седиментационного анализа (молекулярный вес 900 000 и более, константа седиментации 19S).
 |
 |
 |
Рис. 3. | ||
Дифференциальная диагностика чаще всего проводится с миеломной болезнью. При последней также выявляется М-градиент, однако он относится и к другим классам иммуноглобулинов (G, A, D, Е). Кроме того, для миеломной болезни характерны изменения в костях, выраженное увеличение плазматических клеток в костном мозге.
Необходимо различать вторичную (симптоматическую, факультативную) макроглобулинемию, которая иногда наблюдается при раке, различных формах коллагенозов, аутоагрессивных (люпоидный) гепатитах, циррозах печени и другие Дифференциальная диагностика строится на преобладании клинических симптомов основного заболевания и отсутствии клинических и морфологических признаков (по данным пункции, костного мозга, трепанобиопсии и биопсии лимфатических, узлов) Вальденстрема болезнь.
Прогноз в значительной мере определяется характером течения, выраженностью геморрагических и инфекционных осложнений. Полного выздоровления при Вальденстрема болезнь, как и при всяком лейкозном процессе, не наблюдается, однако при отсутствии выраженных геморрагии и септических осложнений больные длительное время (до 9—13 лет) остаются ограниченно трудоспособными.
Лечение направлено на подавление с помощью цитостатических препаратов лимфоидной инфильтрации, на борьбу с анемией, кровоточивостью и сопутствующими инфекционными осложнениями. При прогрессирующем течении заболевания применяется лейкеран (хлораминофен, хлорбутин), который при нормальном количестве лейкоцитов назначается по 6 миллиграмм в сутки; при наклонности к лейкопении доза уменьшается до 4 миллиграмм, при сублейкемической картине крови — повышается до 10—12 миллиграмм. Поддерживающие дозы устанавливаются в зависимости от динамики изменения состава крови и основных клинических симптомов. Лечение продолжается практически в течение всей жизни больного при отсутствии противопоказаний (глубокая анемия, тромбоцитопения). При значительном, особенно опухолевидном, увеличении лимф, узлов применяют циклофосфамид (циклофосфан, эндоксан) в примерной дозе 200 мг в сутки (6 —10 г на курс).
Цитостатическую химиотерапию нередко сочетают с периодическими курсами глюкокортикоидных гормонов в дозах, соответствующих 40—60 миллиграмм преднизолона в сутки с постепенным уменьшением к концу курса.
При кровоточивости применяют интенсивный плазмаферез (смотри) 2— 3 раза в неделю (не менее 10 процедур на курс) на фоне или перед лечением лейкераном. За одну процедуру удаляют от 600 до 1800 миллилитров плазмы. Плазмаферез обычно сочетают с гемотрансфузиями. При инфекционных осложнениях применяют антибиотики (предпочтительнее с широким спектром действия) в больших дозах; стандартный гамма-глобулин вводится внутримышечно по 6—8 доз ежедневно или через день по 10—20 инъекций на курс. Целесообразно вводить внутривенно гамма-глобулин, лишённый с помощью энзимного расщепления фрагмента молекулы IgG комплементарной ак¬тивности. При медленно прогрессирующем течении лечение то же, но менее интенсивное. При бессимптомной форме лечение не проводится.
При опухолевой (саркоматозной) трансформации процесса принципы лечения те же, что и при ретикулосаркоме (смотри).
|
Мокеева P.А.; Неменова Н.М. |

|
⇐ Перейти на главную страницу сайта |
⇑ Вернуться в начало страницы ⇑ |
Библиотека Ordo Deus ⇒ |
⇐ Вакцинальная болезнь |
⇓ Полный свод знаний. Том первый А. ⇓ |
Ван-дер-Хуве синдром ⇒ |
|
Все статьи в полном изложении, Вы можете найти в большой медицинской энциклопедии — Главный редактор: академик АН СССР (РАН) и АМН СССР (РАМН) Б.В. Петровский. — Москва издательство «Советская энциклопедия» 1989г. |
|
Внимание! Вы находитесь в библиотеке «Ordo Deus». Все книги в электронном варианте, содержащиеся в библиотеке «Ordo Deus», принадлежат их законным владельцам (авторам, переводчикам, издательствам). Все книги и статьи взяты из открытых источников и размещаются здесь только для чтения. |
|
Библиотека «Ordo Deus» не преследует никакой коммерческой выгоды. |
|
Все авторские права сохраняются за правообладателями. Если Вы являетесь автором данного документа и хотите дополнить его или изменить, уточнить реквизиты автора, опубликовать другие документы или возможно вы не желаете, чтобы какой-то из ваших материалов находился в библиотеке, пожалуйста, свяжитесь с нами по e-mail: |
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы не желаете закончить свой жизненный путь в виде омерзительной гниющей органической массы пожираемой копошащимися в ней могильными червями? Вы желаете вернувшись в молодость прожить ещё одну жизнь? Начать всё заново? Исправить совершённые ошибки? Осуществить несбывшиеся мечты? Перейдите по ссылке: «главная страница».
|
© Ordo Deus, 2010. При копировании ссылка на сайт http://www.ordodeus.ru обязательна. |